Clear Sky Science · nl
Rottlerin veroorzaakt dubbele afbraak van SLC7A11 en GPX4 om ferroptose en chemosensibilisering in hepato‑cellulair carcinoom te stimuleren
Waarom deze natuurlijke verbinding belangrijk is voor leverkanker
Hepato‑cellulair carcinoom, de meest voorkomende vorm van primaire leverkanker, wordt vaak laat gediagnosticeerd en blijft moeilijk te behandelen. Deze studie onderzoekt of een uit planten afgeleide molecule genaamd rottlerin, lang bekend om zijn brede antikanker‑effecten, kan worden benut om een nieuwere vorm van celdood, ferroptose, in leverkankercellen te induceren. Door te begrijpen hoe rottlerin op moleculair niveau werkt, hopen de onderzoekers nieuwe wegen te openen voor effectievere therapieën die minder snel resistentie opleveren.
Een nieuwe manier om kankercellen te doden
Traditionele anticancermiddelen duwen tumorcellen meestal richting bekende doodsprogramma’s zoals apoptose. Ferroptose is anders: het is een ijzerafhankelijk proces dat wordt aangedreven door de ophoping van toxische lipiden in celmembranen. Leverkankercellen zijn bijzonder kwetsbaar voor dit type schade omdat ze sterk leunen op antioxidant‑systemen om deze vetgebaseerde toxines onder controle te houden. Het team vroeg zich af of rottlerin die verdedigingsmechanismen kon saboteren en zo leverkankercellen tot ferroptose kon dwingen.
Hoe rottlerin de tumorgroei vertraagt
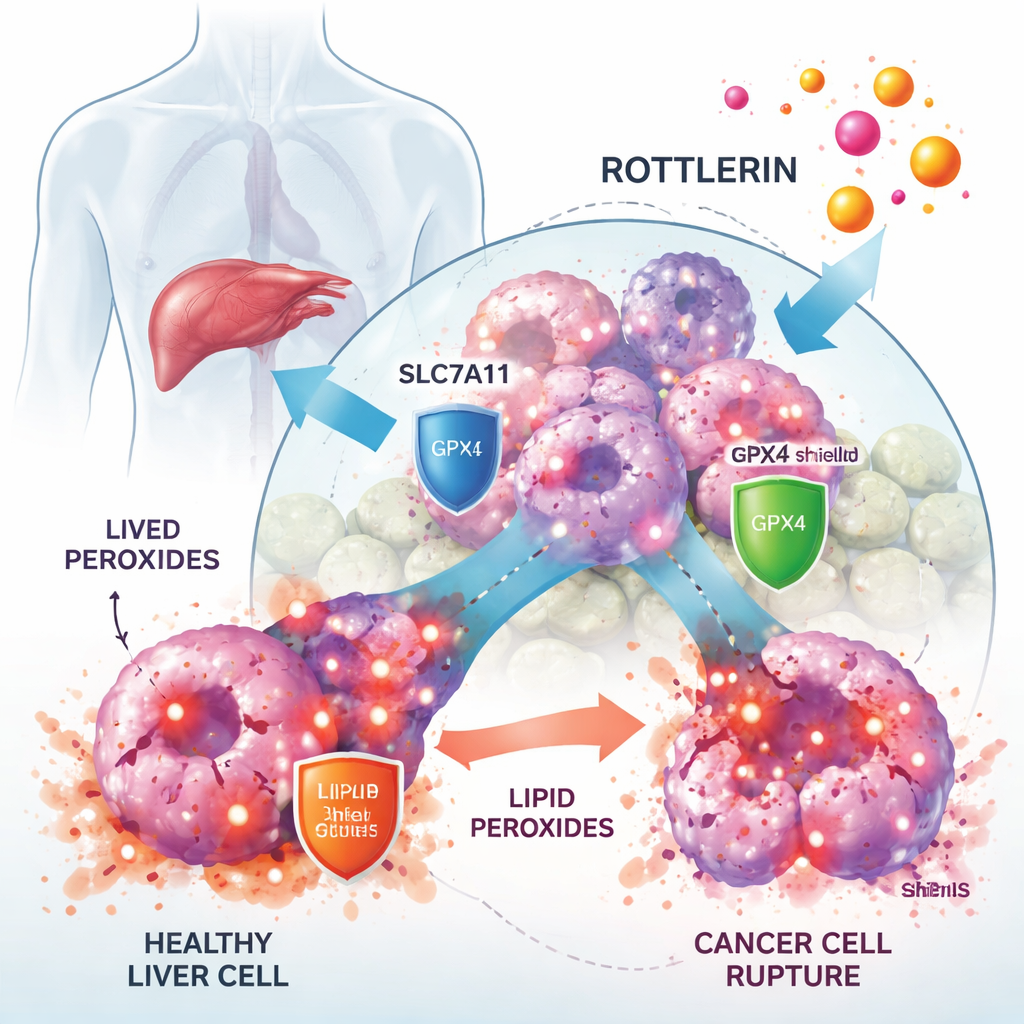
In experimenten met menselijke leverkankercelijnen toonden de onderzoekers aan dat rottlerin de groei van kankercellen sterk verminderde bij lage micromolaire concentraties, terwijl normale levergerelateerde cellen minder werden aangetast. Toen ze een specifieke ferroptose‑remmer, Ferrostatin‑1, toevoegden, werd een groot deel van de door rottlerin geïnduceerde celdood gereduceerd, wat sterk suggereert dat ferroptose de belangrijkste dodelijke route was. Microscopie en biochemische tests ondersteunden dit: rottlerin‑behandelde cellen stapelden hoge niveaus lipidperoxiden op, vertoonden veranderde mitochondriën en hadden gereduceerde hoeveelheden van het antioxidant glutathion—allemaal kenmerken van ferroptose.
De antioxidant‑schilden van de cellen ontwapenen
Leverkankercellen overleven door te steunen op een cruciale verdedigingsas opgebouwd uit de transporter SLC7A11 en het enzym GPX4. SLC7A11 voert cystine binnen, een bouwsteen voor glutathion, terwijl GPX4 glutathion gebruikt om lipidperoxiden te neutraliseren voordat ze membranen beschadigen. De studie vond dat rottlerin zowel SLC7A11‑ als GPX4‑proteïnen over de tijd deed afnemen. Dit kwam niet doordat de cellen stopten met het aanmaken ervan, maar doordat de eiwitten werden gemarkeerd met kleine “vernietig mij” labels (ubiquitine) en richting het proteasoom, het eiwit‑versnipperende systeem van de cel, werden gestuurd. Het blokkeren van het proteasoom keerde dit verlies om, en het kunstmatig verhogen van SLC7A11 of GPX4 in de cellen beschermde ze gedeeltelijk tegen rottlerin. Samen tonen deze bevindingen aan dat rottlerin optreedt als een dubbele degrader van twee centrale ferroptose‑afweermechanismen.
Bestaande leverkankergeneesmiddelen versterken
Veel patiënten met gevorderde leverkanker krijgen sorafenib, een standaard eerstelijnsmiddel dat op zichzelf ferroptose kan induceren, maar resistentie beperkt vaak het nut. De auteurs testten of lage, op zichzelf zwakke doses rottlerin tumoren gevoeliger konden maken voor ferroptose‑inducerende middelen zoals sorafenib en RSL3. In celkweek veroorzaakte de combinatie van lage doses rottlerin met één van deze middelen een duidelijke toename van kankerceldood en verschoof de dosis‑reactiecurven, wat op grotere werkzaamheid duidt. Belangrijk is dat dit sensibiliserende effect aanhield zelfs wanneer het klassieke rottlerin‑doeleiwit PKCδ genetisch werd verlaagd, wat laat zien dat de sleutelwerking niet via deze kinase maar via de afbraak van SLC7A11 en GPX4 verloopt. In muismodellen met menselijke levertumoren vertraagde de gecombineerde behandeling met rottlerin en sorafenib de tumorgroei meer dan sorafenib alleen en verlaagde bovendien de SLC7A11‑ en GPX4‑niveaus in de tumoren verder.
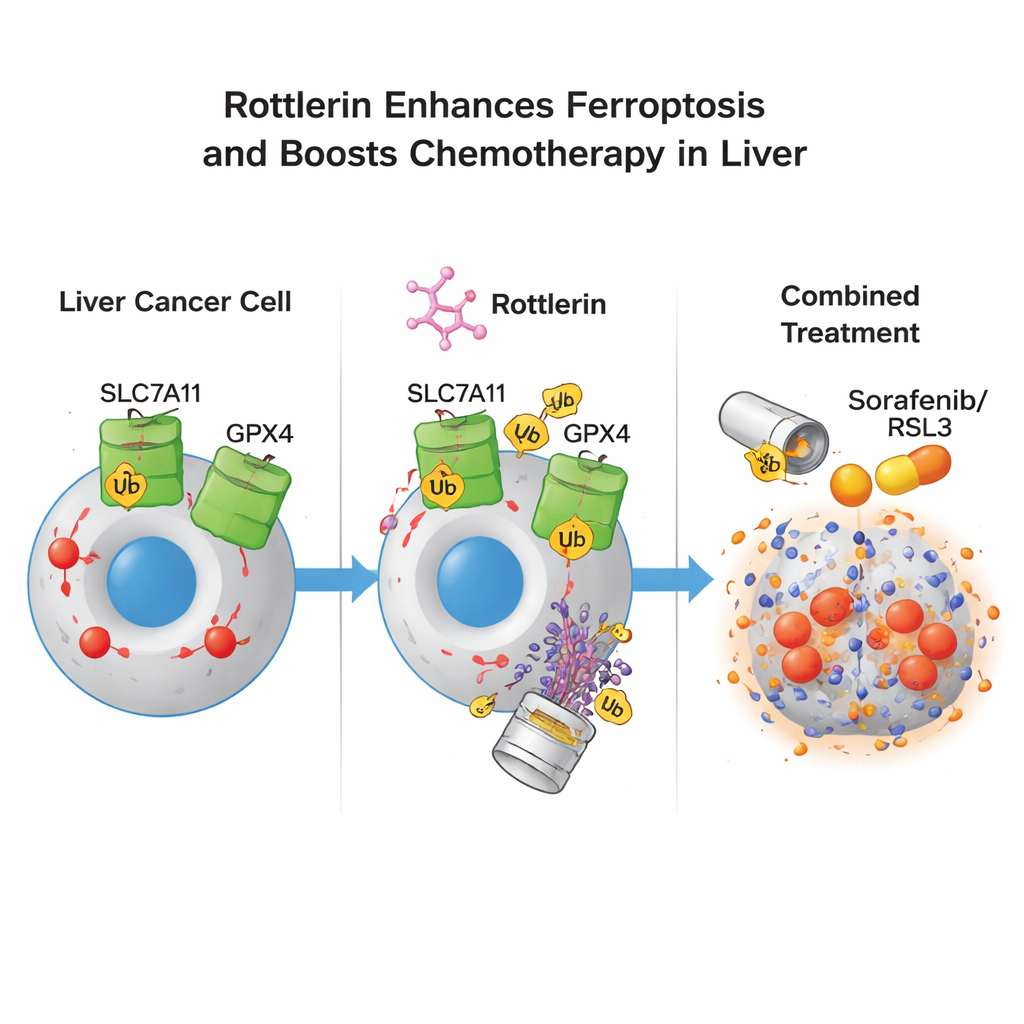
Wat dit kan betekenen voor toekomstige behandelingen
Voor niet‑specialisten is de kernboodschap dat rottlerin fungeert als een “twee‑slot ontgrendelaar” voor leverkankercellen: het verwijdert gelijktijdig twee cruciale sloten—SLC7A11 en GPX4—die cellen normaal beschermen tegen een dodelijke golf van vetgebaseerde oxidatie. Zodra die sloten weg zijn, worden kankercellen veel gevoeliger voor ferroptose, vooral in combinatie met bestaande middelen die hen in die richting duwen. Hoewel er meer onderzoek nodig is voordat rottlerin of aanverwante verbindingen bij patiënten kunnen worden toegepast, biedt deze strategie van dubbele afbraak een veelbelovende manier om de adaptieve afweermechanismen te omzeilen die levertumoren vaak zo moeilijk behandelbaar maken.
Bronvermelding: Luo, H., Jin, X., Gao, C. et al. Rottlerin triggers dual degradation of SLC7A11 and GPX4 to drive ferroptosis and chemosensitization in hepatocellular carcinoma. Cell Death Discov. 12, 89 (2026). https://doi.org/10.1038/s41420-026-02942-1
Trefwoorden: leverkanker, ferroptose, rottlerin, SLC7A11, GPX4