Clear Sky Science · nl
Verlies van DIAPH3 versnelt gliomagenese bij muizen
Waarom deze hersenstudie ertoe doet
Glioblastoom is een van de dodelijkste hersenkankers; ondanks operatie, bestraling en chemotherapie overleven de meeste patiënten niet veel langer dan een jaar. Deze studie stelt een fundamentele maar cruciale vraag: welke vroege veranderingen binnen hersencellen duwen ze richting zulke agressieve tumoren, en waarom zijn deze tumoren zo moeilijk met bestraling te vernietigen? Door een enkele structurele eiwit in muizenhersencellen te volgen, laten de onderzoekers zien hoe het verlies hiervan chromosomen destabiliseert, het verschijnen van tumoren versnelt en tumorachtige stamcellen helpt de bestraling te overleven die hen eigenlijk zou moeten doden.
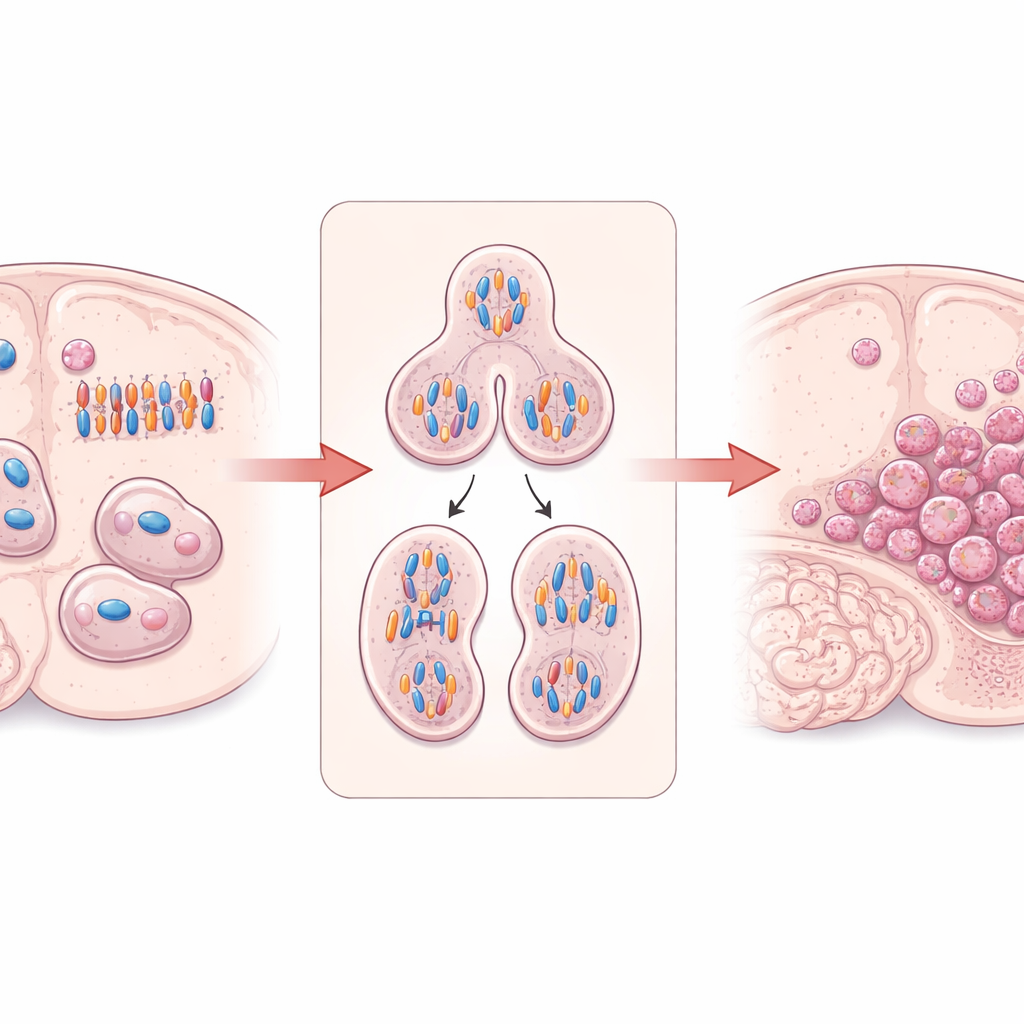
Een cel-‘bouwer’ die de deling in toom houdt
Het werk richt zich op DIAPH3, een eiwit dat helpt bij het opbouwen en organiseren van het interne skelet van de cel, bestaande uit actinefilamenten en microtubuli. In delende hersenstamcellen is DIAPH3 essentieel voor het vormen van een correcte spoelfiguur — de structuur die gedupliceerde chromosomen uit elkaar trekt — en voor het afknijpen van één cel in tweeën. Eerder onderzoek toonde aan dat wanneer DIAPH3 ontbreekt in zich ontwikkelende muizenhersenen, delende cellen vaak chromosomen verkeerd behandelen, wat leidt tot abnormale chromosoomaantallen (aneuploïdie), vastgelopen celdelingen en celdood. Intrigerend is dat een klein gebied op humaan chromosoom 13 dat het DIAPH3-gen bevat vaak gedeleted is in glioblastoom, en dat hogere DIAPH3-niveaus bij sommige patiënten geassocieerd zijn met betere overleving, wat suggereert dat dit eiwit als tumorsuppressor in de hersenen kan functioneren.
Muizenhersenen zo ontwerpen dat tumoren groeien
Om te testen of het verlies van DIAPH3 werkelijk hersenkanker bevordert, creëerde het team muizen waarin twee genen selectief verwijderd konden worden in in de cortex vormende stamcellen: Diaph3 en Trp53, laatstgenoemde codeert voor de bekende bewaker van het genoom, p53. Muizen die alleen in dit gebied Diaph3 misten, ontwikkelden zelfs na twee jaar geen tumoren, wat impliceert dat p53 nog steeds sterk afwijkende cellen kan elimineren. Daarentegen vormden muizen die alleen Trp53 misten, of zowel Trp53 als Diaph3, uiteindelijk hooggradige diffuse gliomen die onder de microscoop sterk leken op de menselijke ziekte. Met herhaalde ultra‑hoge‑veld MRI-scans toonden de onderzoekers aan dat dieren die beide genen misten eerder detecteerbare tumoren ontwikkelden, en dat ze tegen de middenleeftijd vaker grote gliomen droegen, vooral in de reukbollen, dan muizen die alleen Trp53 misten. De tumorgroeisnelheid, eenmaal begonnen, was vergelijkbaar tussen de groepen — wat veranderde was hoe snel tumoren verschenen.
Chromosomaal chaotisch en herschreven genactiviteit
Om te achterhalen waarom verlies van DIAPH3 het ontstaan van tumoren bespoedigt, onderzochten de onderzoekers genexpressie in de reukbollen van jonge muizen voordat er zichtbare tumoren waren. Bij dieren die zowel Diaph3 als Trp53 misten, werden 126 genen op andere niveaus tot expressie gebracht vergeleken met alleen Trp53-mutanten, en bijna de helft van deze genen had eerder een link met kanker. Veel veranderingen concentreerden zich in routes die celgroei, migratie en bloedvatvorming aansturen, waaronder VEGF, MAPK, RAS, Rap1 en cAMP-signaalroutes, evenals G‑eiwitgekoppelde receptor-netwerken. Dit gewijzigde moleculaire landschap suggereerde dat cellen eerder richting een kankergevoelig staat werden geduwd. Whole‑genome copy‑number analyse van volledig ontwikkelde tumoren liet zien dat DIAPH3‑deficiëntie niet sterk het aantal kleine, focale DNA-veranderingen verhoogde, maar eerder grote, gehele‑chromosoom winsten en verlies bevorderde — precies de aneuploïdie die verwacht wordt bij foutieve chromosoomsegregatie.
Ingebouwde DNA‑schade en hardere tumorstamcellen
Aneuploïde tumorcellen droegen meer interne DNA‑schade, gedetecteerd door verhoogde niveaus van de DNA‑breukmarker γ‑H2AX verspreid over celnuclei. Toch bleven deze tumoren groeien, wat impliceert dat ze mechanismen hadden verworven om zulke stress te tolereren. Bij vergelijking van genexpressie in gevestigde tumoren vonden de onderzoekers honderden genen die door DIAPH3‑verlies waren veranderd, waaronder opvallende amplificatie en overproductie van de groeifactorreceptor FGFR2 in veel dubbelmutante tumoren. FGFR2 is bekend als versterker van DNA‑herstelsystemen in glioblastoomcellen, en deactivering ervan is gelinkt aan gevoeligheid voor behandeling; activering daarvan daarentegen is verbonden met resistentie tegen bestraling. Het team isoleerde glioma‑stamachtige cellen uit muizentumoren en testte hun reactie op een klinisch relevante dosis ioniserende straling. Voor behandeling was de frequentie van stamachtige cellen vergelijkbaar in beide genotypen, maar na bestraling behielden kweekmateriaal afkomstig van DIAPH3‑deficiënte tumoren ongeveer twee keer zoveel actieve stamachtige cellen als die van alleen Trp53‑tumoren, wat grotere radioresistentie aantoont.
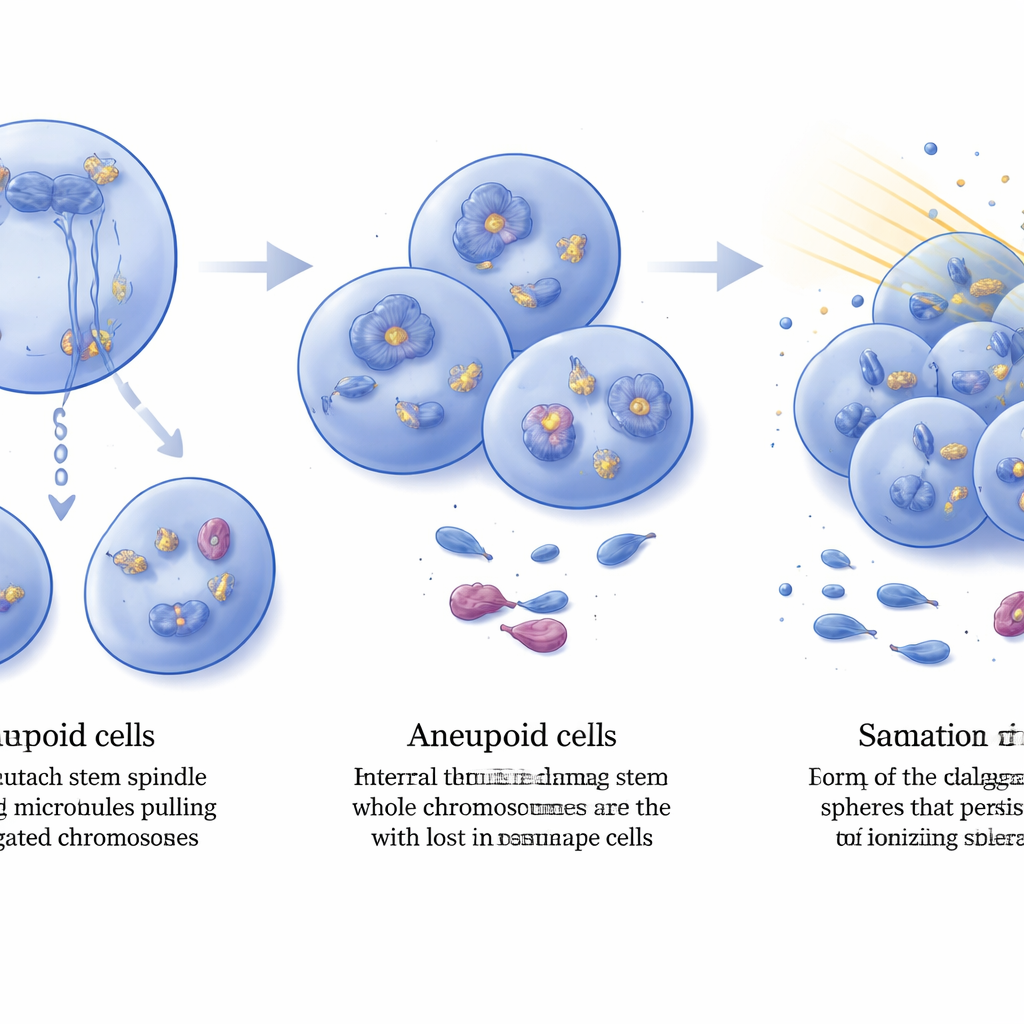
Wat dit betekent voor hersenkanker
Gezamenlijk schetst de studie DIAPH3 als een beschermer die hersenstamcellen helpt delen met het juiste aantal chromosomen. Wanneer zowel DIAPH3 als p53 ontbreken, wordt celdeling foutgevoelig, gaan hele chromosomen verloren of worden extra chromosomen verkregen, en bouwt DNA‑schade zich op. In plaats van te sterven, passen sommige cellen zich aan door herstelgerelateerde factoren zoals FGFR2 te amplifieren, en transformeren ze in aneuploïde, hooggradige gliomen waarvan de stamachtige cellen uitzonderlijk resistent zijn tegen bestraling. Hoewel muismodellen niet elk aspect van menselijk glioblastoom vatten, ondersteunen deze bevindingen DIAPH3 als zowel een potentiële prognostische biomarker als een knooppunt in het netwerk van processen die tumorinitiaties, genoomstabiliteit en behandelrespons reguleren — wat nieuwe wegen opent voor therapieën die deze verwoestende hersenkanker mogelijk kwetsbaarder kunnen maken voor bestaande behandelingen.
Bronvermelding: Chehade, G., Durá, I., Ruiz-Reig, N. et al. Loss of DIAPH3 accelerates glioma genesis in mice. Cell Death Dis 17, 342 (2026). https://doi.org/10.1038/s41419-026-08652-x
Trefwoorden: glioblastoom, chromosomale instabiliteit, hersentumorstamcellen, stralingsresistentie, tumorsuppressorgenen