Clear Sky Science · nl
Glioblastomacellen die chemoradiotherapie-geïnduceerde celdood ontlopen vertonen een gespleten glycolytisch programma
Waarom deze hersenkankerstudie ertoe doet
Glioblastoom is een van de dodelijkste hersentumoren bij volwassenen en groeit vrijwel altijd terug na operatie, chemotherapie en bestraling. Deze studie stelt een cruciale vraag: wat is er bijzonder aan die kleine groep tumorcellen die de behandeling overleven en later de ziekte nieuw leven inblazen? Door te volgen hoe deze cellen in de loop van de tijd suiker verwerken, onthullen de onderzoekers een verborgen overlevingsstrategie die kan verklaren waarom de huidige behandelingen zo vaak falen — en die nieuwe manieren aandraagt om de levenslijn van de tumor door te snijden.
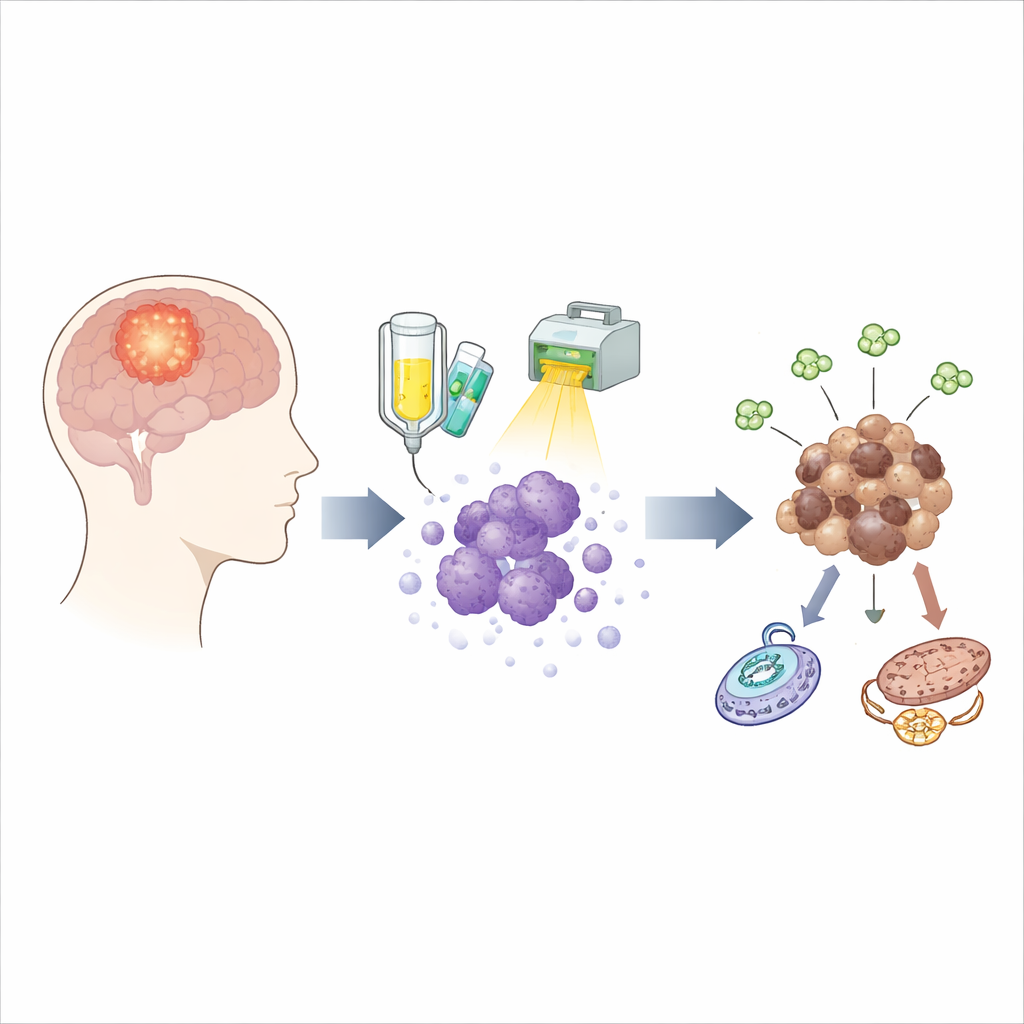
De verborgen overlevenden na behandeling
De standaardzorg voor glioblastoom combineert een middel genaamd temozolomide met bestraling. Hoewel deze combinatie het merendeel van de tumorcellen doodt, overleeft een hardnekkige minderheid en kan maanden later een nieuwe tumor zaaien. Om deze overlevenden in actie te betrappen, gebruikte het team tumorcellen direct afkomstig van tien verschillende patiënten en stelde ze bloot aan een behandelschema dat nauw aansluit bij wat mensen in de kliniek krijgen. Ze namen levendcelmonsters op verschillende momenten tijdens en na de behandeling en bestudeerden ook overeenkomende tumoren die in muizen werden gekweekt, waardoor ze konden volgen hoe de overlevenden in de tijd veranderen in plaats van alleen tumoren voor en na terugkeer te vergelijken.
Hoe tumorcellen veranderen hoe ze suiker gebruiken
Hersenweefsel verbruikt een opmerkelijk deel van de suiker in het lichaam, en glioblastoomcellen zijn er bijzonder gulzig op. De onderzoekers vonden dat de overlevende cellen naarmate de behandeling vorderde nog meer glucose uit hun omgeving opnamen. In een verrassende wending verbrandden ze deze extra brandstof echter niet simpelweg sneller. In plaats daarvan verlaagden deze cellen hun productie van lactaat, het gebruikelijke afvalproduct van snelle suikerafbraak in kanker. Metingen van sleutelproteïnen toonden een opvallend gespleten patroon: componenten die suiker de cel in brengen en het afbreken op gang brengen namen toe, terwijl diegenen die de latere stappen afhandelen en lactaat maken, afnamen. Dit "gespleten" programma betekent dat suiker binnenkomt en begint te worden verwerkt, maar dat de gebruikelijke uitgangsroute naar lactaat gedeeltelijk is afgesloten.
Brandstof omleiden naar bouwstoffen en energiecentrales
Waar gaat de omgeleide suiker naartoe? Met behulp van speciaal gelabelde glucose en geavanceerde metingen van metabolieten toonde het team aan dat de overlevende cellen veel van dit koolstof naar twee belangrijke bestemmingen sturen. De ene is een neventak die pentosefosfaatroute wordt genoemd, die de grondstoffen levert voor de aanmaak van DNA- en RNA-bouwstenen. In deze cellen waren veel nucleotidecomponenten en gerelateerde genen verhoogd, wat wijst op een sterke impuls richting herstel en voorbereiding op hervat groei. De tweede bestemming is de energiefabriek van de cel, de mitochondriën. Enzymen van de mitochondriale energieketen namen toe, en eerder werk van dezelfde groep liet zien dat er meer invoer van suikerafgeleide brandstof in deze structuren plaatsvindt. Samen onthult dit een gecoördineerde herbedrading: minder verspillende fermentatie naar lactaat, meer investering in reparatie, groeimateriaal en flexibele energieproductie.
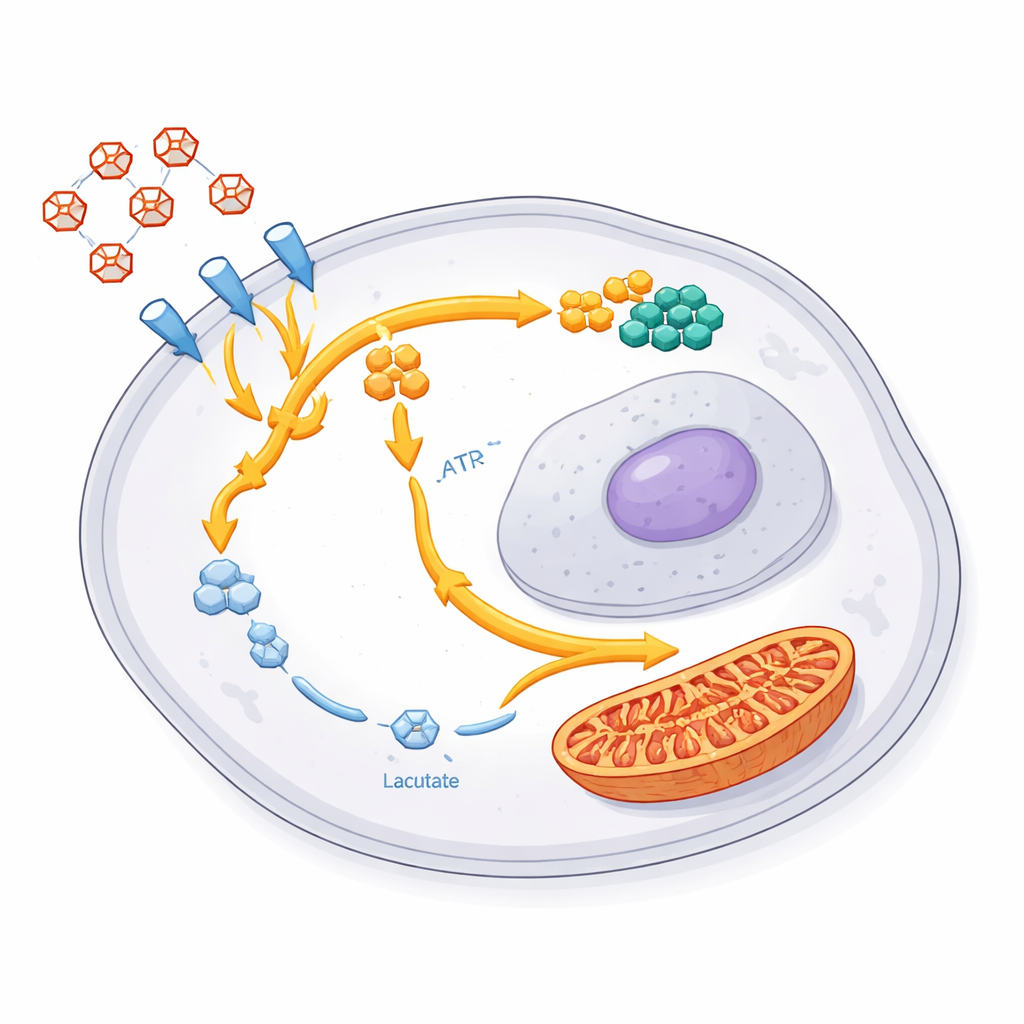
Een gedeeld overlevingsplan in tumoren en bij dieren
Glioblastoomtumoren verschillen sterk van patiënt tot patiënt, wat behandelingen volgens één standaard vaak dwarsboomt. Ondanks deze diversiteit vertoonde elk van de tien patiëntafgeleide modellen dezelfde basale verschuiving na chemoradiotherapie: verhoogde vroege suikerverwerkingsstappen, verlaagde latere stappen en lactaatproductie, en hogere mitochondriale activiteit. Belangrijk is dat hetzelfde kenmerk ook verscheen in muizenhersentumoren die uit patiëntcellen waren gegroeid en waren behandeld met aangepaste versies van de standaardtherapie. Recidiverende tumoren bij deze dieren behielden nog steeds het gewijzigde suikerprogramma, wat aangeeft dat dit geen voorbijgaand effect is maar een stabiele eigenschap van cellen die de behandeling weten te overleven en de kanker weer opbouwen.
Wat dit betekent voor toekomstige behandeling
Voor leken is de kernboodschap dat overlevende glioblastoomcellen zich niet simpelweg verbergen voor de behandeling; ze bedraden actief hoe ze suiker gebruiken om in leven te blijven. Ze nemen meer glucose op, vermijden het omzetten ervan in afval en leiden het in plaats daarvan naar de aanmaak van DNA-bouwstenen en het aandrijven van mitochondriën — wat hen helpt schade te herstellen, een flexibele, stamcelachtige staat te behouden en uiteindelijk de tumor te laten teruggroeien. Door deze gedeelde metabole overlevingsstaat aan het licht te brengen, wijst de studie op nieuwe therapeutische ideeën: het richten op de vroege suikerverwerkingsstappen, de DNA-aanmaak-neventak of de mitochondriale afhankelijkheid van deze cellen zou de standaard chemoradiotherapie vollediger kunnen maken, waardoor er minder ontsnappende cellen overblijven om de ziekte opnieuw te starten.
Bronvermelding: Martell, E., Kuzmychova, H., Chawla, U. et al. Glioblastoma cells that evade chemoradiotherapy-induced cell death exhibit a bifurcated glycolytic program. Cell Death Dis 17, 348 (2026). https://doi.org/10.1038/s41419-026-08646-9
Trefwoorden: glioblastoom, kankermetabolisme, glucosegebruik, therapieresistentie, pentosefosfaatroute