Clear Sky Science · nl
Metabole orkestratie gestuurd door GGCT: glutamine omleiden naar glutathionbiosynthese terwijl glucose-anaplerose wordt versterkt voor tumorproliferatie
Waarom dit belangrijk is voor kankerbehandeling
Kankercellen groeien snel en verbruiken daarbij enorme hoeveelheden brandstof; ze moeten zich voortdurend beschermen tegen toxische bijproducten van hun eigen stofwisseling. Deze studie onthult hoe een weinig bekend enzym, GGCT, helpt bij lever- en prostaattumoren om twee veelvoorkomende voedingsstoffen — glutamine en glucose — slim om te leiden, zodat ze zowel groei kunnen aandrijven als schadelijke moleculen, de zogenoemde reactieve zuurstofsoorten, onder controle houden. Inzicht in dit metabole jongleerwerk kan nieuwe manieren openen om tumoren uit te hongeren of hun verdedigingsmechanismen te overweldigen.
Hoe tumorcellen brandstof en bescherming jongleren
Tumorcellen zijn sterk afhankelijk van glutamine, een aminozuur met een dubbele rol: het kan worden afgebroken om de belangrijkste energieproducerende cyclus van de cel te voeden, en het levert ook bouwstenen voor glutathion, een krachtig antioxidant dat reactieve zuurstofsoorten neutraliseert. De auteurs bevestigden eerst dat glutamine-niveaus hoger zijn in levertumoren dan in nabijgelegen gezond weefsel, en dat kankercellen die met meer glutamine worden gekweekt sneller delen, zowel in kweekschalen als in muizen. Wanneer glutamine schaars is, vertragen cellen, nemen sleutelproteïnen van de celcyclus af, en krimpen tumoren in dieren — deels omdat de antioxidante verdedigingsmechanismen verzwakken en reactieve zuurstofsoorten zich ophopen.
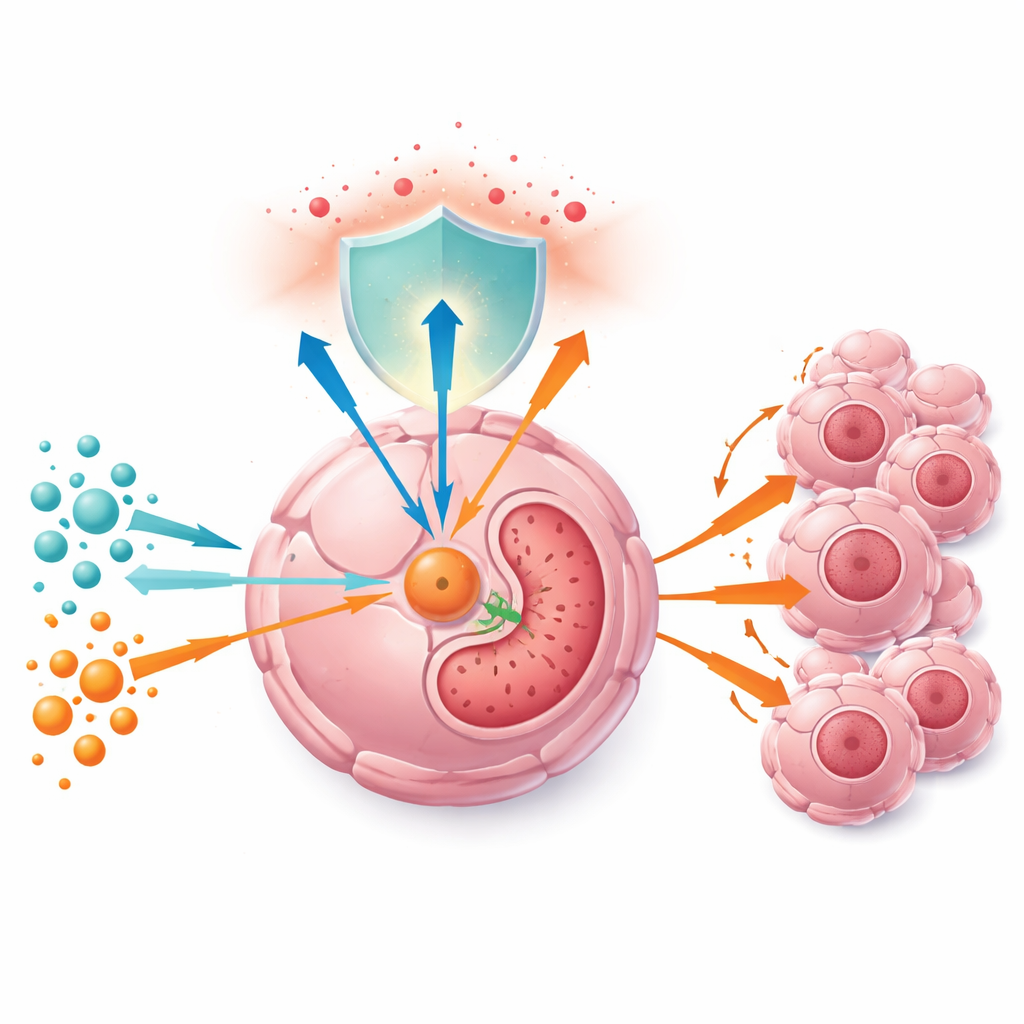
Een metabole schakelaar in het volle zicht
Door patiëntmonsters en grote kanker-databases te analyseren, vond het team dat het enzym GGCT consequent meer voorkomt in lever- en prostaattumoren dan in normaal weefsel, en dat hogere GGCT-niveaus slechtere uitkomsten voorspellen. In zowel tumormonsters als gecultiveerde cellen stijgen GGCT-niveaus in lijn met de glutamineconcentratie, wat suggereert dat tumoren de beschikbaarheid van glutamine via dit eiwit ‘lezen’. De onderzoekers werkten een regelketen uit: glutamine houdt de pro-groeifactor c-Myc actief, die een klein regulatorisch RNA, miR-29b-3p, onderdrukt; wanneer miR-29b-3p laag is, wordt GGCT uit zijn remming vrijgelaten en hoopt het enzym zich op. Bij glutaminegebrek keert deze keten om: miR-29b-3p stijgt, GGCT-boodschappen worden sneller afgebroken en het enzymniveau daalt.
Glutamine omleiden en meer glucose aantrekken
Om te achterhalen wat GGCT binnencellulair daadwerkelijk doet, verlaagden of verhoogden de auteurs de GGCT-niveaus en maten ze zowel celgedrag als honderden metabolieten. Het stilleggen van GGCT blokkeerde cellen in de delingscyclus, verkleinde hun kolonies en verlaagde glutathion sterk terwijl reactieve zuurstofsoorten toenamen; het toevoegen van een chemisch antioxidant herstelde de groei gedeeltelijk. Onder de microscoop werden mitochondriën abnormaal verlengd en minder efficiënt in zuurstofverbruik, terwijl cellen probeerden te compenseren door glycolyse, de eerste stap van suikerafbraak, op te voeren. Gedetailleerde metabole profilering toonde dat tussenproducten van de centrale energiedriehoek daalden wanneer GGCT verloren ging en stegen wanneer het werd overgeproduceerd.
Het spoor van koolstofatomen volgen
Het team volgde vervolgens gelabelde glutamine- en glucoseatomen terwijl ze door het tumormetabolisme stroomden. Bij overexpressie van GGCT kwam minder gelabelde glutamine in de energiedriehoek terecht en meer werd omgeleid naar nieuw gesynthetiseerd glutathion, ter ondersteuning van de antioxidantverdediging. Tegelijkertijd droeg gelabelde glucose sterker bij aan de cyclus en compenseerde zo voor de omgeleide glutamine. Een mutante vorm van GGCT zonder normale enzymatische activiteit kon deze verschuivingen niet aandrijven of proliferatie bevorderen, wat aantoont dat de katalytische functie van GGCT cruciaal is. Belangrijk is dat het toedienen van extra pyruvaat of het aanpassen van de toegang tot de energiedriehoek de cellulaire energieniveaus herstelde maar de reactieve zuurstofsoorten niet verlaagde, wat aangeeft dat GGCT voornamelijk de redoxbalans regelt via glutathion en niet door eenvoudige veranderingen in de energievoorziening.
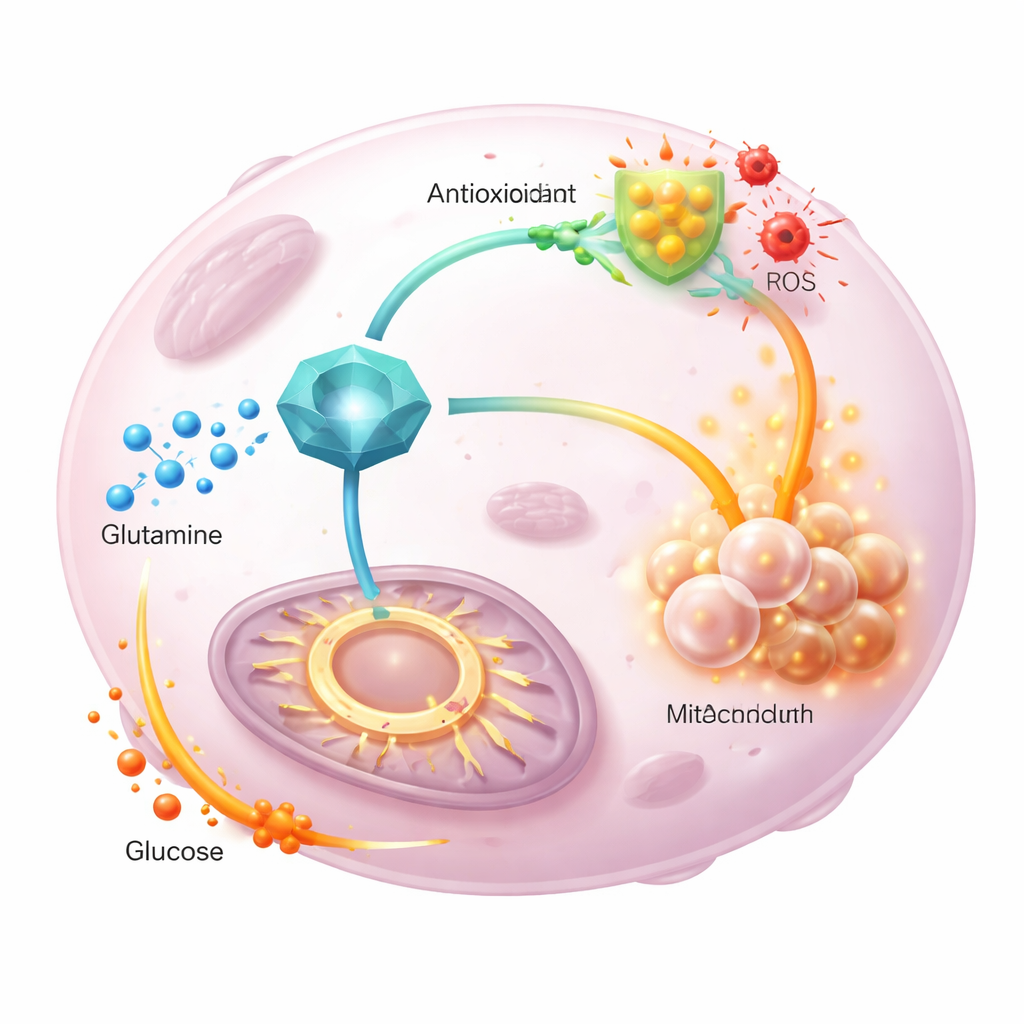
Wat dit betekent voor toekomstige therapieën
Samen genomen positioneren de bevindingen GGCT als een centrale coördinator die tumoren in staat stelt de taken van glutamine te splitsen: het stuurt meer van deze voedingsstof naar de productie van antioxidanten terwijl het glucose naar de energiedriehoek trekt om celdeling op gang te houden. In diermodellen remde het onderdrukken van GGCT tumorgroei, verlaagde het glutathion en verhoogde het oxidatieve stress, en deze effecten konden deels worden teruggedraaid met een antioxidantmiddel. Voor de niet-specialist is de kernboodschap dat sommige kankers overleven door GGCT te gebruiken als een metabole schakelcentrale; geneesmiddelen die deze schakel uitschakelen, zouden zowel de verdediging van de tumor tegen oxidatieve schade kunnen verzwakken als diens flexibele benutting van voedingsstoffen kunnen verstoren, waardoor standaardbehandelingen effectiever worden.
Bronvermelding: Yang, L., Sun, H., Wang, R. et al. Metabolic orchestration driven by GGCT: diverting glutamine to glutathione biosynthesis while enhancing glucose anaplerosis for tumor proliferation. Cell Death Dis 17, 358 (2026). https://doi.org/10.1038/s41419-026-08619-y
Trefwoorden: kankermetabolisme, glutamine, glutathion, oxidatieve stress, GGCT-enzym