Clear Sky Science · nl
Adipogene transdifferentiatie zet EMT-rijke PDAC-cellen om in een post-mitotische vetcelachtige toestand en beperkt metastase
Gevaarlijke kankercellen veranderen in onschuldige vet
Pancreaskanker behoort tot de dodelijkste vormen van kanker, grotendeels omdat het vroeg uitzaait en zich verzet tegen standaardbehandelingen. Deze studie onderzoekt een opvallend andere invalshoek: in plaats van te proberen tumorcellen te vergiftigen of uit te hongeren, wat als we de meest gevaarlijke pancreaskankercellen zouden kunnen aansporen zich te transformeren tot vetachtige cellen die niet meer delen of door het lichaam reizen? Het werk beschrijft hoe onderzoekers hoog-agressieve pancreaskankercellen richting een stabiele, vetcelachtige staat duwden, wat de tumorgroei vertraagde en de uitzaaiing bij muizen verminderde, en zo een nieuwe manier aanwijst om deze verwoestende ziekte te beheersen.
Waarom pancreaskanker zo moeilijk te stoppen is
Pancreasductaal adenocarcinoom, de belangrijkste vorm van pancreaskanker, heeft een zeer slechte prognose: slechts ongeveer één op de acht patiënten leeft vijf jaar na de diagnose. Een deel van het probleem is dat veel tumorcellen in deze kanker in een gedaanteverwisselende toestand leven die EMT wordt genoemd, wat ze mobieler, invasiever en resistenter tegen geneesmiddelen maakt. Pogingen om de vele signalen die deze toestand aansturen te blokkeren hebben weinig opgeleverd. Tegelijkertijd vertoont de pancreas en zijn tumoren een verrassende neiging om vetcellen te accumuleren, wat de vraag oproept of deze verborgen flexibiliteit in celidentiteit benut kan worden. De auteurs redeneerden dat als EMT-rijke pancreaskankercellen al ontvankelijk zijn voor verandering, ze wellicht omgeleid kunnen worden naar een rustige, vetachtige identiteit in plaats van een invasieve.
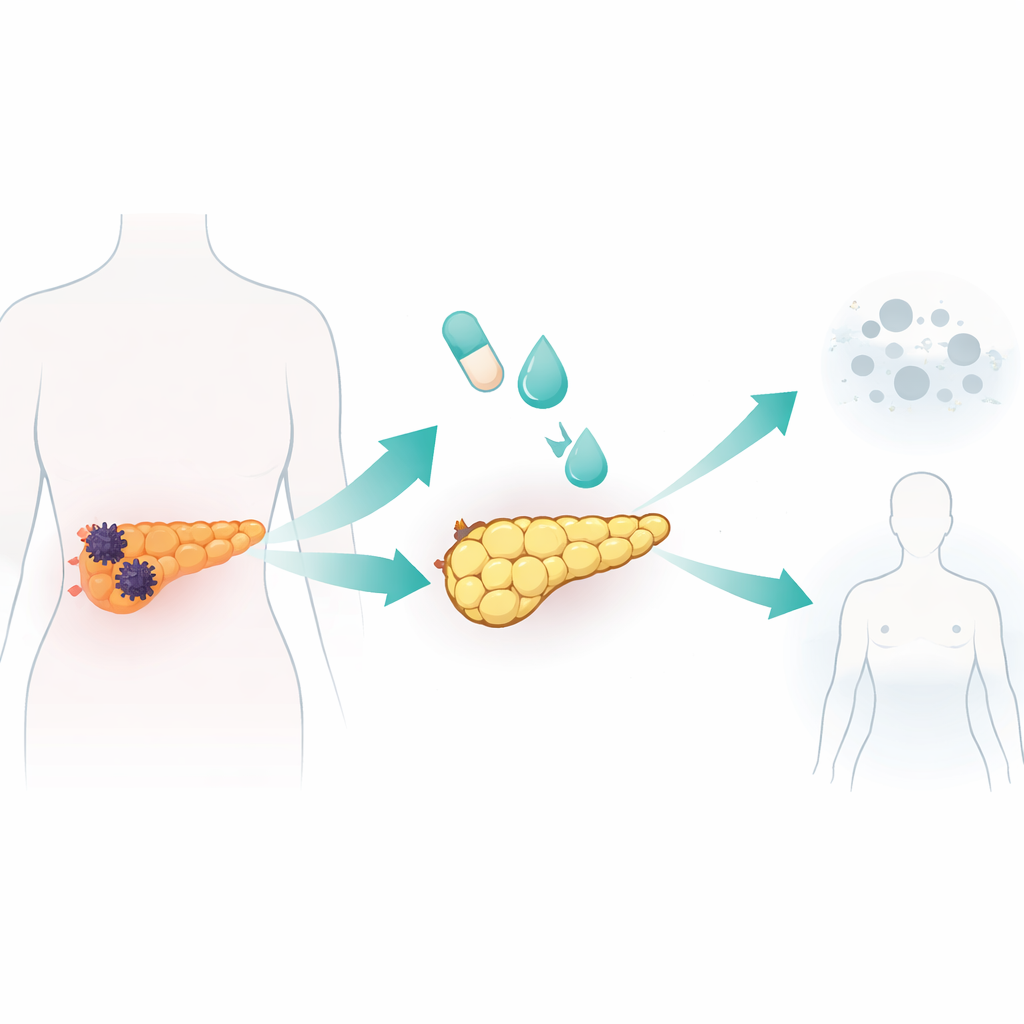
Kankercellen in het lab herprogrammeren tot vetachtige cellen
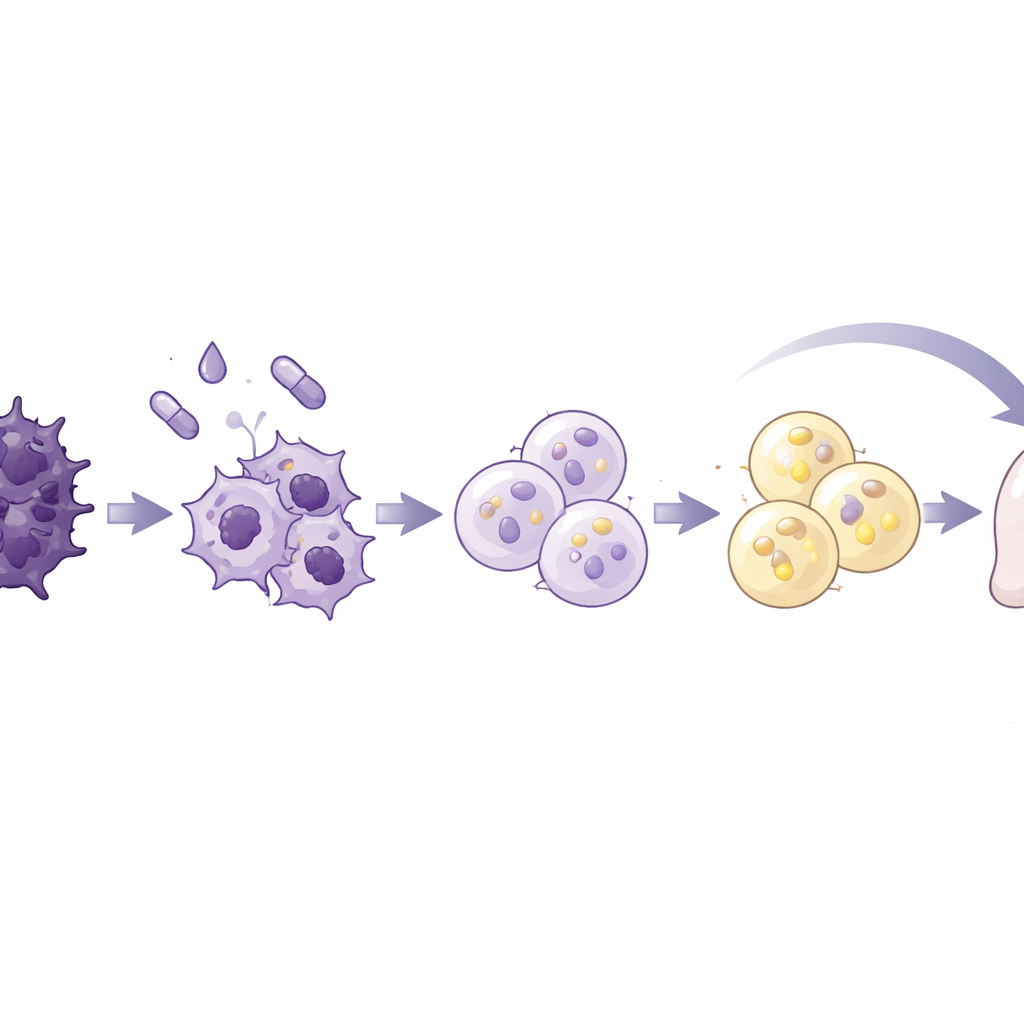
Het team testte een standaard cocktail voor vetcelvorming, gebruikt in eerder vetbiologie- en borstkankeronderzoek, op zeven menselijke pancreaskankercelijnen en één normale pancreascellijn. Het mengsel combineerde insuline en een steroid met rosiglitazon, een medicijn dat een hoofdregelaar van vetvorming activeert, plus een signaalmolecuul genaamd BMP2 om celplasticiteit vrij te maken. Eén kankerlijn, AsPC-1 genaamd, reageerde bijzonder sterk. In tien dagen werden deze cellen groter en ronder en vulden ze zich met lipidedruppels, kenmerken van vetcellen. Ze schakelden genen en eiwitten aan die typisch zijn voor rijpe vetcellen en vertoonden robuuste vetstofwisseling, inclusief afgifte van adiponectine en het afbreken van opgeslagen vet op stimulus. Cruciaal was dat deze omgezette cellen stopten met prolifereren, vastliepen in een vroege fase van de celcyclus en veel minder bewogen en invadeerden dan onbehandelde kankercellen.
Het kankersignaal diep in de cel uitschakelen
Om te zien wat er op moleculair niveau gebeurde, analyseerden de onderzoekers de DNA-verpakking en genactiviteit van de omgezette cellen. Ze vonden een brede verstrakking van chromatine, het DNA–eiwitcomplex dat de toegang tot genen regelt, samen met een wereldwijde daling van genexpressie, beide kenmerken van niet-delende cellen. Genen die EMT, invasie en metastase ondersteunen, inclusief matrixafbrekende enzymen en belangrijke EMT-regulatoren, werden sterk onderdrukt, terwijl vetgerelateerde genen werden versterkt. Het algemene genexpressieprofiel verschoof van een mesenchymale, sterk mobiele identiteit naar een die sterk leek op rijpe vetcellen. Signalen gekoppeld aan celgroei en de respons op een belangrijke EMT-aanjager, TGF-beta, werden afgezwakt, terwijl paden gerelateerd aan lipidehuishouding en celadhesie werden versterkt. Deze veranderingen suggereren dat de cellen niet louter vertraagden, maar fundamenteel hergespecificeerd werden.
De strategie testen in muizen
De wetenschappers vroegen zich vervolgens af of deze geforceerde vetachtige conversie zou helpen tumoren in levende dieren te beheersen. Ze implanteen menselijke pancreaskankercellen in de pancreas of milt van muizen om primaire tumoren en levermetastasen te modelleren. Muizen behandeld met rosiglitazon en BMP2 ontwikkelden kleinere pancreastumoren en toonden rijkere lipidedruppels en vetcelmarkers binnen de tumoren, samen met lagere niveaus van EMT- en invasiegenen. In het metastasemodel veranderde de behandeling de vroege tumorzaai niet, maar in de loop van de tijd vertraagde ze de uitbreiding van de tumorbelasting in de lever vergeleken met onbehandelde dieren. Belangrijk is dat aangrenzend normaal pancreastweefsel geen opvallende vetcelconversie vertoonde, en de vetachtige toestand in tumoren hield ten minste een maand aan nadat de medicijnen stopten, wat duidt op een zekere duurzaamheid en specificiteit.
Wat dit kan betekenen voor toekomstige kankerzorg
Deze studie ondersteunt een provocerend concept: voor sterk plastische, EMT-rijke pancreastumoren kan het mogelijk zijn om te "converteren in plaats van doden", gevaarlijke, rondzwervende tumorcellen om te leiden naar stabiele, niet-delende vetachtige cellen die minder in staat zijn uit te zaaien. Hoewel dit vroegfasewerk is in cellen en muismodellen, en niet alle pancreaskankers even responsief zullen zijn, opent het een nieuw therapeutisch pad dat werkt door celidentiteit te veranderen in plaats van alleen groeisignalen te blokkeren. In de toekomst zouden dergelijke transdifferentiatie-benaderingen gecombineerd kunnen worden met gerichte middelen of immunotherapieën om pancreaskanker in een rustiger, beter beheersbare staat te houden en het risico op dodelijke metastase te verkleinen.
Bronvermelding: Qian, Y., Yan, Z., Wang, J. et al. Adipogenic transdifferentiation reprograms EMT-high PDAC cells into a post-mitotic adipocyte-like state and limits metastasis. Cell Death Dis 17, 330 (2026). https://doi.org/10.1038/s41419-026-08613-4
Trefwoorden: pancreaskanker, celplasticiteit, transdifferentiatie, epitheliale-mesenchymale overgang, vetcelachtige cellen