Clear Sky Science · nl
CBX2-vastestofscheiding draagt bij aan homologe recombinatiereparatie en medicijnresistentie bij eierstokkanker
Waarom dit onderzoek ertoe doet
Eierstokkanker behoort tot de dodelijkste vormen van kanker bij vrouwen, grotendeels omdat veel tumoren stoppen met reageren op chemotherapie. Deze studie onthult een verborgen overlevingstruc die door hooggradig sereus eierstokkanker wordt gebruikt: ze vormen kleine, vloeistofachtige druppels in de celkern die DNA-reparatie stimuleren en tumorcellen helpen schade door standaardmedicatie te weerstaan. Het werk wijst ook op een bestaand middel, Ibrutinib, als een mogelijke manier om deze zwakte uit te buiten bij patiënten van wie de tumoren afhankelijk zijn van dit druppelgebaseerde reparatiesysteem.
Tumorcellen die hun DNA te goed repareren
De meest krachtige kankertherapieën werken door DNA zo ernstig te beschadigen dat tumorcellen zich niet langer kunnen delen. Bij hooggradig sereus eierstokkanker worden veel tumoren echter bedreven in het herstellen van deze schade, wat leidt tot resistentie tegen platina-gebaseerde chemotherapie en PARP-remmers. De auteurs richtten zich op een eiwit genaamd CBX2, dat chemische markeringen op DNA-verpakking afleest en in hogere niveaus wordt aangetroffen in eierstoktumoren dan in normaal weefsel. In patiëntendatasets en weefselmonsters waren tumoren met meer CBX2 vaker resistent tegen behandeling met platina en keerden ze eerder terug, vooral in deze agressieve subtype van eierstokkanker.
Druppels in de kern: een reparatie-"werkbank"
CBX2 heeft de ongewone eigenschap om dichte, druppelachtige clusters te vormen in de celkern, een proces dat bekendstaat als vastestofscheiding. Deze druppels gedragen zich als kleine vloeibare werkbanken die specifieke eiwitten kunnen concentreren. Door kankercellen met normale CBX2, zonder CBX2 of een gemuteerde vorm die geen druppels kan vormen te vergelijken, toonden de onderzoekers aan dat CBX2-druppels centraal staan in hoe tumorcellen gebroken DNA herstellen. Wanneer CBX2 werd verwijderd, braken chromosomen vaker, stapelden signalen van DNA-schade zich op en raakten beide hoofdroutes voor het repareren van dubbele strengbreuken verzwakt. Het herstellen van normaal CBX2 bracht deze reparatiecapaciteiten terug, maar een druppel-defecte versie deed dat niet, ook al kon deze nog steeds aan DNA binden. 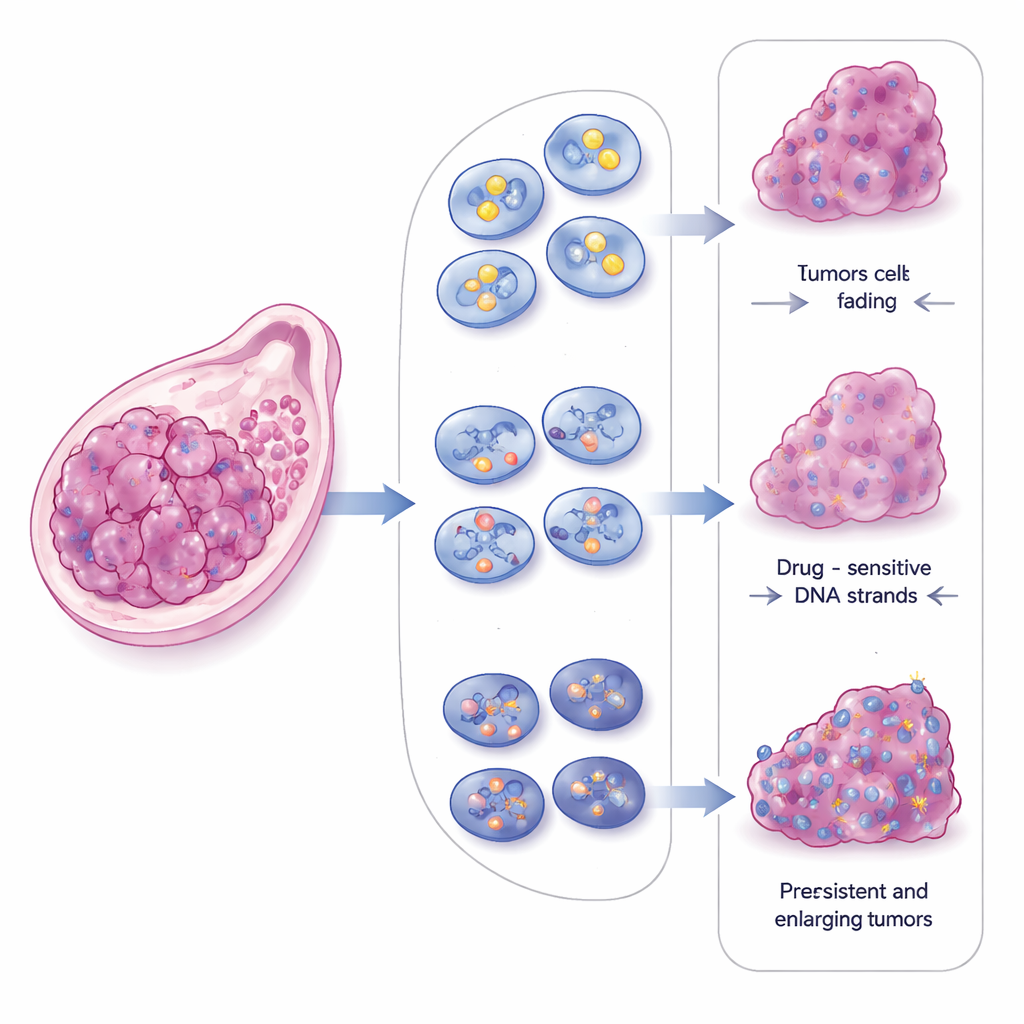
Hoe CBX2-druppels de reparatieploeg organiseren
Dieper gravend onderzochten de onderzoekers welke reparatie-eiwitten daadwerkelijk aan DNA worden gerekruteerd in de aanwezigheid of afwezigheid van CBX2-druppels. Ze vonden dat CBX2-druppels helpen sleutelspelers van de schade-respons aan te trekken, waaronder PARP1, 53BP1, BRCA1 en RAD51—eiwitten die bepalen hoe een breuk wordt hersteld en vervolgens de reparatie uitvoeren. Live-celbeeldvorming toonde twee varianten van CBX2-druppels: een mobiele, vloeibare vorm die dynamisch mengt met beschadigd chromatine, en een dichte, meer vaste vorm die dat niet doet. Alleen de mobiele druppels overlappen met DNA-schadefoci en de belangrijkste reparatie-eiwitten, wat suggereert dat deze vloeibare fase fungeert als het functionele geraamte dat de reperaturmachinerie juist daar verzamelt en organiseert waar het nodig is.
Een kracht omzetten in een zwakte met een bestaand medicijn
Aangezien CBX2-druppels tumorcellen bijzonder goed maken in het repareren van DNA, vroegen de auteurs zich af of deze verhoogde reparatiecapaciteit tegen de cellen kon worden gebruikt. Ze screeneden een bibliotheek met verbindingen op cellen met of zonder functionele CBX2-druppels en ontdekten dat Ibrutinib—een orale medicatie die al is goedgekeurd voor bepaalde bloedkankers—specifiek toxisch was voor cellen die afhankelijk waren van CBX2-condensaten. Ibrutinib verhinderde niet dat de druppels zich vormden, maar verzwakte selectief de hoog-fidele reparatieroute waarop deze cellen vertrouwen. In diermodellen krompen tumoren met CBX2-druppels onder Ibrutinib-behandeling, en driedimensionale organoïden gekweekt uit tumoren van patiënten met hoge CBX2-niveaus waren gevoeliger voor het middel dan organoïden met lage niveaus. 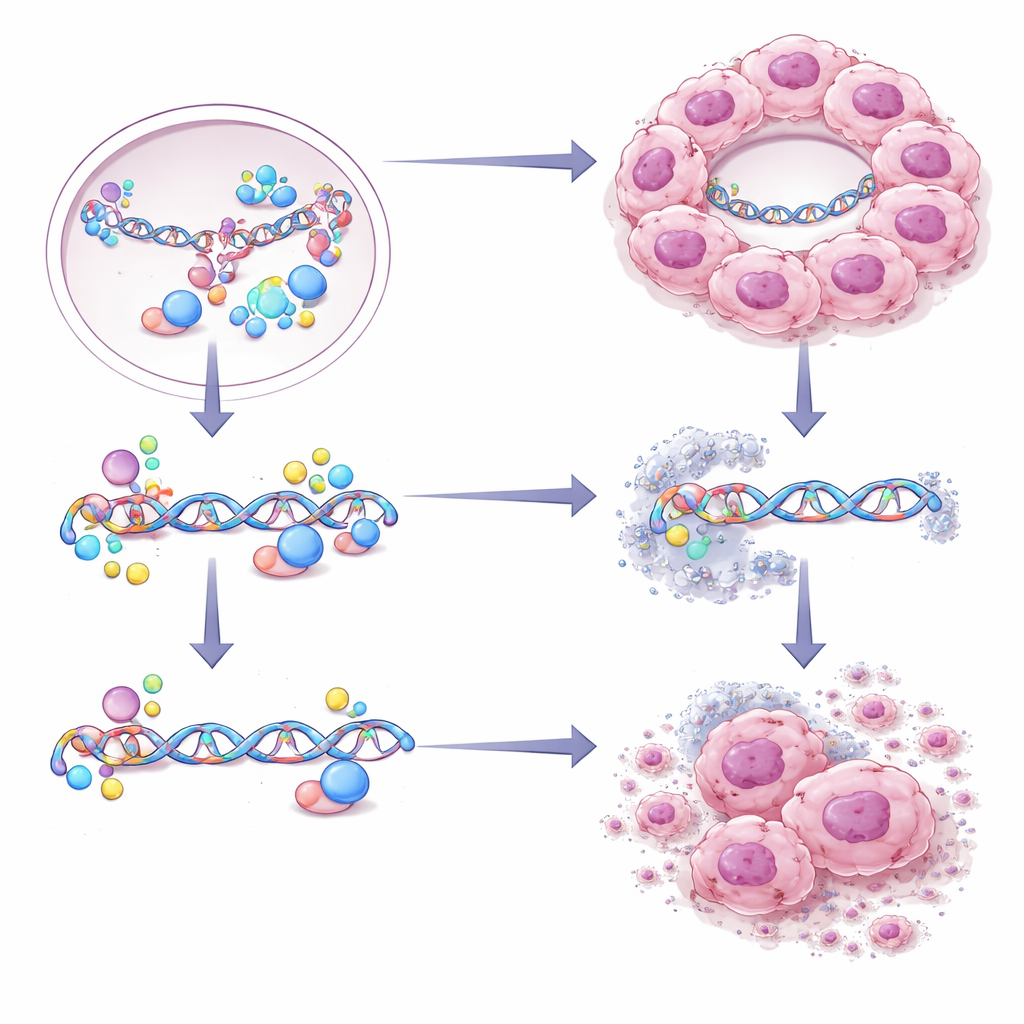
Wat dit voor patiënten zou kunnen betekenen
Voor patiënten suggereert de studie twee belangrijke ideeën. Ten eerste kan de aanwezigheid en het patroon van CBX2-druppels in tumorweefsel helpen voorspellen hoe goed iemand zal reageren op platina-chemo en PARP-remmers: patiënten zonder CBX2 doen het het best, degenen met diffuse CBX2 zitten ertussen en degenen met duidelijke CBX2-condensaten hebben de slechtste uitkomsten. Ten tweede kan datzelfde druppelpatroon patiënten aanwijzen die mogelijk baat hebben bij Ibrutinib, waarmee een bloedkankergeneesmiddel wordt herbestemd voor een moeilijk te behandelen subtype van eierstokkanker. In wezen toont het werk aan dat de structuren die het tumordna beschermen ook een nieuwe Achillespees kunnen blootleggen—wat een potentiële route biedt naar meer gepersonaliseerde en effectieve behandeling.
Bronvermelding: Sun, S., Huang, L., Ma, Y. et al. CBX2 phase-separation contributes to homologous recombination repair and drug resistance in ovarian cancer. Cell Death Dis 17, 366 (2026). https://doi.org/10.1038/s41419-026-08605-4
Trefwoorden: eierstokkanker, medicijnresistentie, DNA-reparatie, vastestofscheiding, Ibrutinib