Clear Sky Science · nl
HNRNPH1 bestuurt de progressie van glioblastoom door het spleisen van celdelingsgenen te reguleren
Waarom deze studie over hersenkanker ertoe doet
Glioblastoom is een van de dodelijkste vormen van hersenkanker, deels omdat de kankercellen zich snel delen maar toch weten te voorkomen dat ze zichzelf vernietigen. Deze studie onthult hoe een weinig bekend molecuul in tumorcellen hen helpt om op een ordelijke manier te blijven delen, in plaats van uiteen te vallen. Door dit verborgen ondersteuningssysteem bloot te leggen, wijst het werk op nieuwe manieren waarop artsen mogelijk glioblastoomcellen uiteindelijk over de rand kunnen duwen en de groei van tumoren kunnen stoppen.
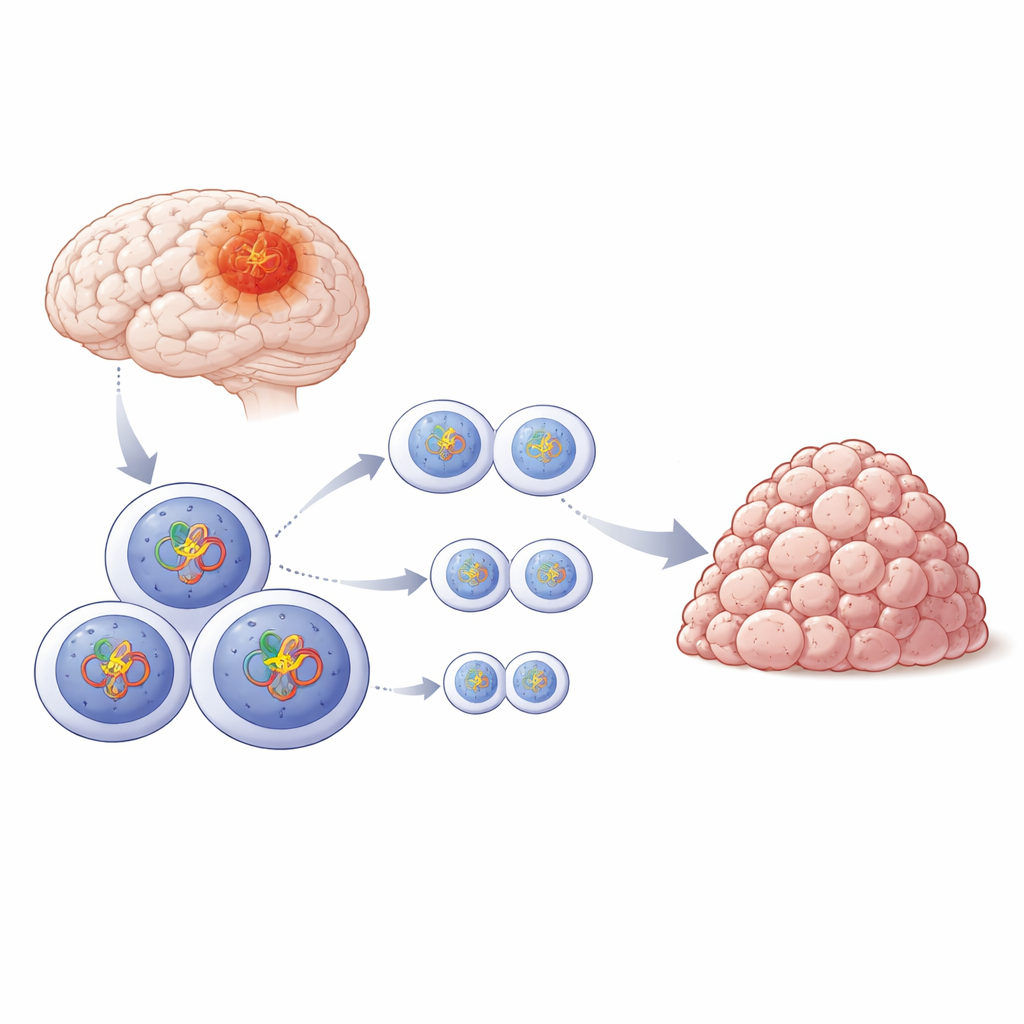
De verborgen helper in tumorcellen
De onderzoekers richtten zich op glioblastoom, een agressieve hersentumor die vaak weerstand biedt tegen chirurgie, bestraling en chemotherapie. Kankercellen dragen meestal veel DNA‑mutaties die hen aanzetten tot delen, maar ze zijn nog steeds afhankelijk van intacte mechanismen om hun chromosomen tijdens elke celdeling te kopiëren en te scheiden. Als dit systeem faalt, kunnen cellen sterven in een proces dat “mitotische catastrofe” wordt genoemd. Het team stelde zich de vraag welke moleculaire spelers glioblastoomcellen helpen om dit fragiele delingsproces te behouden, ondanks hun beschadigde genoom.
Een verkeersregelaar voor genetische boodschappen
Ze concentreerden zich op een eiwit genaamd HNRNPH1, behorend tot een familie van moleculen die RNA binden—de kortlevende boodschappen die van DNA worden gekopieerd. Deze eiwitten helpen bepalen hoe ruwe RNA‑transcripten worden geknipt en aan elkaar geplakt voordat ze in eiwitten worden omgezet, een proces dat spleisen wordt genoemd. Door grote patiëntendatasets en tumorstalen te analyseren, ontdekten de wetenschappers dat HNRNPH1 veel hoger wordt geproduceerd in glioblastoomweefsel dan in normaal hersenweefsel. Enkel‑cel‑ en ruimtelijke kaarten toonden aan dat het vooral overvloedig is in tumorcellen die lijken op onrijpe, snel delende hersencellen en in goed geoxygeneerde, sterk prolifererende gebieden van de tumor, maar veel lager in zuurstofarme, gestresste zones.
Hoe HNRNPH1 de celdeling op koers houdt
Om te zien wat er gebeurt als HNRNPH1 verdwijnt, gebruikte het team genetische bewerking en RNA‑stilleggende middelen om dit eiwit in gekweekte glioblastoomcellen te verminderen. Dit veroorzaakte ingrijpende veranderingen in de activiteit van duizenden genen, met bijzonder sterke effecten op degenen die het G2/M‑controlepunt regelen—de laatste kwaliteitscontrole voordat een cel deelt. HNRNPH1 bleek rechtstreeks te binden aan de RNA‑blauwdrukken van meerdere sleutelregulatoren van de deling, waaronder eiwitten die helpen om chromosomen correct te scheiden. Wanneer HNRNPH1 verdween, werden deze RNA’s onjuist gespleisd of in lagere hoeveelheden geproduceerd, wat leidde tot minder van de eiwitten die nodig zijn voor ordelijke mitose.
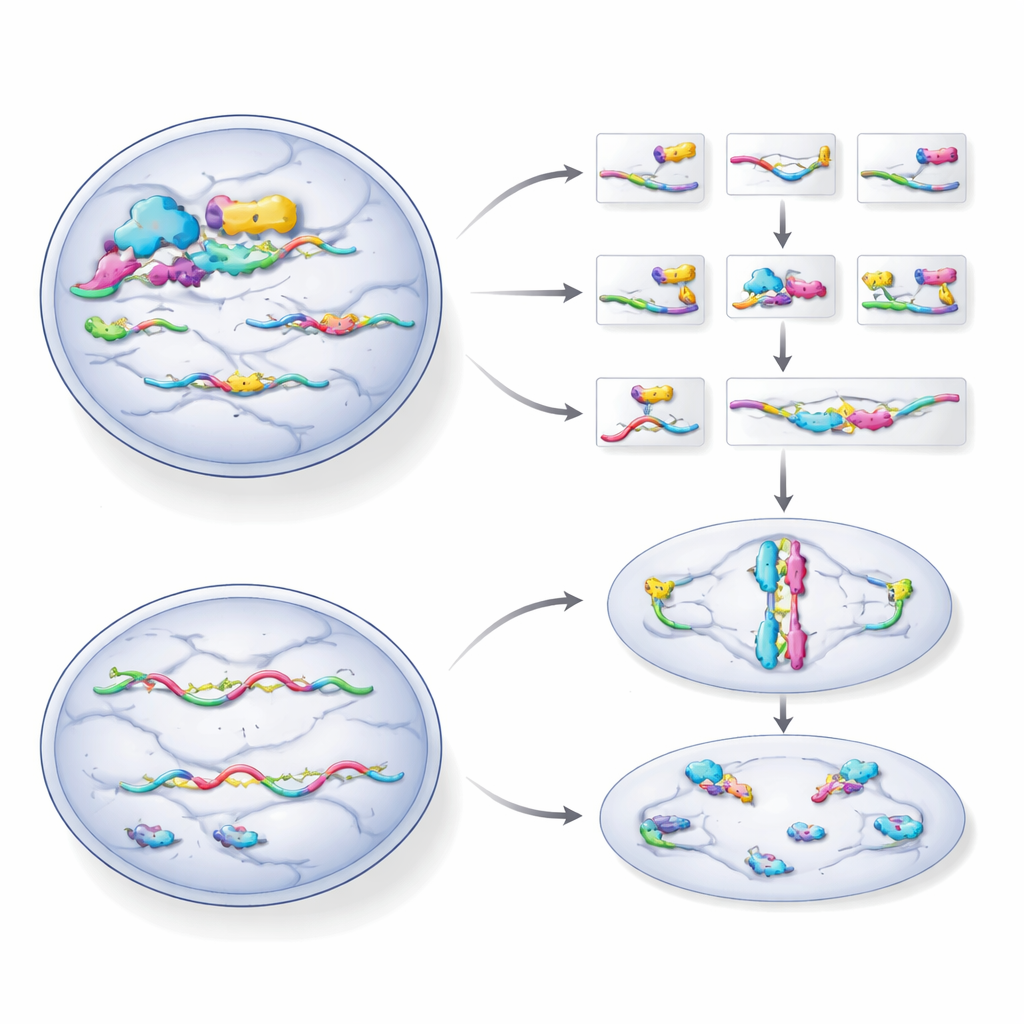
Als de helper wegvalt, hapert de celdeling
Cellen zonder HNRNPH1 groeiden langzamer, stapelden zich op in de late stadia van de celdeling en ontwikkelden vergrote, verkeerd gevormde of gefragmenteerde kernen—klassieke tekenen dat de deling misgaat. Onder de microscoop waren er minder cellen die normale mitose uitvoerden, en hun interne steigers voor het uit elkaar trekken van chromosomen waren verstoord. Het team ontdekte ook dat HNRNPH1 het spleisen van een andere regelaar, UHRF2, stuurt, waarbij zijn RNA schakelt tussen een productieve vorm en een defecte vorm. Zonder HNRNPH1 werden meer UHRF2‑boodschappen foutief bewerkt, wat de hoeveelheid functioneel eiwit verlaagde en de controle over de celdeling verder verstoorde.
Bewijs uit tumoren in levende hersenen
De wetenschappers testten vervolgens het belang van HNRNPH1 in muismodellen. Ze implanteerden menselijke glioblastoomcellen, ofwel normaal of zodanig gemodificeerd dat HNRNPH1 was verlaagd, in de hersenen van muizen. Dieren die controlecellen ontvingen ontwikkelden snel grote tumoren en stierven eerder. Muizen die cellen met gereduceerde HNRNPH1 kregen, ontwikkelden veel kleinere of vertraagde tumoren en leefden langer. De tumoren die uiteindelijk toch groeiden hadden echter HNRNPH1‑activiteit herwonnen, wat suggereert dat cellen die dit eiwit niet konden herstellen een groot nadeel hadden en de tumorgroei niet konden volhouden.
Wat dit betekent voor toekomstige behandelingen
In het algemeen laat de studie zien dat glioblastoomcellen afhankelijk zijn van HNRNPH1 om een netwerk van genetische boodschappen correct te verwerken dat de celdeling regelt, waardoor ze kunnen prolifereren zonder zichzelf direct te vernietigen. Voor een lezer zonder specialistische kennis kan dit eiwit worden gezien als een redacteur achter de schermen die het instructieboekje van de kankercel leesbaar houdt. Het verstoren van HNRNPH1—of van de specifieke spleisingsevenementen die het controleert—zou tumorcellen vatbaarder kunnen maken voor fatale fouten tijdens deling, en zo een potentiële nieuwe route openen voor therapieën die glioblastoom voorbij zijn breekpunt duwen, als aanvulling op bestaande behandelingen.
Bronvermelding: Villa, G.R., Alimonti, P., Toker, J.S. et al. HNRNPH1 drives glioblastoma progression by regulating the splicing of cell cycle genes. Cell Death Dis 17, 352 (2026). https://doi.org/10.1038/s41419-026-08576-6
Trefwoorden: glioblastoom, celdeling, RNA-splijting, tumorbiologie, hersen‑kanker