Clear Sky Science · nl
Remming van Vaccinia-related kinase 2 onthult kwetsbaarheid van glutathionmetabolisme bij alvleesklierkanker
Waarom dit belangrijk is voor alvleesklierkanker
Alvleesklierkanker behoort tot de dodelijkste vormen van kanker, mede omdat standaardbehandelingen vaak tekortschieten. Deze studie onthult een verborgen zwakte in bepaalde alvleeskliertumoren: een afhankelijkheid van een cellair “schild” tegen giftige zuurstofbijproducten. Door te begrijpen wanneer dat schild kwetsbaar is en hoe een kankergen genaamd VRK2 het versterkt, suggereren de onderzoekers nieuwe manieren om kankercellen selectief te vergiftigen en tegelijkertijd gezond weefsel te sparen.
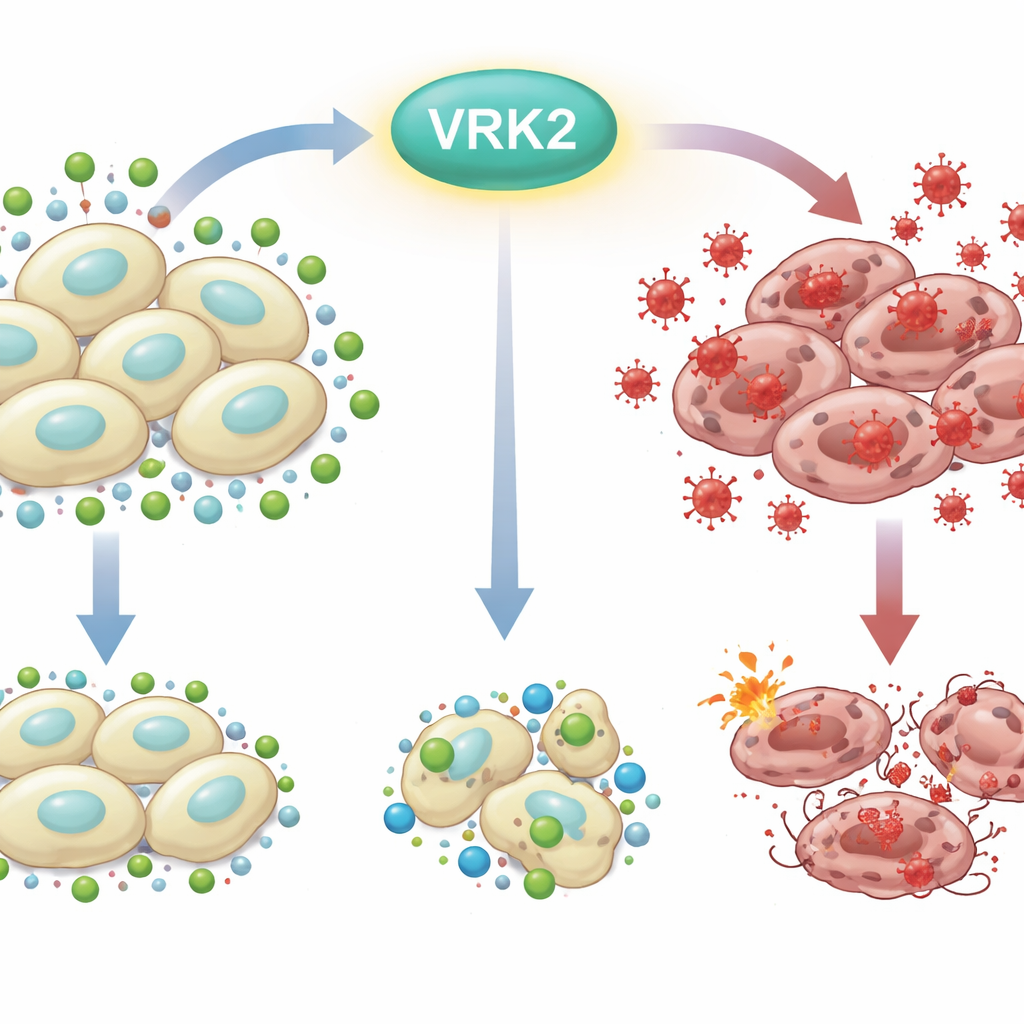
Het roestprobleem van de cel
Elke cel voert voortdurend strijd tegen “van binnenuit roesten” veroorzaakt door reactieve zuurstofsoorten—zeer reactieve vormen van zuurstof die DNA, vetten en eiwitten kunnen beschadigen. Om te overleven gebruiken cellen chemische verdedigingsmechanismen, waarbij glutathion een van de belangrijkste schilden vormt. Alvleesklierkankercellen, die onder zware omstandigheden leven en snel groeien, leunen sterk op metabolische trucs om voldoende glutathion voorradig te houden. Het verstoren van dit evenwicht tussen schadelijke oxidanten en beschermende antioxidanten kan kankercellen over de rand duwen naar celdood.
Een verborgen zwakke plek vinden
De onderzoekers begonnen met het uitschakelen van VRK2, een kankerverhogend gen dat eerder in verband werd gebracht met slechte uitkomsten bij alvleesklierkanker, en testten vervolgens 281 stoffen die het metabolisme richten. Ze ontdekten dat cellen zonder VRK2 opvallend gevoelig waren voor geneesmiddelen die de glutathionproductie blokkeren. In deze VRK2-deficiënte cellen daalden de glutathionniveaus terwijl de reactieve zuurstof toenam, wat leidde tot celdood. Het toedienen van extra antioxidanten of glutathionachtige moleculen redde de cellen, wat bevestigt dat de cruciale kwetsbaarheid precies lag in hun verminderde vermogen om oxidatieve stress te ontgiften.
Hoe VRK2 kankercellen helpt bewapenen
Vervolgens vroeg het team zich af waarom VRK2 het glutathionmetabolisme verandert. Ze richtten zich op een transportereiwit genaamd SLC7A11, dat in het buitenmembraan van de cel zit en cystine binnensmokkelt, een bouwsteen die nodig is om glutathion te maken. Verrassend genoeg veranderde VRK2 niet in welke hoeveelheid SLC7A11 de cel totaal produceerde; in plaats daarvan bepaalde het of die transporter succesvol het celoppervlak bereikte. In gezonde VRK2-actieve cellen reist SLC7A11 van het endoplasmatisch reticulum naar het Golgi en vervolgens naar het membraan. VRK2 bevordert dit transport door een cargo-sorterend eiwit genaamd Sec24C chemisch te modificeren, wat helpt SLC7A11 in vervoersblaasjes te laden. Wanneer VRK2 ontbreekt of wordt geblokkeerd, blijft SLC7A11 vastzitten in de cel, bereiken minder transporters het oppervlak en verzwakt het glutathionschild.
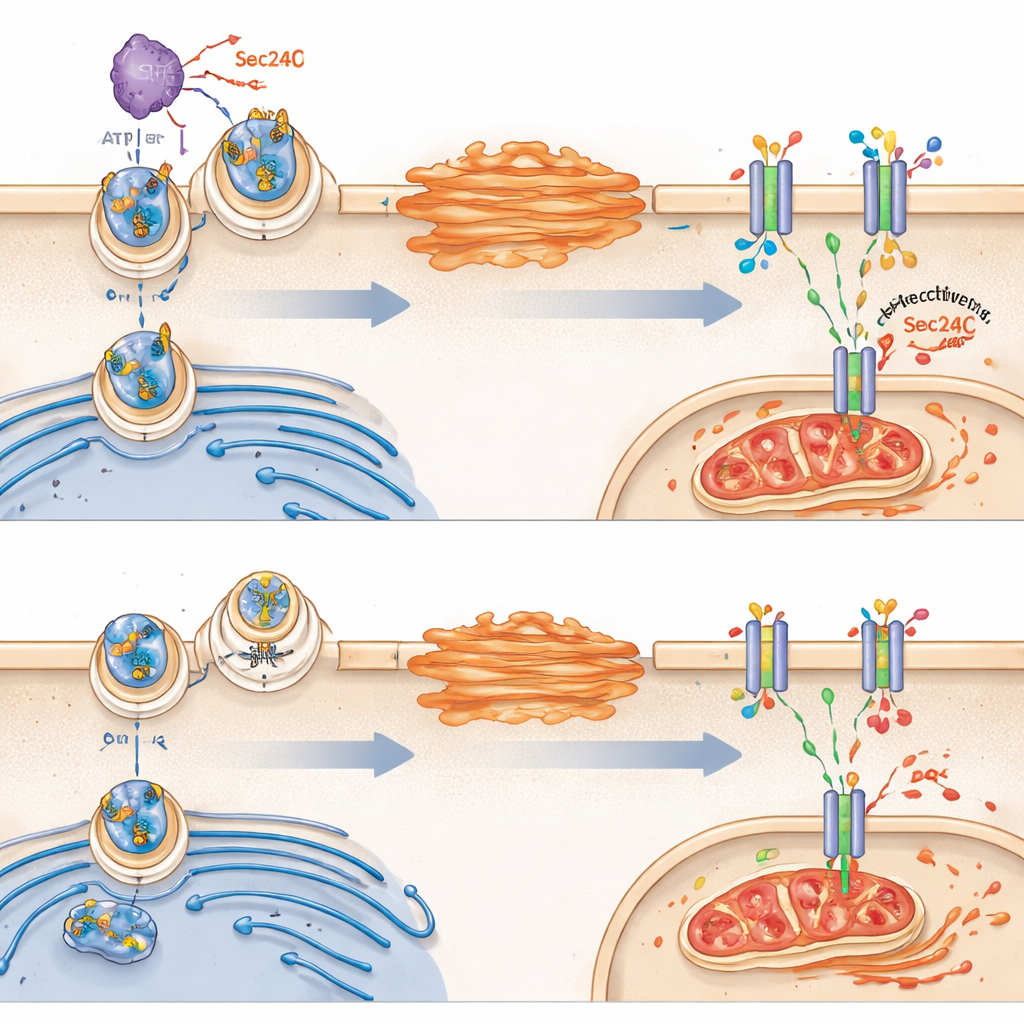
Van gebroken schild naar ferroptose
Zonder voldoende membraan-SLC7A11 hebben VRK2-deficiënte cellen moeite met het importeren van cystine en het behouden van glutathion. Dit maakt ze bijzonder kwetsbaar voor een vorm van ijzerafhankelijke celdood die ferroptose wordt genoemd, gekenmerkt door escalerende oxidatie van membraanvetten en mitochondriale schade. De studie toonde aan dat geneesmiddelen die de glutathionsynthese afsnijden tekenen van ferroptose teweegbrachten in VRK2-deficiënte cellen, inclusief vervormde mitochondriën en ophoping van lipide-oxidatieproducten. Het blokkeren van ferroptose, maar niet van andere vormen van celdood, beschermde deze cellen, wat benadrukt dat hun achilleshiel een onvermogen is om oxidatieve schade te beheersen.
Het sturen van gepersonaliseerde behandelkeuzes
Tot slot brachten de onderzoekers het werk naar diermodellen en cellen die recent van patiënten waren afgeleid. Tumoren met lage VRK2-niveaus krompen wanneer ze behandeld werden met een glutathion-gerichte stof, terwijl tumoren met hoge VRK2-expressie er grotendeels tegen bestand waren. Echter, toen VRK2-hoge tumoren ook een VRK2-remmer kregen, herkregen ze gevoeligheid voor glutathioninhibitie. Dit suggereert dat VRK2-niveaus patiënten kunnen indelen in groepen: degenen wier tumoren van nature kwetsbaar zijn voor glutathiongerichte therapie, en degenen die baat kunnen hebben bij een tweesporenstrategie die eerst VRK2 uitschakelt en vervolgens het glutathionmetabolisme aanvalt.
Wat dit betekent voor patiënten
Kort gezegd laat dit werk zien dat sommige alvleesklierkankers overleven door VRK2 te gebruiken om hun antioxidatieve schild sterk te houden. Haal VRK2 weg en dat schild wordt dunner; haal daarnaast glutathion weg en de kankercellen bezwijken onder oxidatieve stress. Het meten van VRK2 in tumoren zou artsen daarom kunnen helpen bepalen wie het meest waarschijnlijk profiteert van middelen die het glutathionmetabolisme verstoren, en wie eerst een VRK2-richting nodig heeft. Hoewel meer testen bij mensen nodig is, schetst de studie een helder pad naar meer op maat gemaakte, metabolisme-gebaseerde therapieën voor een kanker die dringend betere opties nodig heeft.
Bronvermelding: Chen, S., Fu, X., Zhang, T. et al. Vaccinia-related kinase 2 inhibition elicits vulnerability of glutathione metabolism in pancreatic cancer. Cell Death Dis 17, 325 (2026). https://doi.org/10.1038/s41419-026-08573-9
Trefwoorden: alvleesklierkanker, glutathionmetabolisme, VRK2, ferroptose, SLC7A11