Clear Sky Science · nl
Onderdrukking van EGFR door nieuwe biguanide 4C versterkte gevoeligheid van eierstokkanker voor PARP-remmers via downregulatie van BRCA2 en Rad51
Waarom dit onderzoek ertoe doet
Voor veel mensen bij wie eierstokkanker wordt vastgesteld, werken de huidige gerichte geneesmiddelen slechts voor een kleine minderheid van wie de tumoren specifieke genetische defecten dragen. Deze studie onderzoekt een manier om de voordelen van een belangrijke klasse medicijnen, PARP-remmers genoemd, uit te breiden naar de veel grotere groep patiënten wiens tumoren die mutaties niet hebben. Door een nieuw experimenteel molecuul te combineren met bestaande geneesmiddelen laten de onderzoekers een strategie zien om kankercellen in een dodelijke impasse te duwen terwijl gezond weefsel gespaard blijft.
Een knelpunt in de huidige behandeling van eierstokkanker
Eierstokkanker wordt vaak laat ontdekt en blijft een van de dodelijkste vormen van kanker bij vrouwen. PARP-remmers, zoals olaparib, kunnen opmerkelijk effectief zijn, maar voornamelijk bij patiënten waarvan de tumoren al defecten hebben in een DNA-herstelroute die samenhangt met de BRCA1- en BRCA2-genen. De meeste tumoren hebben echter nog intacte herstelmechanismen en kunnen de DNA-schade veroorzaakt door deze medicijnen repareren, waardoor kankercellen overleven. Een belangrijk onderdeel van dit herstel bestaat uit twee eiwitten, BRCA2 en Rad51, die gebroken DNA-strengen helpen herstellen via een proces dat homologe recombinatie heet. Manieren vinden om deze herstelroute selectief te verzwakken in kankercellen zou PARP-remmers voor veel meer patiënten bruikbaar kunnen maken.
De rol van een bekend groeischema
Het team richtte zich op een veelvoorkomend kancerelated molecuul, de epidermale groeifactorreceptor (EGFR), die op het oppervlak van veel tumorcellen zit en hun groei aanstuurt. Ze vonden dat EGFR meer doet dan groeisignalen uitzenden: in eierstokkankercellen met normale BRCA-genen hing een hoog EGFR-gehalte samen met een slechte overleving van patiënten en resistentie tegen PARP-remmers. Wanneer EGFR werd verminderd of uitgeschakeld in kweekcellen en muismodellen, werden tumoren veel gevoeliger voor olaparib. De onderzoekers toonden aan dat EGFR helpt BRCA2 en Rad51 naar de celkern te brengen na DNA-schade, waar ze breuken kunnen repareren en de impact van behandeling kunnen afzwakken. Simpelweg de enzymatische activiteit van EGFR blokkeren was niet voldoende; de totale hoeveelheid EGFR-eiwit moest worden verlaagd om deze herstelroute significant te verstoren.
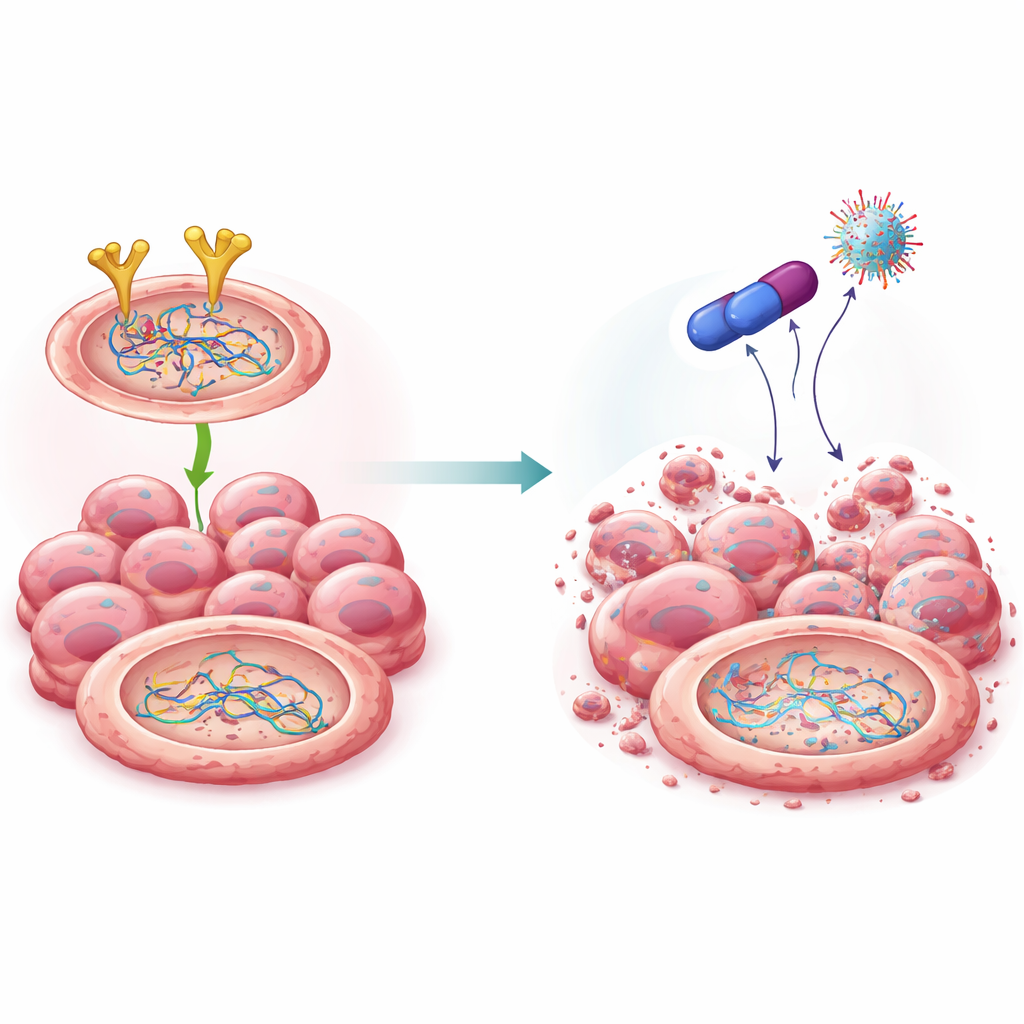
Een nieuw verbinding die de herstelploeg ontwapent
Voortbouwend op eerder werk met een geneesmiddel-familie die bekendstaat als biguaniden, synthetiseerden de wetenschappers verschillende chemische verwanten en identificeerden één opvallend molecuul, genoemd 4C. Deze verbinding was sterk toxisch voor eierstokkankercellen maar relatief mild voor normale cellen. Computermodellering en laboratoriumtests gaven aan dat 4C direct aan EGFR bindt en het markeert voor afbraak in het eiwitafbrekende systeem van de cel. Anders dan sommige bestaande EGFR-middelen verminderde 4C de totale hoeveelheid EGFR in plaats van alleen de activiteit ervan te onderdrukken. Naarmate EGFR-niveaus daalden, nam ook de stabiliteit van BRCA2 en Rad51 af: ze werden gemarkeerd voor verwijdering, afgebroken en waren niet langer in staat om efficiënt DNA-herstel te ondersteunen. Belangrijk is dat deze snoeiing op eiwitniveau plaatsvond zonder de onderliggende genen te veranderen.
Een reddingsroute in de cel blokkeren
De studie onthulde een meer gedetailleerde keten van gebeurtenissen die DNA-schade verbindt met tumorovertleving. Nadat PARP-remmers het DNA beschadigen, stuurt een ander sensor-eiwit, ATM, een signaal van de kern naar het cellichaam. In reactie daarop werkt EGFR samen met BRCA2 en Rad51 en helpt hen de kern binnen te gaan, waar ze de schade repareren. De onderzoekers ontdekten dat een derde eiwit, c-Cbl, normaal gesproken fungeert als een soort etiketteerder voor verwijdering van BRCA2 en Rad51. EGFR concurreert met c-Cbl om toegang tot deze herstelproteïnen en beschermt ze zo tegen markering voor afbraak. Wanneer 4C de EGFR-niveaus verlaagt, kan c-Cbl makkelijker binden aan BRCA2 en Rad51, wat leidt tot hun markering, afbraak en verlies. Met minder herstelproteïnen in de kern hopen DNA-laesies zich op en worden kankercellen veel gevoeliger voor PARP-remmers.
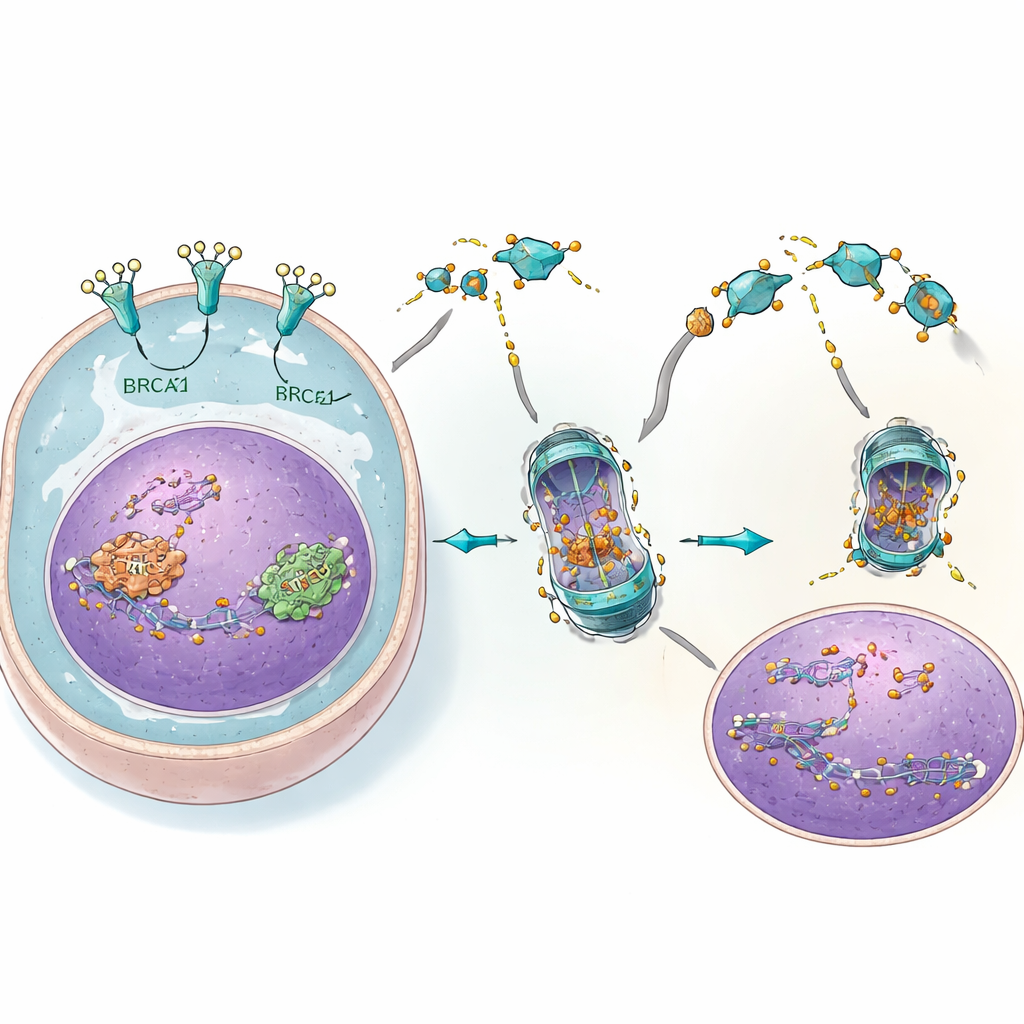
Van cellen naar dieren: een krachtige combinatie
In zowel gecultiveerde cellen als muismodellen produceerde de combinatie van 4C met PARP-remmers een krachtige tweeslag. Tumoren met normale BRCA-genen die resistent waren tegen elk geneesmiddel afzonderlijk, krimpten dramatisch of stopten met groeien wanneer ze aan beide tegelijk werden blootgesteld. Markers van DNA-schade stegen sterk, wat consistent is met het idee dat het herstel werd overweldigd. Tegelijkertijd lieten normale cellen en belangrijke organen zoals de lever en nieren weinig aanwijzingen van schade zien, waarschijnlijk omdat zij veel lagere EGFR-niveaus hebben en minder afhankelijk zijn van deze specifieke herstelomweg. De voordelen van de combinatie strekten zich ook uit tot het verminderen van de verspreiding van eierstokkankercellen in het lichaam.
Wat dit zou kunnen betekenen voor patiënten
Dit werk stelt een manier voor om de kracht van een kankercel in een zwakte te veranderen. Door EGFR te richten met de nieuwe verbinding 4C, ontdoen de onderzoekers tumoren van de bescherming die BRCA2 en Rad51 bieden, waardoor tumoren met verder normaal DNA-herstel zich meer als BRCA-gemuteerde kankers gedragen in hun reactie op PARP-remmers. Deze afgedwongen kwetsbaarheid, bekend als "synthetische lethality," zou het bereik van bestaande geneesmiddelen voor veel meer vrouwen met eierstokkanker kunnen vergroten, terwijl bijwerkingen beheersbaar blijven. Hoewel 4C nog experimenteel is en uitgebreide tests in meer geavanceerde modellen en klinische onderzoeken zal vereisen, biedt de studie een duidelijk stappenplan voor hoe het ontmantelen van specifieke herstelhelpers in tumorcellen de behandeluitkomsten zou kunnen verbeteren.
Bronvermelding: Xiao, D., Yao, J., Yang, X. et al. Repression of EGFR by new biguanide 4C potentiated ovarian cancer to PARP inhibitors through down-regulation of BRCA2 and Rad51. Cell Death Dis 17, 317 (2026). https://doi.org/10.1038/s41419-026-08556-w
Trefwoorden: eierstokkanker, PARP-remmers, EGFR, DNA-herstel, gerichte therapie