Clear Sky Science · nl
Verlies van PRKACB bevordert metastase van diffuse maagkanker via activatie van RhoA-signaalgeving
Waarom deze studie belangrijk is voor maagkanker
Diffuse maagkanker is een bijzonder agressieve vorm van maagkanker die vaak wijdverspreid in de buik voorkomt, waardoor behandeling moeilijk is en de prognose slecht. Deze studie onderzoekt waarom deze tumoren zo vatbaar zijn voor uitzaaiing en onthult een moleculair remsysteem dat normaal voorkomt dat kankercellen wegtrekken — en laat zien wat er gebeurt wanneer die rem faalt. Inzicht in deze verborgen schakelaar kan nieuwe wegen openen om te voorspellen welke patiënten het grootste risico lopen en om geneesmiddelen te ontwikkelen die gevaarlijke verspreiding vertragen of stoppen.
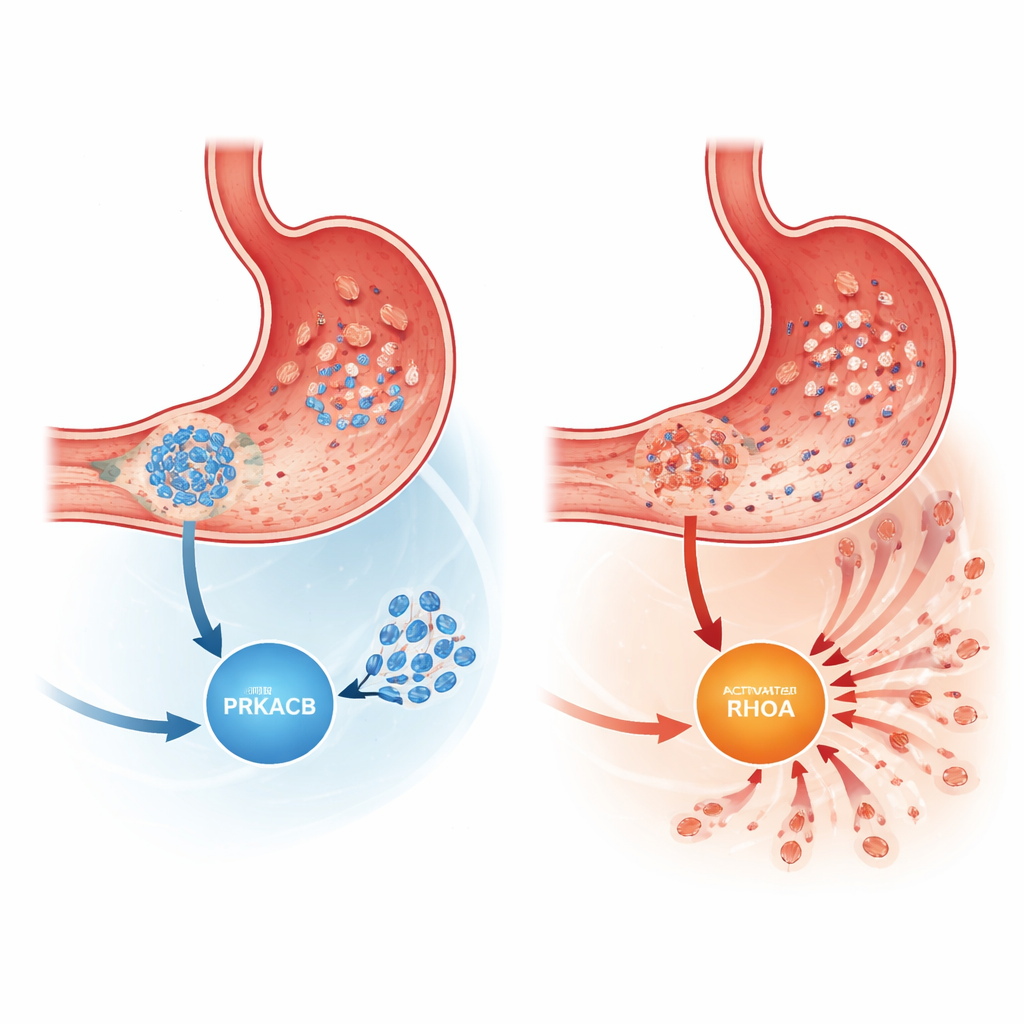
Een gevaarlijke vorm van maagkanker
Niet alle maagkankers gedragen zich hetzelfde. Intestinaire tumoren vormen vaak meer gestructureerde massa’s, terwijl diffuse maagkanker (DGC) bestaat uit verspreide cellen die gemakkelijk van de primaire tumor wegglippen. Patiënten met DGC hebben een hoger sterfterisico dan patiënten met intestinale tumoren, deels omdat hun tumoren makkelijker nieuwe groeisels door de buikholte verspreiden. Eerdere genetische studies hadden DGC al gekoppeld aan terugkerende veranderingen in het gen RHOA, dat de beweging en vorm van cellen beïnvloedt. Het was echter onduidelijk hoe die veranderingen verband hielden met de bredere signaalnetwerken die bepalen of kankercellen blijven zitten of migreren.
Het vinden van een ontbrekende rem in tumormonsters
De onderzoekers concentreerden zich op een eiwit genaamd PRKACB, een catalytische subeenheid van het bekende enzym proteïnekinase A, dat vele celprocessen fijnregelt door fosfaatgroepen aan andere eiwitten toe te voegen. Een eerdere proteomics-enquête suggereerde dat PRKACB-niveaus ongewoon laag waren in agressieve DGC. Om dit te testen onderzochten de onderzoekers tumormonsters van 376 patiënten, waarbij ze diffuse- en intestinale tumoren en het omliggende niet-kankerachtige weefsel vergeleken. Ze vonden dat PRKACB-niveaus duidelijk verlaagd waren in diffuse tumoren, vooral in gevorderde stadia, maar niet in intestinale tumoren. Patiënten van wie de tumoren weinig PRKACB hadden, hadden een significant slechtere algemene overleving, zelfs na correctie voor andere klinische factoren, wat suggereert dat PRKACB in deze context als tumorrepressor functioneert.
Hoe laag PRKACB celontsnapping aanwakkert
Om te zien wat PRKACB in kankercellen doet, gebruikten de onderzoekers gekweekte cellijnen die DGC nabootsen. Wanneer ze PRKACB kunstmatig verlaagden, werden de cellen beweeglijker en invasiever in laboratoriumtests: ze persten zich gemakkelijker door barrières en vormden vingervormige uitlopers, pseudopodia genoemd, die cellen helpen kruipen. Deze cellen schakelden ook over van een meer geordende epitheliale toestand naar een lossere, mesenchymale-achtige toestand die samenhangt met metastasering, waarbij ze het adhesiemolecuul E‑cadherine verloren dat cellen normaal bij elkaar houdt. Omgekeerd maakte het verhogen van PRKACB de cellen minder migratoir en minder invasief. Belangrijk is dat deze veranderingen de celdelingssnelheid niet beïnvloedden, wat wijst op een specifieke rol van PRKACB bij het mogelijk maken van verspreiding en niet bij groei.
Inzoomen op de RhoA-signaalschakelaar
De onderzoekers vroegen vervolgens hoe PRKACB dit anti-metastatische effect uitoefent. Met eiwit–eiwit interactiemethoden en structurele modellering toonden ze aan dat PRKACB direct bindt aan RhoA, een moleculaire schakelaar die tussen inactieve en actieve vormen wisselt om celvorm en -beweging te regelen. PRKACB plaatst een fosfaatgroep op een specifieke positie van RhoA (serine 188), waardoor RhoA wordt geremd en de downstream ROCK- en FAK-pathways die cytoskelettransformaties en celmotiliteit aansturen, worden gedempt. Wanneer PRKACB werd onderdrukt, was RhoA minder gefosforyleerd, actiever en nam de ROCK/FAK-signaalgeving toe, wat leidde tot agressievere celbeweging. In muismodellen waarbij mensachtige tumoren in de maagwand werden geïmplanteerd, veroorzaakte verlaagde PRKACB meer en grotere metastatische knobbels in de buik en een eerdere zichtbare verspreiding, wederom zonder verandering in de groeisnelheid van gevestigde metastasen.
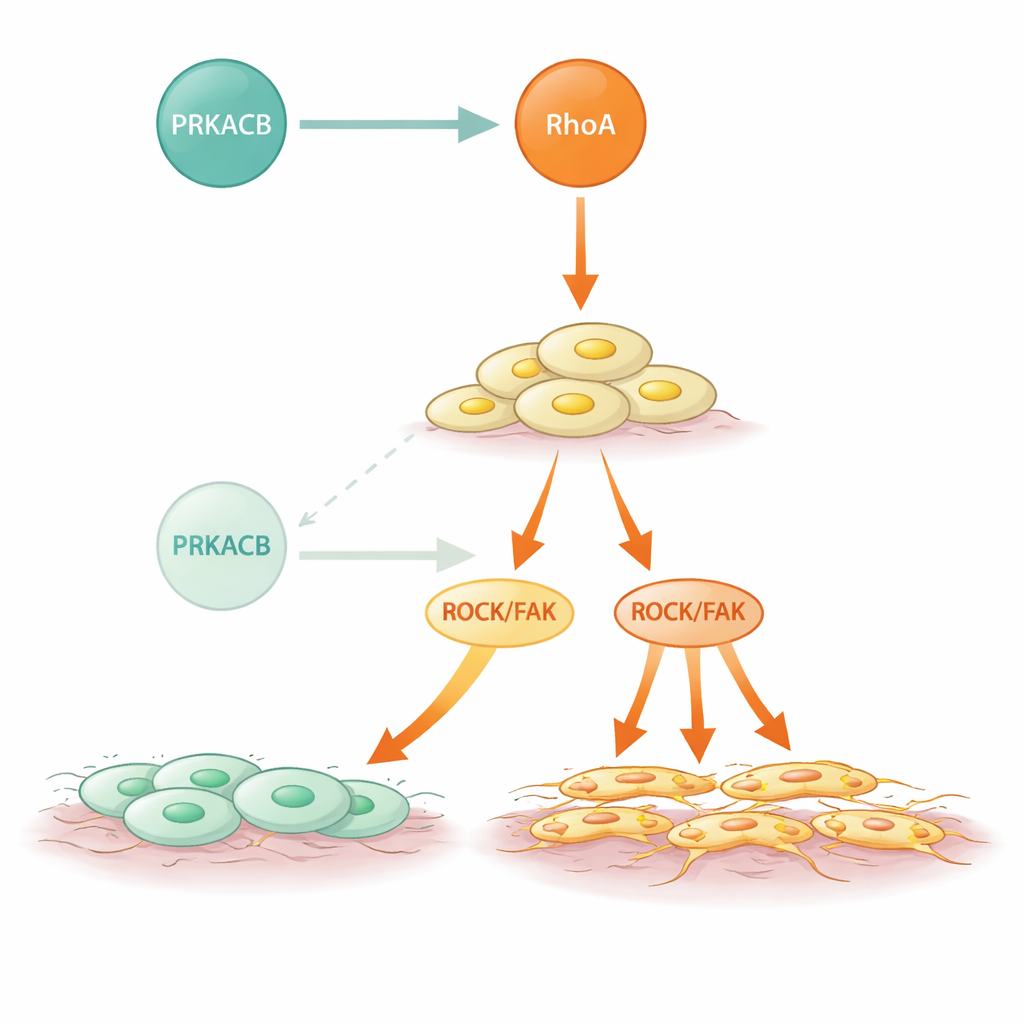
Mutante signaalgeving en een mogelijke interventie
Diffuse maagkankers dragen vaak RHOA-mutaties en deze studie laat zien hoe sommige van die veranderingen het probleem verergeren. Meerdere veelvoorkomende DGC-geassocieerde mutaties in RhoA verzwakten of maakten de binding met PRKACB ongedaan, maar belemmerden RhoA’s vermogen om zijn downstream partners te activeren niet. Daardoor ontliepen deze mutante vormen de remmende fosforylering door PRKACB en toonden ze verhoogde ROCK-activiteit en sterkere invasief gedrag. Opmerkelijk genoeg keerde behandeling van cellen en muizen met een RhoA-remmende verbinding de extra metastase veroorzaakt door laag PRKACB grotendeels om. Dit suggereert dat zelfs in tumoren waar de natuurlijke rem zwak of afwezig is, het direct targeten van de overactieve RhoA-route de verspreiding kan beperken.
Wat dit betekent voor patiënten en toekomstige therapieën
Kort gezegd identificeert dit werk PRKACB als een sleutelcomponent van een intern “anti-migratie”-circuit in diffuse maagkanker. Wanneer PRKACB-niveaus dalen, of wanneer RhoA zodanig gemuteerd is dat PRKACB er niet aan kan binden en het niet kan modificeren, loopt RhoA-signaalgeving op en worden kankercellen beter in staat om los te breken en de buikholte te koloniseren. Het meten van PRKACB- en RhoA-status in tumoren kan artsen helpen inschatten hoe waarschijnlijk het is dat iemands kanker zal uitzaaien en wie het meest zou profiteren van geneesmiddelen die de RhoA–ROCK–FAK-route remmen. Hoewel zulke behandelingen verdere ontwikkeling en klinische tests vereisen, legt de studie een duidelijke moleculaire route bloot van een ontbrekende rem naar dodelijke verspreiding — en wijst ze op nieuwe manieren om die reis te vertragen.
Bronvermelding: Sun, J., Zhao, J., Yang, X. et al. Loss of PRKACB facilitates metastasis of diffuse-type gastric cancer through RhoA signaling activation. Cell Death Dis 17, 281 (2026). https://doi.org/10.1038/s41419-026-08553-z
Trefwoorden: diffuse maagkanker, metastase, PRKACB, RhoA-signaalgeving, ROCK FAK-route