Clear Sky Science · nl
Lang niet-coderend RNA ADEI/miR-93-3p/STAT3-as bevordert progressie en immuunontduiking van Epstein–Barrvirus-positieve diffuus grootcellig B‑cellymfoom via regulatie van de PD-1/PD-L1-checkpoint
Waarom dit belangrijk is voor onze immuunverdediging
Sommige lymfomen die verbonden zijn aan het veelvoorkomende Epstein–Barr-virus (EBV) zijn bijzonder moeilijk te behandelen en ontkomen vaak aan de immuunreactie van het lichaam. Deze studie onthult een verborgen boodschapsysteem binnen deze kankers: kleine blaasjes genaamd exosomen die een lang RNA-molecuul vervoeren dat tumoren helpt groeien en zich te verbergen voor immuuncellen. Inzicht in deze geheime communicatie kan nieuwe wegen openen om deze hardnekkige bloedkankers te diagnosticeren en te behandelen.
Een virus dat het evenwicht verstoort
Diffuus grootcellig B‑cellymfoom (DLBCL) is het meest voorkomende agressieve lymfoom. Wanneer tumorcellen EBV dragen, reageren patiënten doorgaans slechter op standaard chemo-immunotherapie. De onderzoekers vergeleken eerst in het laboratorium EBV‑positieve en EBV‑negatieve lymfoomcellen. Ze ontdekten dat EBV-infectie lymfoomcellen sneller liet delen, meer kolonies liet vormen en grotere tumoren in muizen veroorzaakte. EBV‑positieve cellen toonden ook meer van een oppervlaktemolecuul genaamd PD‑L1, dat met PD‑1 op immuuncellen interageert om hun aanval uit te schakelen. Toen het team lymfoomcellen mengde met doder CD8-T-cellen, verminderden EBV‑positieve tumoren het aantal en de werkzaamheid van deze T‑cellen — een effect dat ongedaan kon worden gemaakt met antilichamen die de PD‑1/PD‑L1-rem blokkeren.
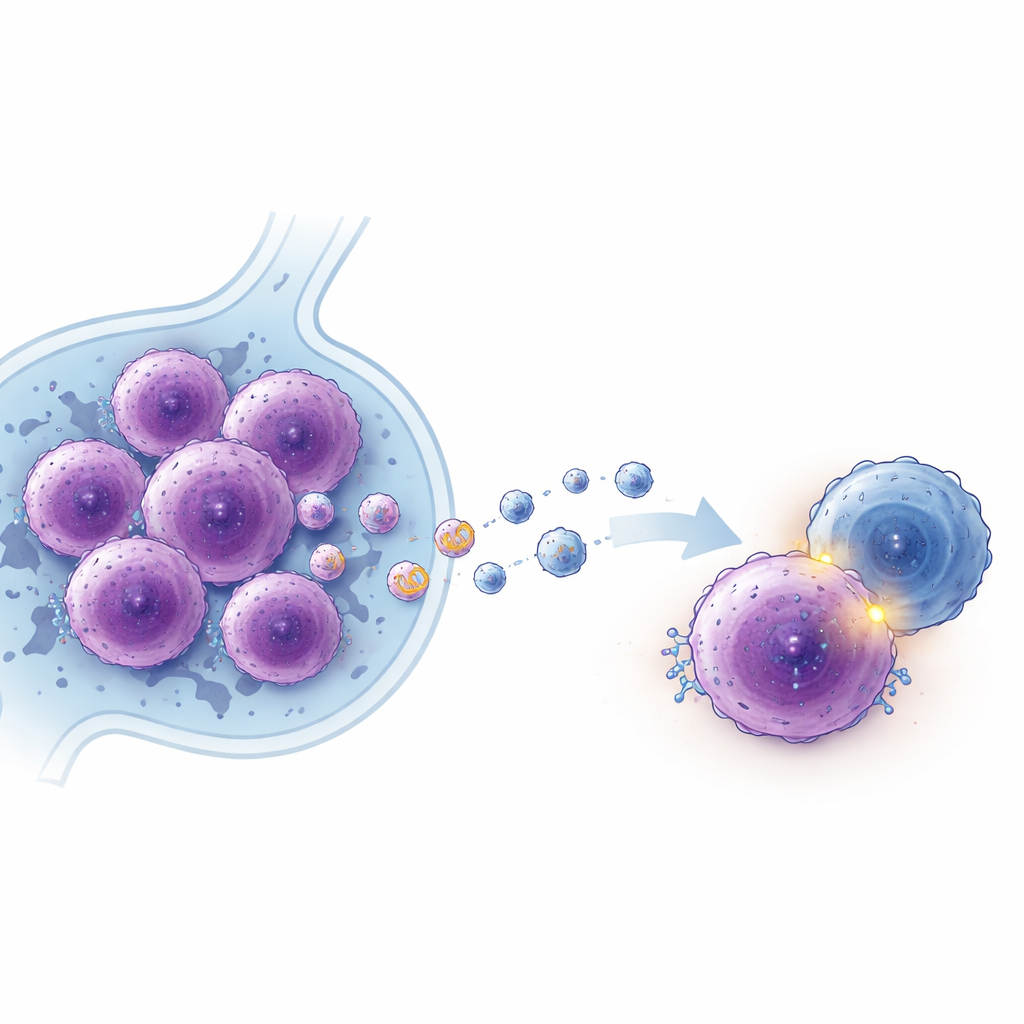
Een lang RNA dat tumoren helpt groeien en verbergen
Om te begrijpen hoe EBV het gedrag van tumoren herschikt, onderzochten de onderzoekers lange niet-coderende RNA’s — RNA‑stukken die geen eiwitten maken maar veel celprocessen kunnen reguleren. Door de RNA‑samenstelling van exosomen vrijgegeven door EBV‑positieve en EBV‑negatieve DLBCL‑cellen te scannen, ontdekten zij een eerder niet-gekarakteriseerd RNA, dat zij lncADEI noemden en dat sterk verhoogd was in EBV‑positieve cellen en hun exosomen. Wanneer zij lymfoomcellen dwongen meer lncADEI te produceren, deelden de cellen sneller, vormden ze meer kolonies en weerstonden ze geprogrammeerde celdood. Het verminderen van lncADEI had het tegenovergestelde effect: de groei vertraagde en de celdood nam toe, zowel in kweek als in muizen tumormodellen.
Hoe lncADEI immuunontduiking herbedraadt
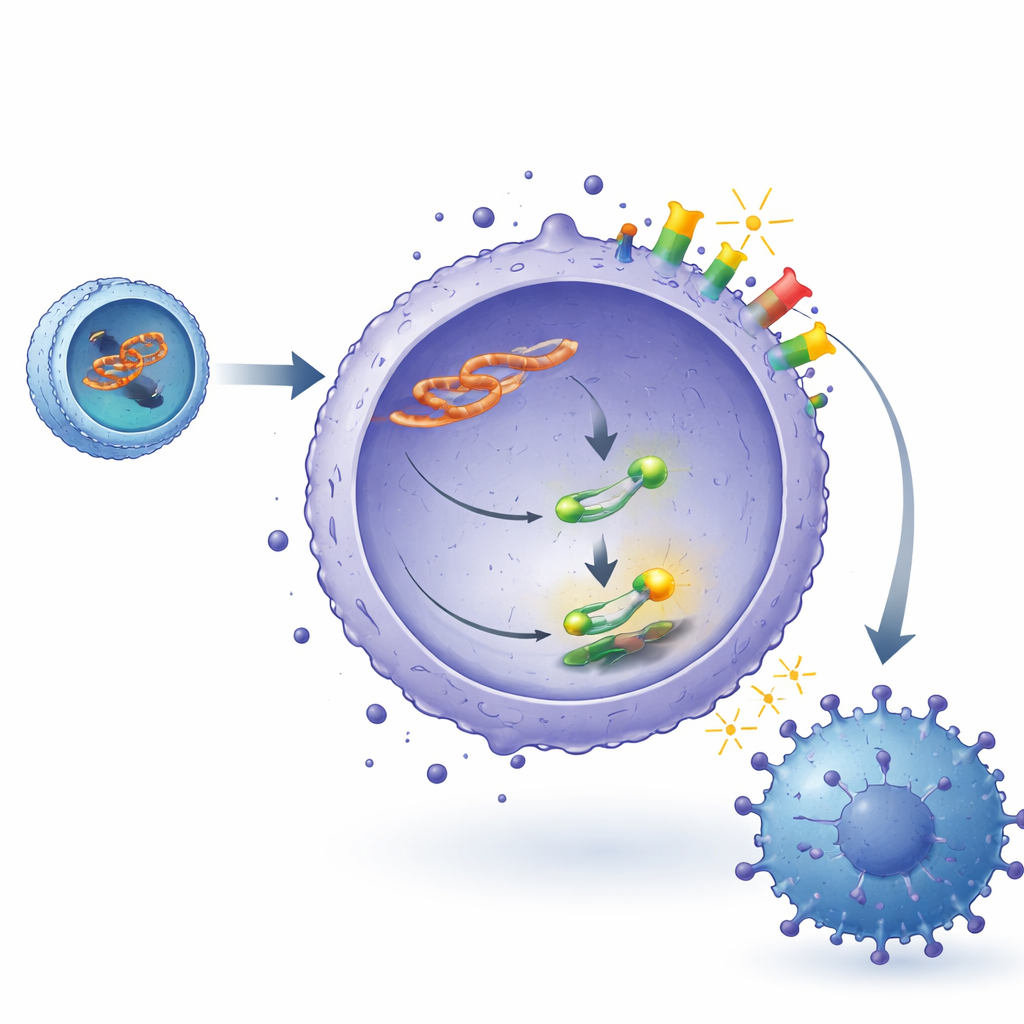
De onderzoekers volgden vervolgens hoe lncADEI verbonden is met de PD‑1/PD‑L1-immuuncheckpoint. Binnen lymfoomcellen bevindt lncADEI zich voornamelijk in het cytoplasma, waar het werkt als een spons voor een klein regulatorisch RNA genaamd miR‑93‑3p. Onder normale omstandigheden helpt miR‑93‑3p een belangrijk signaalproteïne, STAT3, onder controle te houden door zich aan zijn boodschapper-RNA te binden en de productie ervan te beperken. Wanneer lncADEI miR‑93‑3p opvangt, wordt er meer STAT3 gemaakt en geactiveerd. STAT3 bindt op zijn beurt rechtstreeks aan het controlegebied van het PD‑L1-gen in lymfoomcellen en verhoogt de PD‑L1-productie. Deze keten — lncADEI die miR‑93‑3p blokkeert, STAT3 vrijmaakt en PD‑L1 aandrijft — resulteert in hogere PD‑L1-expressie op tumorcellen, sterkere uitschakelsignalen naar CD8‑T‑cellen en verminderde T‑celactiviteit.
Exosomaal "post" dat schadelijke instructies verspreidt
EBV‑positieve lymfoomcellen houden lncADEI niet voor zichzelf. Ze scheiden veel meer exosomen uit dan EBV‑negatieve cellen, en deze exosomen zitten vol met lncADEI. Wanneer EBV‑negatieve lymfoomcellen werden blootgesteld aan exosomen van EBV‑positieve cellen, namen ze deze op, steeg hun interne lncADEI-gehalte en begonnen ze zich agressiever te gedragen — sneller delen en meer kolonies vormen. In gemengde kweeken met T‑cellen verminderden exosomen verrijkt met lncADEI het aantal en de dodelijke werking van CD8‑T‑cellen en verhoogden ze PD‑1 op deze immuuncellen, wat de immuunrespons verder verzwakte. Dit suggereert dat EBV‑positieve tumoren naburige tumorcellen kunnen "oplijnen" en hun micro‑omgeving kunnen herstructureren via lncADEI‑rijke exosomen.
Aanwijzingen uit patiëntbloedmonsters
Om deze laboratoriumbevindingen aan echte ziekte te koppelen, maten de onderzoekers lncADEI in bloedexosomen van 47 patiënten met DLBCL. Degenen wier tumoren EBV‑positief waren, hadden significant hogere niveaus van exosomaal lncADEI dan EBV‑negatieve patiënten. Hoge lncADEI in het bloed werd ook geassocieerd met een verder gevorderd ziektestadium, een agressievere tumortype, hogere standaard risicoscores en verhoogde markers van weefselschade. Deze patronen suggereren dat exosomaal lncADEI in het bloed als een minimaal invasieve indicator van EBV‑gedreven lymfoom en de ernst ervan zou kunnen dienen.
Wat dit betekent voor toekomstige zorg
In eenvoudige bewoordingen onthult dit werk een drie‑stappentruc die door EBV‑gerelateerde lymfomen wordt gebruikt: ze overproduceren een lang RNA (lncADEI), verpakken het in reizende blaasjes en gebruiken het zowel binnen de tumor als in naburige cellen om een bekende immuunrem, PD‑L1, op te voeren. Het resultaat is snellere tumorgroei en een gedempte T‑celaanval. Omdat elke stap in deze keten — lncADEI zelf, de interactie met miR‑93‑3p en STAT3, en de afgifte van lncADEI‑rijke exosomen — een mogelijk aangrijpingspunt of meetpunt biedt, wijst de studie op nieuwe strategieën om immunotherapie te verbeteren en EBV‑geassocieerde lymfomen te monitoren met een eenvoudige bloedtest.
Bronvermelding: Zheng, W., Lai, G., Liao, Z. et al. Long noncoding RNA ADEI/miR-93-3p/STAT3 axis promotes Epstein–Barr virus-positive diffuse large B-cell lymphoma progression and immune evasion through regulating the PD-1/PD-L1 checkpoint. Cell Death Dis 17, 280 (2026). https://doi.org/10.1038/s41419-026-08532-4
Trefwoorden: Epstein–Barr-virus lymfoom, immuuncheckpoint, lang niet-coderend RNA, exosomen, STAT3-signaaltransductie