Clear Sky Science · nl
Nucleair myosine 1 koppelt genomische architectuur aan herstructurering van vetweefsel, metabole ontsteking en obesitas bij muizen
Waarom het cel-skelet ertoe doet voor lichaamsvet
Obesitas wordt vaak toegeschreven aan wat we eten en hoeveel we bewegen, maar diep in onze cellen kan ook de manier waarop DNA is verpakt en afgelezen het evenwicht verstoren. Deze studie toont aan dat een klein motorisch eiwit, nucleair myosine 1 (NM1), dat helpt DNA in de celkern te organiseren, een verrassende rol speelt in hoe vetcellen zich vormen, energie opslaan en ontstekingsreacties opwekken. Door muizen te bestuderen die dit eiwit misten, onthulden de onderzoekers een directe link tussen de fysieke architectuur van onze genen en de ontwikkeling van ongezond visceraal vet en metabole problemen.
Van stamcellen naar vetcellen
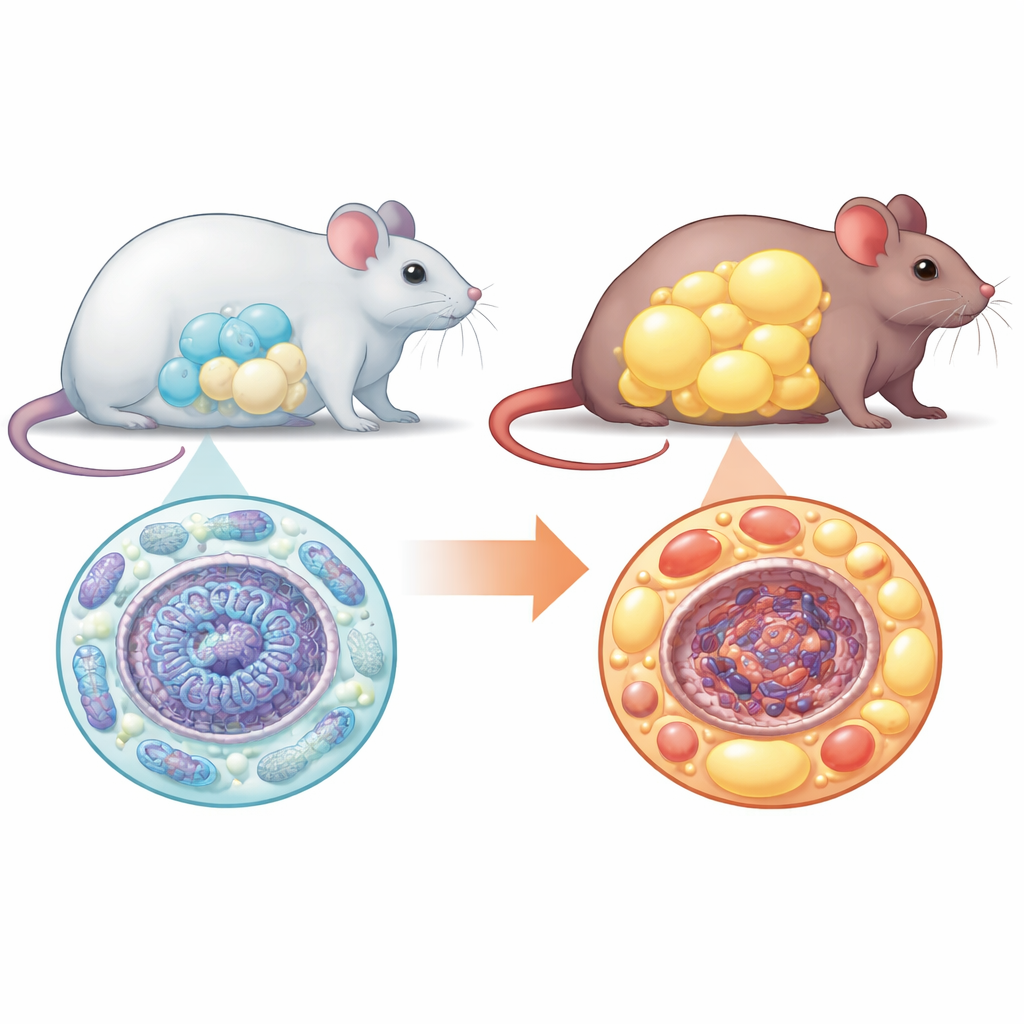
Vetcellen ontstaan uit veelzijdige voorlopers die mesenchymale stamcellen worden genoemd. Normaal gesproken delen deze voorlopers zich, schakelen ze hun energiemetabolisme om en rijpen ze uit tot veel kleine, goed functionerende vetcellen die overtollige calorieën veilig opslaan. Het team ontdekte dat dit ordelijke proces verstoord raakt zonder NM1. Wanneer ze stamcellen van normale en NM1-deficiënte muizen in het laboratorium lieten uitrijpen tot vetcellen, voltooiden veel minder cellen de transitie in afwezigheid van NM1. De cellen die wel rijpten, waren opvallend groter dan normaal, vol vet maar misten het gebruikelijke merkteken van gezonde vetcellen op gen- en proteïneniveau. Dit patroon – minder cellen maar elk vergroot – is kenmerkend voor ongezond vetweefsel.
Hoe genopslag het gedrag van vetcellen vormt
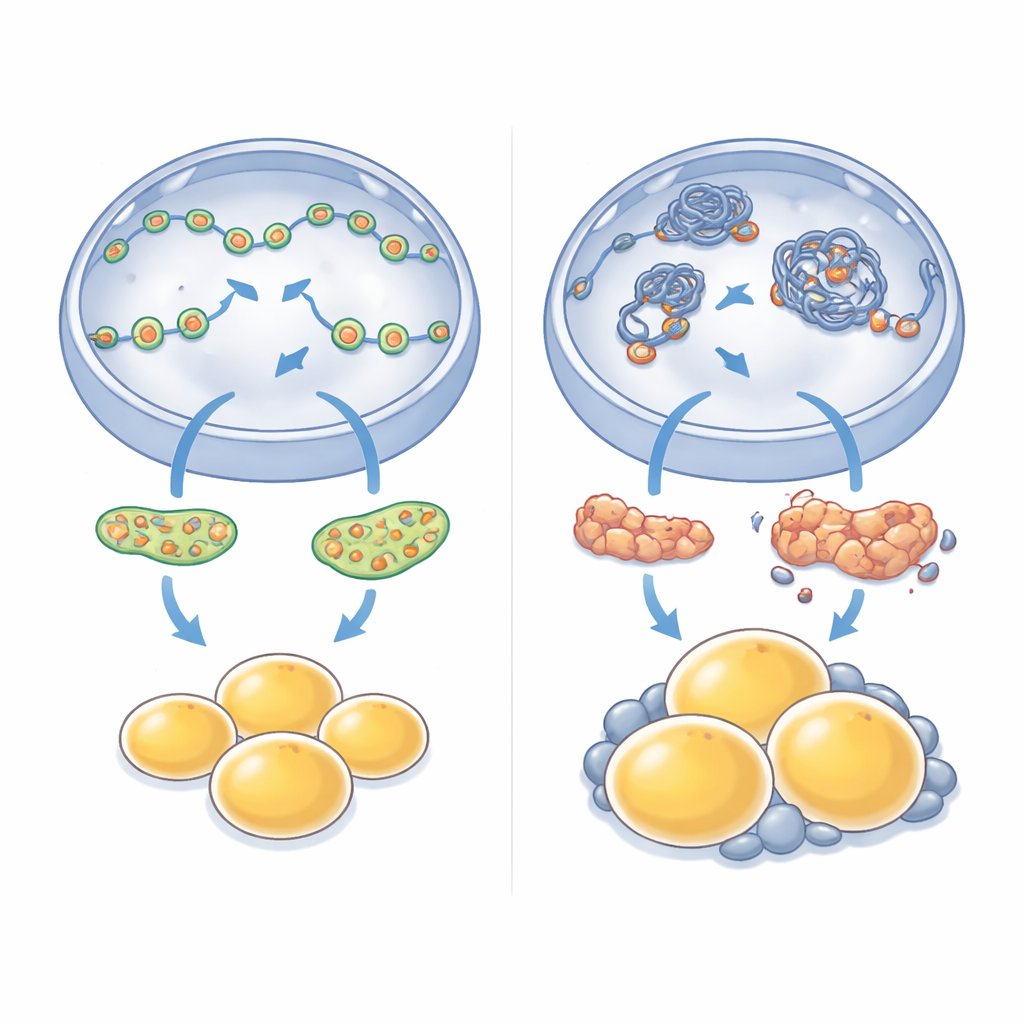
NM1 werkt in de kern, waar het helpt gedeeltes DNA toegankelijk te houden zodat belangrijke genen kunnen worden aangezet. Om te begrijpen hoe het verlies daarvan het celgedrag verandert, legden de onderzoekers kaarten van open DNA-regio’s naast metingen van genactiviteit in cellen met en zonder NM1. Ze zagen dat veel genen die nodig zijn voor vetcelvorming, het beheer van vetdruppels en het onderhoud van mitochondriën zowel toegankelijkheid als activiteit verloren wanneer NM1 ontbrak. Tegelijkertijd werden andere genen die betrokken zijn bij groeig- en signaalroutes opener en actiever. Dit wees op NM1 als een belangrijke verkeersregelaar: het helpt een evenwichtig landschap van open en gesloten DNA-regio’s te behouden zodat de juiste genetische netwerken gezonde vetcelontwikkeling en stofwisseling aansturen.
Wanneer lokale veranderingen leiden tot gewichtstoename in het hele lichaam
De gevolgen van het verlies van deze enkele nucleaire motor bleven niet beperkt tot cellen in een kweekschotel. Muizen zonder NM1 werden geleidelijk zwaarder dan hun normale nestgenoten, hoewel ze niet meer aten. Beeldvorming en weefselanalyse toonden een duidelijke ophoping van vet, vooral rond inwendige organen in de buik, en de individuele vetcellen in deze gebieden waren opvallend vergroot. Toen de onderzoekers maten welke genen in dit visceraal vet omhoog- of omlaagreguleerden, vonden ze ingrijpende veranderingen: routes die betrokken zijn bij energiegebruik, insulinesignalering en weefselherstructurering waren geherprogrammeerd. Genen die geassocieerd worden met vetcelgroei en -uitbreiding waren vaak verhoogd, terwijl meerdere centrale regelaars van gezonde vetcelvorming onderdrukt waren, wat de defecten weerspiegelde die in gekweekte stamcellen werden gezien.
Ontstoken vet en verstoorde energiecentrales
Buiten hun omvang vertoonde het vetweefsel van NM1-deficiënte muizen tekenen van ontsteking en metabole stress. Een gedetailleerde routeanalyse benadrukte sterke activatie van immuunsignalen aangedreven door moleculen zoals interferon-gamma en tumor necrose factor, die bekendstaan om bij te dragen aan insulineresistentie en metabole ziekte. Tegelijkertijd werden regulatoren die een rustig, energie-efficiënt vetweefsel ondersteunen onderdrukt. De studie koppelde het verlies van NM1 ook aan verstoorde mitochondriën – de energiecentrales van de cel. Genen die normaal de kwaliteit van mitochondriën bewaken en de verschuiving tussen efficiënte energieproductie en snelle glycolytische energie reguleren, waren verkeerd gereguleerd, wat suggereert dat vetcellen bij afwezigheid van NM1 een minder efficiënte, meer stressgevoelige energiestrategie aannemen.
Gedeelde signalen tussen muizen en mensen
Om te onderzoeken of deze nucleaire motorroute ook van belang kan zijn bij mensen, bestudeerden de auteurs grote genetische datasets van menselijk visceraal vet. Ze focusten op een menselijke verwant van NM1 genaamd MYO1C en keken naar netwerken van varianten die de activiteit van nabijgelegen genen bijsturen. Ze vonden dat veel van dezelfde thema’s die bij muizen voorkwamen – cytoskeletcontrole, immuunsignaleriging en metabole regulatie – ook opdoken in humane genennetwerken gecentreerd rond MYO1C. Meerdere genen die veranderd waren in NM1-deficiënt vet van muizen waren ook ingebed in deze menselijke netwerken en zijn gekoppeld aan herstructurering van vetweefsel en metabolisme. Deze soortoverschrijdende overlap suggereert dat vergelijkbare nucleaire mechanismen het obesitasrisico bij mensen kunnen beïnvloeden.
Wat dit betekent voor obesitas en metabole gezondheid
Alles bij elkaar laat het werk zien dat NM1 veel meer is dan een nucleaire hulp; het is een centraal knooppunt dat DNA-organisatie verbindt met hoe vetcellen groeien, energie opslaan en communiceren met het immuunsysteem. Wanneer NM1 ontbreekt, worden gen-schakelaars in vetvoorlopers verkeerd ingesteld, functioneren mitochondriën slecht, vermenigvuldigen vetcellen zich niet maar worden ze juist groter, en raakt visceraal vet ontstoken – een combinatie die lijkt op het ongezonde vet dat gezien wordt bij obesitas en insulineresistentie. Voor een niet-specialistische lezer is de boodschap dat de fysieke ordening van DNA en zijn helpers in de kern weefsels kan predisponeren voor gezonde of schadelijke vetuitbreiding. Eiwitten zoals NM1 en zijn menselijke tegenhanger MYO1C zouden mogelijk toekomstige therapeutische doelen kunnen zijn om vetweefsel van binnenuit te hervormen en zo obesitasgerelateerde ziekten preciezer aan te pakken.
Bronvermelding: Khalaji, S., Venit, T., Lukáčová, Z. et al. Nuclear Myosin 1 links genomic architecture to adipose tissue remodeling, metabolic inflammation and obesity in mice. Cell Death Dis 17, 270 (2026). https://doi.org/10.1038/s41419-026-08525-3
Trefwoorden: adipogenese, chromatine, mitochondriën, visceraal vet, metabole ontsteking