Clear Sky Science · nl
Trimethylatie van histon 3 lysine 36 door SETD2 vormt een epigenetisch landschap in intestinale stamcellen om vetstofwisseling te orkestreren en celsenescentie te verminderen
Waarom darmstamcellen ertoe doen naarmate we ouder worden
Diep in de bekleding van onze darmen werken kleine stamcellen onafgebroken om het weefsel te vernieuwen dat ons helpt voedsel te verteren en voedingsstoffen op te nemen. Naarmate we ouder worden, raken deze stamcellen uitgeput, waardoor de darm vatbaarder wordt voor ziekte en langzamer geneest. Deze studie onderzoekt hoe subtiele chemische labels op DNA-verpakkende eiwitten helpen intestinale stamcellen jong te houden, hoe het verlies ervan de vetverbranding in cellen verstoort, en hoe zorgvuldig gekozen geneesmiddelen mogelijk deze achteruitgang zouden kunnen vertragen.
Verouderende cellen in een veeleisende omgeving
Het binnenoppervlak van de darm is een van de weefsels met de snelste vernieuwing in het lichaam. Stamcellen, genesteld aan de basis van kleine zakjes die crypten worden genoemd, delen zich om miljarden cellen elke paar dagen te vervangen. Dit constante werk vereist een stabiele energievoorziening, veelal afkomstig van de afbraak van vetten. Tegelijk worden deze stamcellen gereguleerd door een "epigenetische" code—chemische markeringen op histoneiwitten die helpen bepalen welke genen actief of stil zijn. De auteurs richtten zich op één van die markeringen, bekend als H3K36-trimethylatie, aangebracht door een enzym dat SETD2 heet, en vroegen zich af of veranderingen in deze markering zouden kunnen verklaren waarom intestinale stamcellen hun kracht verliezen met de leeftijd.
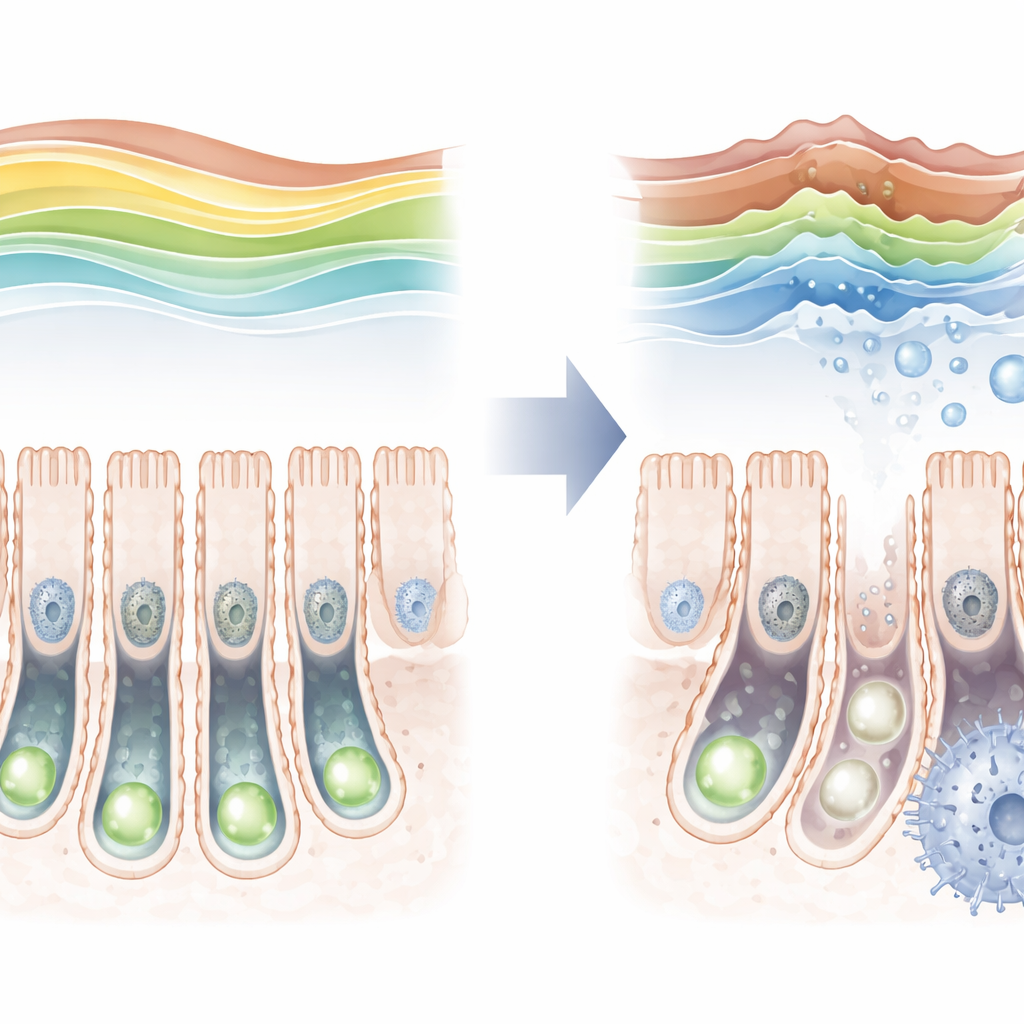
Een beschermend merkteken dat vervaagt met de leeftijd
Door de darmen van muizen over de levensduur heen te onderzoeken, vonden de onderzoekers dat de H3K36-trimethylmarkering niet statisch is. Ze is relatief laag kort na de geboorte, stijgt dan naar een piek bij jonge volwassenen en daalt weer op latere leeftijd. Naarmate deze markering afnam bij oudere dieren, namen markers van cellulair verouderen toe in stamcellen, wat wijst op een verband tussen beide. Om dit directer te testen, creëerde het team muizen waarbij SETD2 alleen in intestinale stamcellen kon worden verwijderd. Wanneer dit enzym werd uitgezet, verdween het beschermende merkteken bijna volledig, deelden stamcellen zich minder vaak en hadden ze moeite om het volledige spectrum gespecialiseerde darmscellen te produceren.
Hoe epigenetische veranderingen de vetverbranding ontsporen
Het verlies van dit enkele histonmerkteken zette een keten van veranderingen in gang binnen stamcellen. Metingen van genactiviteit toonden aan dat veel genen die betrokken zijn bij de celcyclus en DNA-replicatie werden afgeremd, terwijl genen verbonden met stress en veroudering werden opgeregeld. Opvallend was dat het sterkste signaal wees op verstoorde vetafhandeling: genen die normaal vetzuuroxidatie ondersteunen—de gecontroleerde verbranding van vetten voor energie—waren onderdrukt, en vetten begonnen zich op te hopen in de crypten. Metabolietprofilering bevestigde dat lange-keten vetzuren zich ophoopten, een teken dat de gebruikelijke vetverwerkingsroutes haperen. Tegelijkertijd verschuift de fysieke verpakking van DNA in de kern, waarbij veel gebieden meer bloot komen te liggen of juist strakker gesloten raken, waardoor verandert welke genen de cel gemakkelijk kan gebruiken.
Chromatine-remodellers en de mars richting senescentie
Om te begrijpen hoe deze veranderingen in DNA-verpakking ontstaan, brachten de auteurs zowel open chromatinegebieden als een reeks andere histonmarkeringen in kaart over het genoom. Toen H3K36-trimethylatie verloren ging, kregen grote stukken DNA "actieve" markeringen en werden ze beter toegankelijk, vooral nabij genen die verbonden zijn met stofwisseling en veroudering. Een sleutelfiguur in deze overgang was het SWI/SNF-chromatine-remodelingcomplex, aangedreven door een kernsubunit genaamd SMARCA4. In stamcellen zonder SETD2 steeg het SMARCA4-niveau, en het complex leek te helpen regio’s open te wrikken die senescentieprogramma’s aansturen. Wanneer de onderzoekers SMARCA4-activiteit genetisch of met een gerichte remmer verminderden, herwonnen stamcellen een deel van hun vermogen om gezonde mini-darmen in een schaaltje te vormen, en namen verouderingsmarkers af—wat suggereert dat overmatige remodeling deze cellen richting een vermoeide, senescente toestand duwt.
Het heractiveren van energiepaden om stamcellen te redden
Aangezien verstoorde vetverbranding als een centraal probleem naar voren kwam, testte het team of het versterken van deze route de veroudering van stamcellen kon tegengaan. Ze gebruikten een middel dat PPARα activeert, een hoofdregelaar van vetzuuroxidatie. In organoïden gekweekt uit SETD2-deficiënte stamcellen zorgde deze behandeling voor meer groei, herstelde de uitgroeistructuren die kenmerkend zijn voor vitale stamcellen, en verminderde vetophoping. In levende muizen vulde dezelfde interventie gedeeltelijk de stamcelvoorraad aan, verlaagde markers van senescentie en normaliseerde de lipidenophoping in de intestinale crypten. Deze bevindingen plaatsen vetzuuroxidatie als een cruciale schakel tussen epigenetische controle en stamcelgezondheid.
Wat dit betekent voor gezond ouder worden
Samengevat toont het werk aan dat een specifiek histonmerkteken, aangebracht door SETD2, helpt een gebalanceerd epigenetisch landschap in intestinale stamcellen te behouden. Wanneer dit merkteken vervaagt, wordt chromatine abnormaal geremodelleerd, hapert de vetverbranding, hopen lipiden zich op en glijden cellen in senescentie, waardoor het herstelvermogen van de darm verzwakt. Door óf de overactieve remodeling-machinerie te remmen óf de vetstofwisseling te herstellen met gerichte geneesmiddelen, kan het mogelijk zijn stamcelfunctie en darmgezondheid op latere leeftijd te behouden. Hoewel deze bevindingen afkomstig zijn uit muizen, echoën ze patronen die worden gezien bij menselijk darmaandoeningen, wat het vooruitzicht opent dat zorgvuldig afgestelde metabolische therapieën ooit kunnen helpen de leeftijdsgebonden achteruitgang van onze eigen intestinale stamcellen tegen te gaan.
Bronvermelding: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
Trefwoorden: intestinale stamcellen, epigenetica, vetzuuroxidatie, cellulaire senescentie, SETD2