Clear Sky Science · nl
Shp1-fosfatase reguleert CXCR2-eiwitstabiliteit en IL8-gemedieerde invasiviteit bij borstkanker
Waarom dit onderzoek belangrijk is voor borstkanker
Borstkanker blijft een van de belangrijkste oorzaken van overlijden door kanker bij vrouwen, grotendeels omdat sommige tumoren invasief worden en uitzaaien naar andere organen. Deze studie licht toe hoe een veelvoorkomend ontstekingssignaal in tumoren, IL8 genoemd, communiceert met borstkankercellen en hoe een moleculaire "rem" genaamd Shp1 meebepaalt of die cellen op hun plaats blijven of agressiever worden. Inzicht in dit moleculaire touwtrekken kan nieuwe mogelijkheden openen om de verspreiding van moeilijk te behandelen borstkankers, vooral triple-negatieve ziekte, te vertragen of te stoppen.
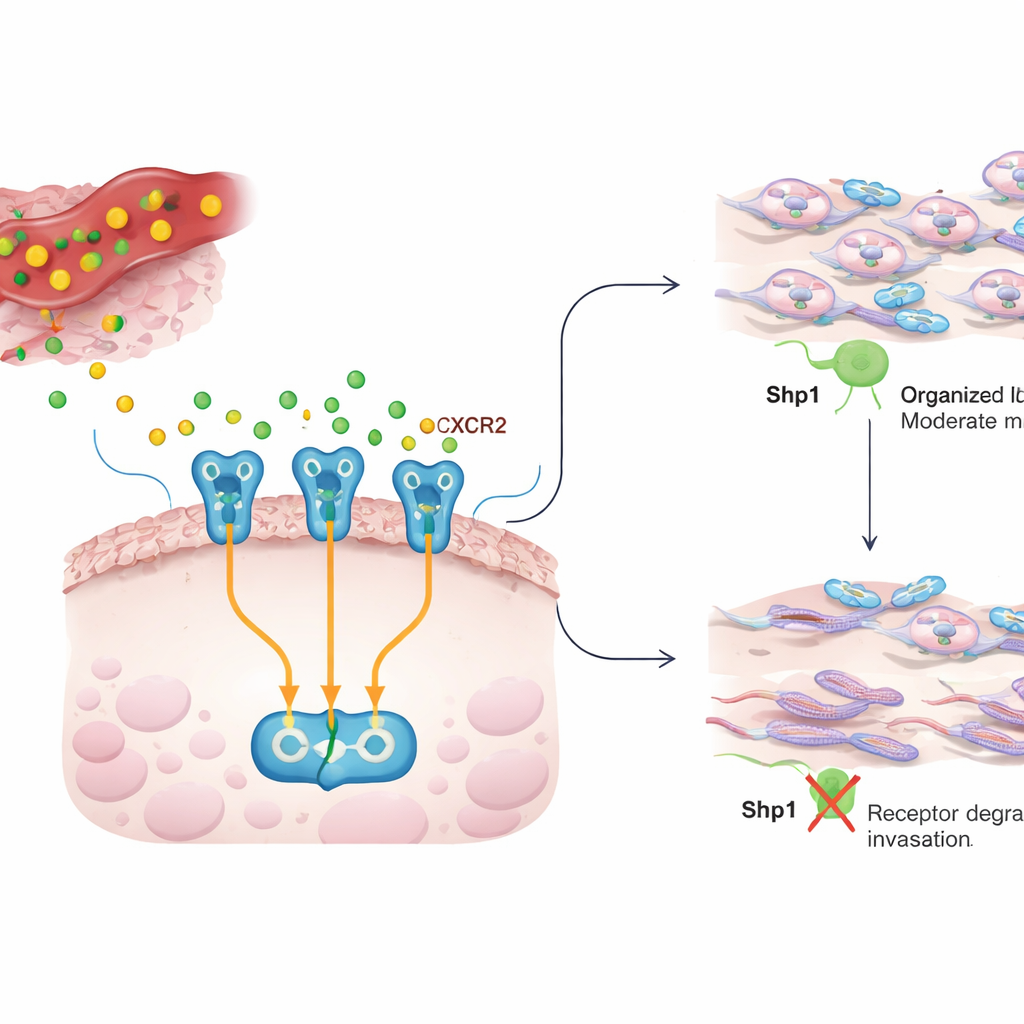
Een gesprek tussen ontsteking en kankercellen
In een tumor zijn kankercellen omgeven door immuun- en ondersteunende cellen die chemische boodschappers, cytokines, afgeven. IL8 is een van die boodschappers en komt vaak in hoge concentraties voor in veel kankers, waar het groei, vaatvorming en het vermogen van kankercellen om te bewegen en te infiltreren stimuleert. IL8 signaleert via een receptor aan het celoppervlak, CXCR2. Wanneer IL8 zich bindt aan CXCR2, schakelt het verschillende interne circuits in die het celskelet herschikken, waardoor cellen door weefsels kunnen kruipen en zich kunnen verspreiden. Het huidige werk onderzoekt hoe dit IL8–CXCR2-gesprek onder controle wordt gehouden en of Shp1, een enzym dat gewoonlijk wordt gezien als een tumoronderdrukkende rem op groeisignalen, ook dit invasieve gedrag beïnvloedt.
De verborgen rol van Shp1 in celbeweging
De onderzoekers verwijderden of blokkeerden Shp1 chemisch in een veelgebruikte luminale borstkankercellijn (MCF7) en maten hoe goed de cellen konden migreren en door een gel die weefsel nabootst konden invaseren. Zonder Shp1 sloten kankercellen wonden sneller en duwden ze zich twee- tot driemaal efficiënter door de gel, wat aangeeft dat Shp1 beweging normaal gesproken remt. Met behulp van patiëntgegevens vonden ze ook dat vrouwen van wie de tumoren minder Shp1 uitdrukten een slechtere overleving en kortere tijd tot terugkeer hadden. Gezamenlijk suggereren deze resultaten dat Shp1 het agressieve gedrag van borstkankercellen beperkt en dat het verliezen van deze rem samenhangt met slechtere uitkomsten.
Hoe IL8 Shp1 uitschakelt en een sleutelreceptor herprogrammeert
Vervolgens onderzocht het team hoe IL8 Shp1 zelf beïnvloedt. Ze ontdekten dat IL8 een eiwit activeert dat PKC heet en dat Shp1 op een specifieke plaats markeert, waardoor de enzymatische activiteit met ongeveer 60 procent afneemt. Wanneer Shp1 op deze manier wordt geremd, wordt een ander enzym, PP2A, minder actief en blijft de CXCR2-receptor in een sterk gemodificeerde toestand die haar lot binnen de cel verandert. In plaats van te worden opgeschoond en teruggerecycled naar het celoppervlak, wordt CXCR2 gemarkeerd voor afbraak, voornamelijk via het eiwitafbrekende machinerie van de cel, het proteasoom. Een specifieke modificatie op CXCR2, bij een aminozuur genaamd Ser347, bleek cruciaal voor het vasthechten van deze degradatietags. In cellen zonder Shp1 werd CXCR2 zwaarder getagd en sneller afgebroken, wat leidde tot minder receptoren op het celoppervlak en een verzwakte respons op IL8 in de loop van de tijd.
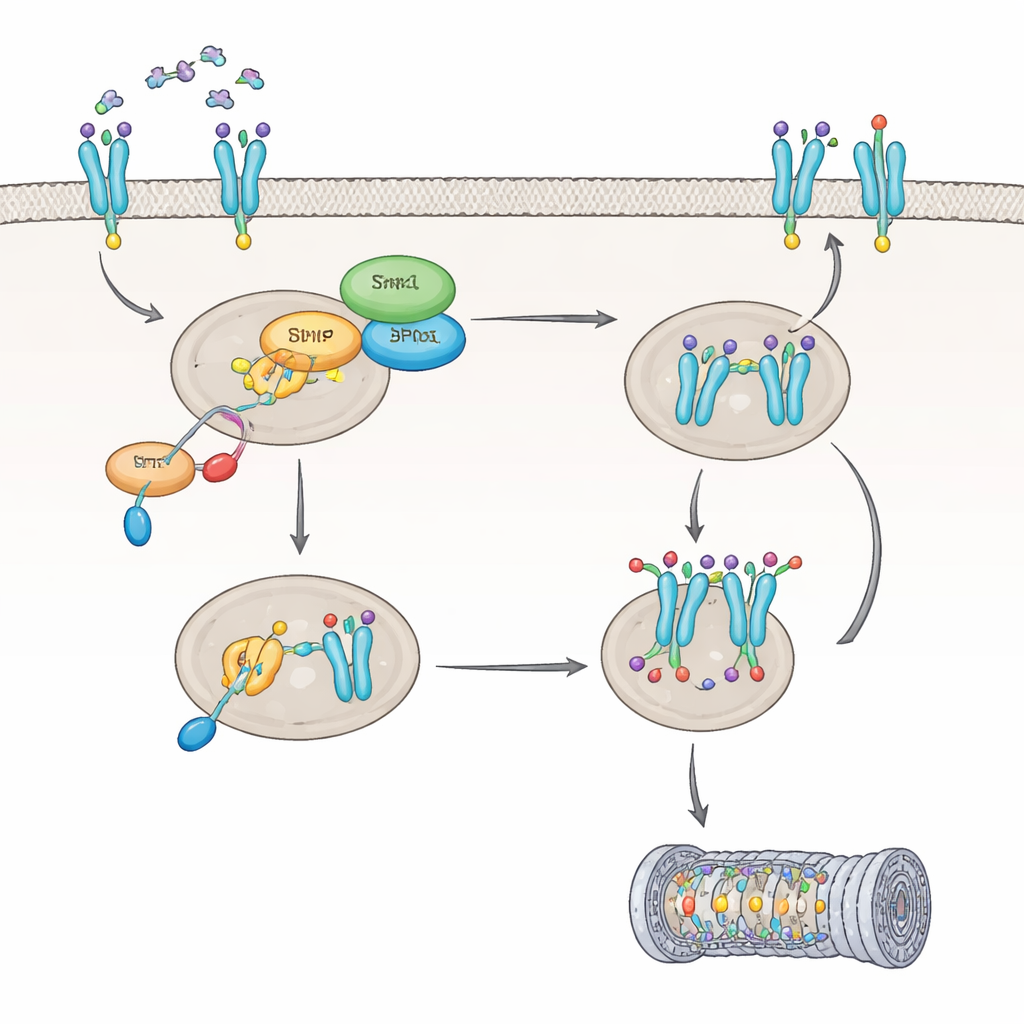
Verschillende borstkankertypes, verschillende bedrading
Borstkanker is geen eenduidige ziekte; tumoren worden ingedeeld in luminale, HER2-positieve en triple-negatieve subtypes op basis van hun receptorpatronen. De onderzoekers testten het IL8–CXCR2–Shp1-circuit in verschillende cellijnen die elk subtype vertegenwoordigen. In luminale en triple-negatieve cellen activeerde IL8 de Shp1–PP2A–CXCR2-cascade, en het blokkeren van Shp1 verhoogde zowel de basale invasiviteit als maakte het gebruikelijke pro-invasieve effect van IL8 ongedaan. Daarentegen reageerden HER2-positieve cellen nog steeds op IL8, maar veranderde het blokkeren van Shp1 hun gedrag nauwelijks, wat suggereert dat in deze tumoren Shp1 verstrikt is in andere signalen, zoals HER2, en minder beschikbaar is om CXCR2 te reguleren. Grootschalige genexpressie-analyses ondersteunden dit beeld: triple-negatieve lijnen hadden de neiging minder Shp1 te hebben, veranderde GPCR-gerelateerde signalering en hogere IL8, wat overeenkomt met een agressiever, ontsteking-gedreven profiel.
Wat dit betekent voor toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat het enzym Shp1 fungeert als verkeersregelaar voor de IL8-receptor CXCR2, en bepaalt of de receptor wordt hergebruikt of afgebroken en daarmee hoe sterk borstkankercellen op ontstekingssignalen kunnen reageren. In luminale en triple-negatieve borstkankers blijkt dit controlepunt bijzonder belangrijk: wanneer Shp1-niveaus laag zijn of zijn activiteit wordt geblokkeerd, worden cellen invasiever en verslechteren de patiëntuitkomsten. Omdat Shp1 kan worden versterkt of gemoduleerd door bepaalde bestaande geneesmiddelen, kan het richten op de Shp1–CXCR2-as, mogelijk in combinatie met IL8- of CXCR2-remmers, een nieuwe strategie bieden om invasie en metastase bij agressieve borstkankersubtypes te beperken.
Bronvermelding: Monti, M., Amendola, P.G., Filograna, A. et al. Shp1 phosphatase regulates CXCR2 protein stability and IL8-mediated invasiveness in breast cancer. Cell Death Dis 17, 297 (2026). https://doi.org/10.1038/s41419-026-08516-4
Trefwoorden: invasie bij borstkanker, IL8-signaal, CXCR2-receptor, Shp1-fosfatase, triple-negatieve borstkanker