Clear Sky Science · nl
CRMP2 remt de vorming van metastasen door ILF3‑afhankelijke stabilisatie van CXCL10‑mRNA in borstkanker te verstoren
Waarom het stoppen van kankerverschuiving belangrijk is
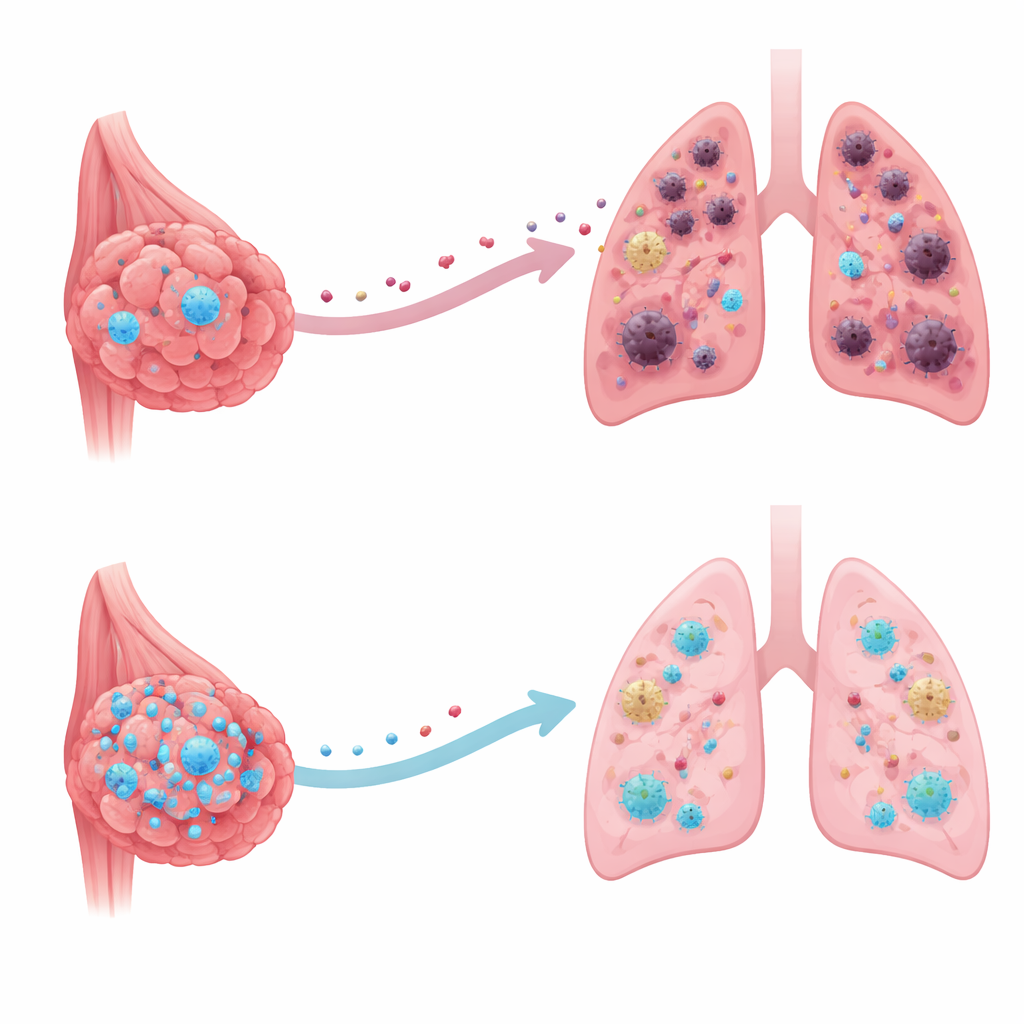
De meeste sterfgevallen door borstkanker komen niet door de oorspronkelijke tumor, maar doordat kankercellen naar vitale organen zoals de longen migreren en daar nieuwe gezwellen vormen. Deze studie onthult een ingebouwd beschermend eiwit in borstkankercellen dat deze verspreiding kan vertragen of zelfs blokkeren door de "welkomstmat" te veranderen die verre organen uitrollen voor rondzwervende kankercellen. Inzicht in deze verborgen veiligheidschakelaar kan de deur openen naar nieuwe behandelingen die voorkomen dat kanker elders in het lichaam wortel schiet.
Een stille verdediger in kankercellen
De onderzoekers richtten zich op een eiwit genaamd CRMP2, vooral bekend voor het helpen van zenuwcellen bij groei en het onderhouden van hun interne skelet. Bij onderzoek van grote openbare kankerdatabases en patiënttumormonsters vonden ze dat de CRMP2‑niveaus ongewoon laag waren in borstumoren, vooral in kankers die zich al hadden verspreid. Patiënten van wie de tumoren nog relatief veel CRMP2 bevatten, leefden gemiddeld langer en ontwikkelden minder vaak afstandsmetastasen. Dit patroon suggereert dat CRMP2 zich in borstkanker meer als een rem dan als een versneller gedraagt, en fungeert als een interne verdediger in plaats van een ziekteveroorzaker.
Hoe de longen worden voorbereid op invasie
Kankercellen arriveren zelden als een verrassing in een verre orgaan. Lang voordat ze daar zijn, scheidt de oorspronkelijke tumor moleculen uit die dat orgaan hervormen tot wat wetenschappers een "pre‑metastatische niche" noemen – een micro‑omgeving die gunstig is voor het overleven van kanker. Met behulp van een goed vastgesteld muismodel dat nauw lijkt op menselijke borstkanker, toonde het team aan dat wanneer borstumorcellen zo werden gemodificeerd dat ze extra CRMP2 produceren, de primaire tumoren even snel groeiden, maar de longen veel minder gastvrij werden. Merkers van ontsteking en weefsel‑hermodellering in de longen namen af, en minder van de immuuncellen die normaal de antitumorverdediging onderdrukken werden aangetrokken. Als gevolg daarvan vormden er na verwijdering van de hoofdtumor veel minder metastatische noduli in de longen.
Een signaleringsketen die problemen veroorzaakt
Dieper gravend vroegen de wetenschappers welke tumorsecreties verantwoordelijk waren voor het voorbereiden van de longen. Ze richtten zich op CXCL10, een kleine boodschapperprotein (chemokine) die bekendstaat om het aantrekken van bepaalde immuuncellen en het wekken van sluimerende kankercellen. In zowel in het laboratorium gekweekte menselijke als muisborstkankercellen verminderde het verhogen van CRMP2 sterk de hoeveelheid CXCL10 die werd geproduceerd en uitgescheiden. In muizen toonden longen die waren blootgesteld aan tumormateriaal met veel CRMP2 veel lagere CXCL10‑waarden en minder binnenkomende immuuncellen die normaal beschermende T‑celactiviteit dempen. Toen de onderzoekers CXCL10 blokkeerden met een antilichaam, nam longkolonisatie door kankercellen af; wanneer ze extra CXCL10 toevoegden, verdween het beschermende effect van CRMP2. Dit plaatste CXCL10 ondubbelzinnig stroomaf van CRMP2 als een belangrijke aanstichter van een metastase‑vriendelijke niche.
De verborgen tussenpersoon die schadelijke signalen stabiliseert
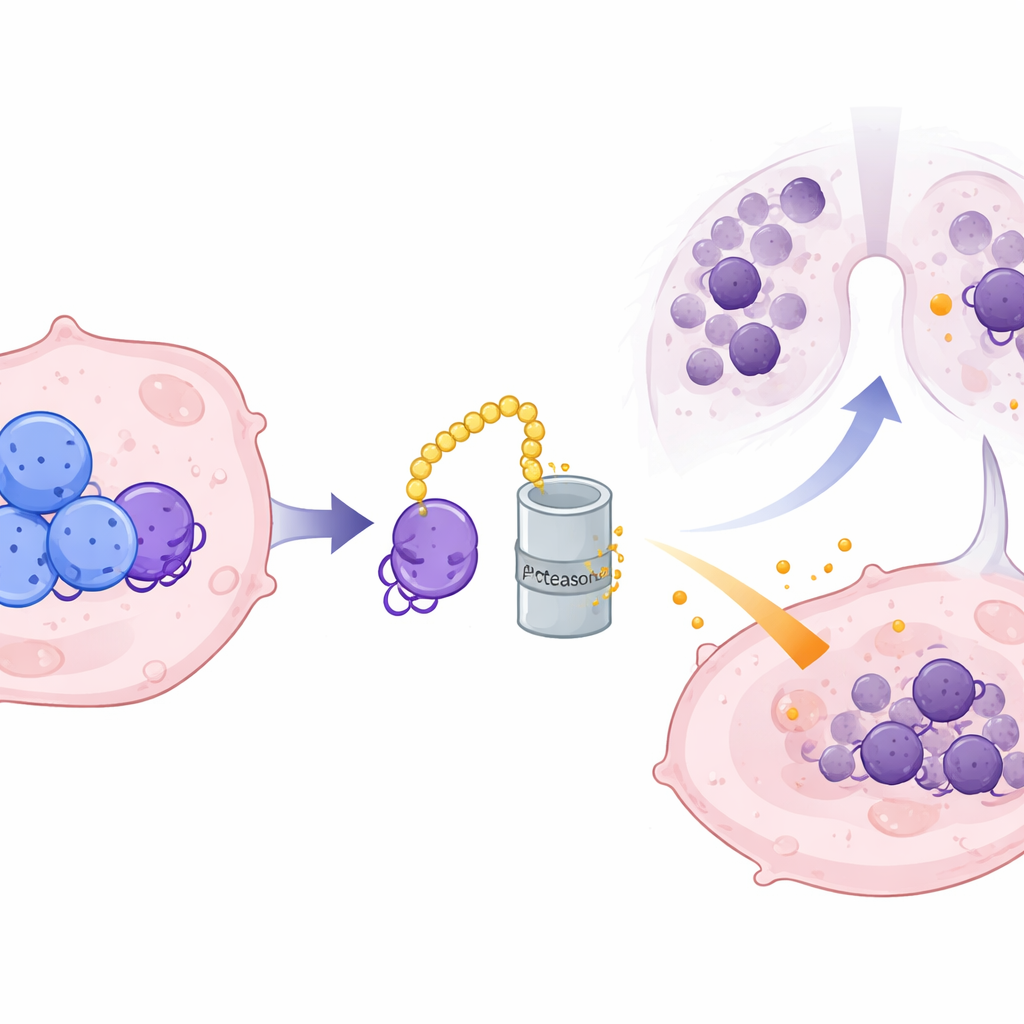
Aangezien CRMP2 binnenin cellen leeft terwijl CXCL10 wordt uitgescheiden, vermoedde het team een moleculaire tussenpersoon. Ze identificeerden ILF3, een RNA‑bindend eiwit, als een directe partner van CRMP2. ILF3 hecht zich aan het RNA‑blauwdruk van CXCL10 en beschermt het normaal tegen afbraak, waardoor meer CXCL10‑eiwit kan worden geproduceerd. CRMP2 bindt ILF3 op specifieke contactpunten en markeert het voor afbraak via het eiwit‑recyclingsysteem van de cel, waardoor de levensduur van ILF3 wordt verkort en zijn greep op CXCL10‑RNA wordt verbroken. Wanneer CRMP2‑niveaus hoog zijn, wordt ILF3 sneller afgebroken, wordt CXCL10‑RNA onstabieler en wordt er minder van het ontstekingschemokine uitgescheiden. Toen ILF3 kunstmatig werd hersteld, kon het de onderdrukking van CXCL10 door CRMP2 overrulen, waarmee zijn rol als cruciale schakel in deze keten werd bevestigd.
Een plantverbinding omvormen tot een potentiële bondgenoot
Om te onderzoeken of deze route therapeutisch benut kon worden, schermden de onderzoekers een bibliotheek van natuurlijke verbindingen en vonden dat psoraleen – een plantaardige molecule die al lange tijd in huidbehandelingen wordt gebruikt – direct aan CRMP2 bindt en het stabieler maakt. In celexperimenten verhoogde psoraleen CRMP2‑niveaus, verlaagde ILF3 en CXCL10, en verminderde het invasieve gedrag van borstkankercellen zonder hun algemene levensvatbaarheid te schaden. In meerdere muismodellen verkleinde psoraleen de primaire borstumoren niet, maar het verminderde sterk longmetastasen en remde de vorming van de pre‑metastatische niche, eveneens op een manier die afhankelijk was van CRMP2. Hoewel psoraleen zelf levertoxische effecten kan hebben en verfijning behoeft, tonen deze resultaten aan dat kleine moleculen de beschermende rol van CRMP2 kunnen versterken.
Wat dit betekent voor patiënten
Samengevat onthult dit werk een beschermende as in borstkankercellen waarbij CRMP2 ILF3 destabiliseert, wat op zijn beurt CXCL10 verlaagt en voorkomt dat de longen vruchtbare grond voor metastasen worden. In plaats van kankercellen direct aan te vallen, richt deze strategie zich op het ontwapenen van de verre niches waarop ze vertrouwen, en kantelt daarmee de balans in het voordeel van de eigen afweer van het lichaam. Hoewel er nog veel moet gebeuren voordat een dergelijke benadering de kliniek bereikt, biedt het richten op de CRMP2–ILF3–CXCL10‑route – mogelijk met veiligere psoraleen‑achtige middelen – een veelbelovende nieuwe invalshoek om te voorkomen dat borstkanker zich verspreidt.
Bronvermelding: Lin, B., Luo, M., Zhou, Y. et al. CRMP2 inhibits metastasis formation by impairing ILF3-dependent stabilization of CXCL10 mRNA in breast cancer. Cell Death Dis 17, 255 (2026). https://doi.org/10.1038/s41419-026-08515-5
Trefwoorden: borstkankermetastasen, pre‑metastatisch niche, chemokinesignaalgeving, RNA‑bindende eiwitten, natuurlijke producttherapieën