Clear Sky Science · nl
Onderzoek naar de wisselwerking tussen kanker-geassocieerde fibroblasten en tumorcellen met co-cultuur-organoïden
Waarom de tumorbuurt ertoe doet
Kanker is meer dan een massa ontspoorde cellen; het groeit binnen een dynamische omgeving van ondersteunende cellen, steunweefsels, bloedvaten en immuunverdedigers. Onder deze buren vormen een groep die bekendstaat als kanker-geassocieerde fibroblasten, of CAFs, stilletjes de manier waarop tumoren ontstaan, zich verspreiden en reageren op behandeling. Dit overzichtsartikel legt uit hoe wetenschappers kleine driedimensionale mini-tumoren, organoïden genoemd, samen met CAFs kweken om dit verborgen gesprek bloot te leggen en slimmere, preciezere therapieën te ontwerpen.
Kleine tumoren in een schaaltje
Traditioneel kankeronderzoek steunde vaak op platte celmonolagen in plastic schaaltjes of op diermodellen, die beide slechts een deel van de werkelijke ziekte vangen. Organoïden veranderen dat beeld. Het zijn driedimensionale clusters van patiënt-afgeleide tumorcellen die veel van de structuur, genetische samenstelling en het gedrag van de oorspronkelijke tumor behouden. Wanneer deze organoïden samen met CAFs worden gekweekt, beginnen ze echte solide tumoren na te bootsen, ook in hoe ze op chemotherapie en bestraling reageren. Verschillende kweekopzetten zijn ontwikkeld: eenvoudige gelgebaseerde systemen waarin tumorcellen en CAFs dezelfde matrix delen, gemengde "hanging drop"-methoden die eerst compacte sferoïden vormen, en geavanceerde microfluïdische chips die vloeistofstromen en organoïde-grootte beheersen voor grootschalige medicijntests. Elke benadering balanceert realisme, kosten en technische complexiteit.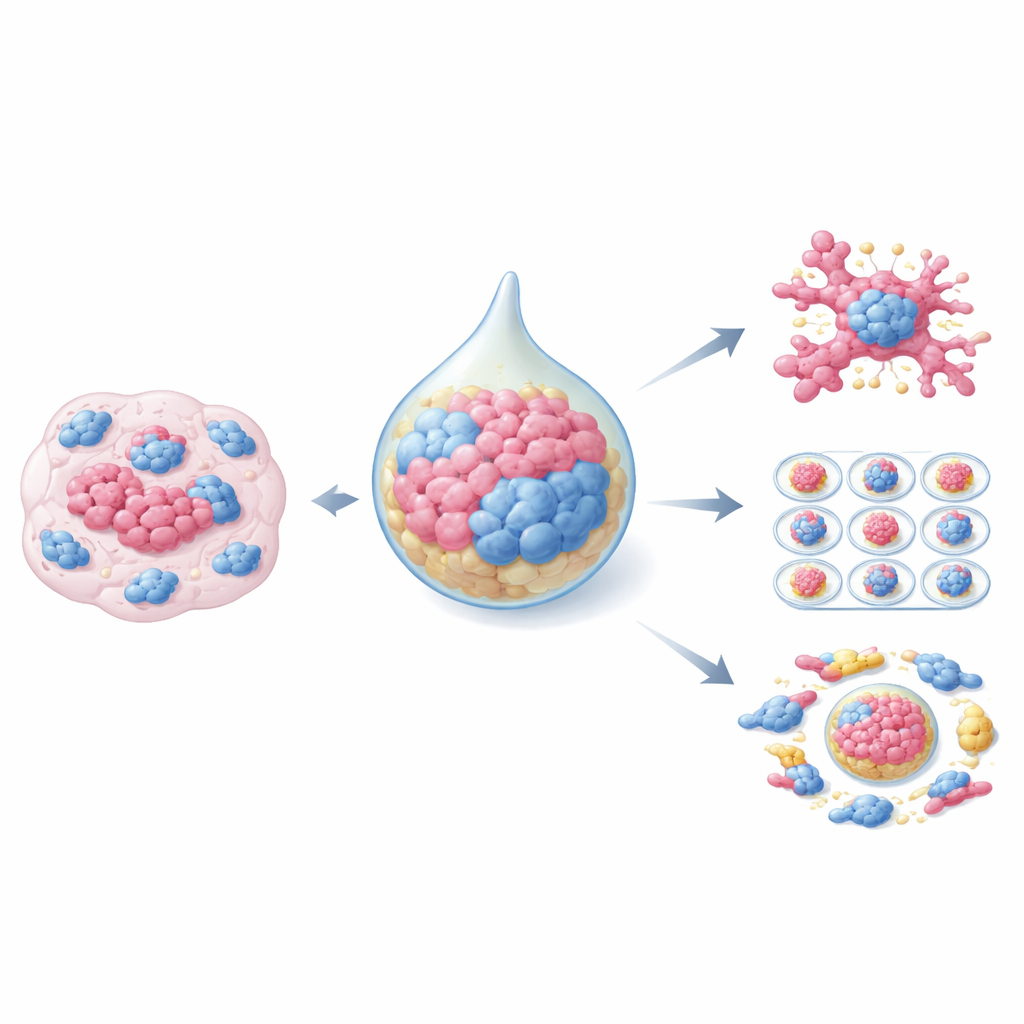
Hoe ondersteunende cellen tumoren laten gedijen
CAFs vormen geen uniforme celtype; ze komen in vele varianten, elk met een eigen taak. In co-cultuur-organoïden helpen CAFs het vezelige raamwerk rond kankercellen op te bouwen en te vernieuwen, waardoor stijfheid en structuur veranderen op manieren die tumorgroei en invasie bevorderen. Ze scheiden een cocktail van signalen uit die kankercellen aanzetten tot vermenigvuldiging, migratie en invasie van nabijgelegen weefsels, en ze kunnen gewone cellen zelfs aansporen stamcelachtige eigenschappen te verwerven die nieuwe tumoren zaaien. CAFs herschikken ook hoe kankercellen energie produceren en gebruiken, door voedingsstoffen heen en weer te ruilen om beide partners onder stress te laten overleven. In veel modellen maken CAFs tumoren resistenter tegen chemotherapie en gerichte geneesmiddelen, bijvoorbeeld door kankercellen te beschermen binnen dichte collageenlagen, survivalroutes te activeren of kleine blaasjes boordevol RNA te sturen die DNA-reparatie versterken.
Immuunontsnapping en bloedtoevoer
Buiten het voeden en huisvesten van kankercellen beïnvloeden CAFs sterk de afweer van het lichaam. Co-cultuur-organoïden en organoïde-op-chip-systemen tonen aan dat CAFs moordende immuuncellen kunnen afstoten, onderdrukkende immuunpartners kunnen aantrekken en immuuncellen in een staat kunnen drijven waarin ze niet langer kunnen aanvallen. Sommige CAF-subsets overladen natural killer-cellen met ijzer en drijven ze in een vorm van celdood, terwijl anderen tumorondersteunende macrofagen binnenroepen. Tegelijkertijd stimuleren CAFs de groei van nieuwe bloedvaten door factoren af te scheiden die vatvormende cellen aanzetten tot uitgroei en kanaalvorming, zodat tumoren een gestage toevoer van zuurstof en voedingsstoffen krijgen. Het verhaal is echter niet geheel eenzijdig: bepaalde zeldzame CAF-typen kunnen juist de anti-tumorimmuniteit ondersteunen door T-cellen te helpen activeren of andere immuuncellen te herprogrammeren naar een behulpzamere staat.
Een tweerichtingsgesprek met tumorcellen
De relatie tussen CAFs en kankercellen is een feedbacklus. Tumorcellen sturen signalen uit die nabijgelegen normale fibroblasten omzetten in CAFs en deze vervolgens in verschillende subgroepen vormen, zoals contractiele, matrix-producerende cellen of ontstekingsgedreven cellen die veel cytokinen uitscheiden. Via oplosbare factoren en kleine blaasjes kunnen kankercellen CAFs in richtingen duwen die het weefsel verstevigen, invasie bevorderen en medicijnresistentie aandrijven. Co-cultuur-organoïden hebben laten zien hoe specifieke signaalroutes fungeren als knoppen die CAF-identiteit verschuiven, waardoor tumoren zich kunnen aanpassen aan veranderende omstandigheden of behandelingen. Het begrijpen van dit heen-en-weer is cruciaal, want grove benaderingen die simpelweg alle CAFs proberen te elimineren hebben in sommige dierstudies en klinische proeven onverwacht de tumorprogressie versneld.
Nieuwe manieren om de tumorbuurt aan te pakken
Gewapend met organoïde-modellen die CAF–tumor crosstalk behouden, onderzoeken onderzoekers verfijndere behandelingsstrategieën. In plaats van alle fibroblasten uit te roeien, richten sommige aanpakken zich op het blokkeren van schadelijke signalen tussen CAFs en kankercellen, het ontregelen van hun gedeelde metabolisme, of het zachtjes "heropvoeden" van CAFs naar meer goedaardige of zelfs tumorremmende staten. Experimentele tactieken omvatten kleine moleculen die CAF-signaleringsroutes wijzigen, geneesmiddelen die de vezelige schaal van de tumor verzachten of dunner maken, en geavanceerde celtherapieën zoals geconstrueerde immuuncellen die ontworpen zijn om specifieke CAF-subsets te herkennen en aan te vallen. Organoïde-gebaseerde platforms maken het mogelijk deze ideeën op patiënt-afgeleid weefsel in het laboratorium te testen, wat een weg biedt naar gepersonaliseerde combinaties die zowel kankercellen als hun ondersteunende omgeving aanpakken.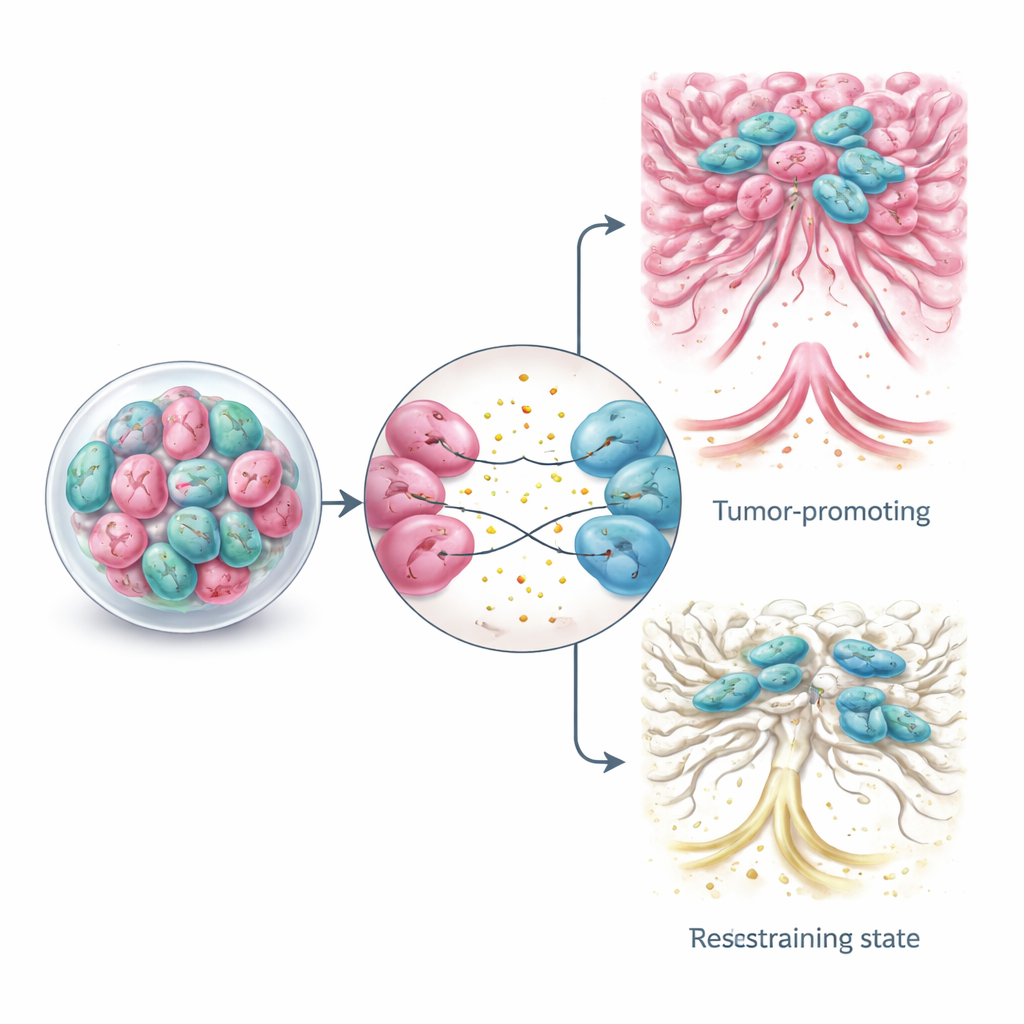
Wat dit betekent voor toekomstige kankerzorg
Dit overzicht concludeert dat CAFs zowel krachtige bondgenoten als soms stille tegenstanders van kanker zijn. Hun diversiteit en flexibiliteit verklaren waarom eenvoudige "CAF-uitschakeling"-behandelingen vaak hebben gefaald en soms schade veroorzaakten. Door co-cultuur-organoïden als realistische testbanken te gebruiken, kunnen wetenschappers nu goed en kwaad in CAF-gedrag scheiden, de signalen in kaart brengen die hen met tumorcellen verbinden, en therapieën ontwerpen die selectief tumorbevorderende rollen blokkeren terwijl beschermende functies behouden of versterkt worden. Voor patiënten legt dit werk de basis voor nauwkeuriger medicijntests en combinatietherapieën die niet alleen de tumor aanvallen, maar ook de buurt hervormen die haar doet gedijen.
Bronvermelding: Wang, M., Ding, X., Chen, L. et al. The research advances of crosstalk between cancer-associated fibroblasts and tumor cells using co-culture organoids. Cell Death Dis 17, 267 (2026). https://doi.org/10.1038/s41419-026-08512-8
Trefwoorden: kanker-geassocieerde fibroblasten, tumororganoïden, tumormicro-omgeving, therapieresistentie, 3D co-cultuurmodellen