Clear Sky Science · nl
CCL11 bevordert recidief van hepatocellulair carcinoom na operatie door immunosuppressieve CCR5 + CD206 + M2‑achtige macrofagen te versterken en tumorinvasiviteit te bevorderen
Waarom leverkanker na een operatie kan terugkeren
Leveroperatie is vaak de beste kans voor mensen met vroeg stadium leverkanker, maar veel patiënten zien hun kanker binnen enkele jaren terugkomen. Deze studie stelt een simpele maar cruciale vraag: helpt de eigen ontstekingsreactie van het lichaam op de operatie per ongeluk achtergebleven kankercellen te groeien en uit te zaaien? De onderzoekers richten zich op een signaalmolecuul genaamd CCL11 en laten zien hoe een piek van dit molecuul na de operatie zowel de antikankerimmuniteit kan verzwakken als overlevende tumorcellen agressiever kan maken.
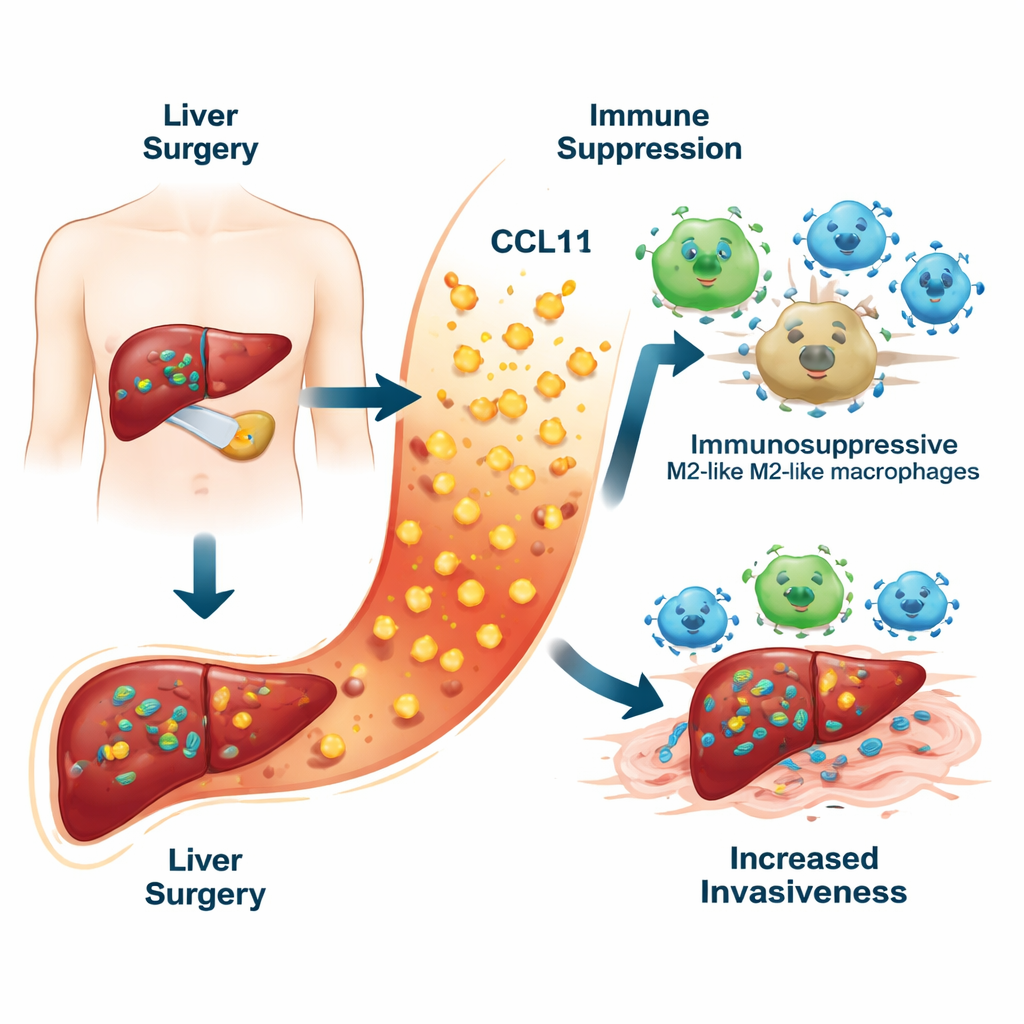
Een verborgen gevaar in de genezingsreactie
Wanneer chirurgen een levertumor verwijderen, moeten ze bloedvaten afklemmen en het omringende weefsel beschadigen. Deze schade veroorzaakt een golf van ontsteking die de lever helpt genezen. Door tien verschillende ontstekingsmoleculen in het bloed van patiënten één week na de operatie te meten, vond het team dat één chemokine, CCL11, er uitsprong. Patiënten bij wie de leverkanker later terugkeerde, hadden significant hogere CCL11‑waarden dan degenen die kankervrij bleven. Hoge CCL11‑waarden correleerden ook met slechtere overleving. Toen de onderzoekers CCL11 combineerden met routinematige klinische gegevens zoals bloedtests en tumoreigenschappen, bouwden ze een risicokaart die het vijfjaarrecidief nauwkeuriger voorspelde dan traditionele modellen.
Het leverweefsel dat er normaal uitziet doet er nog steeds toe
De meeste aandacht in kankeronderzoek gaat uit naar de tumor zelf, maar deze studie toont aan dat het omringende “normale” leverweefsel net zo belangrijk kan zijn. In monsters van meer dan 100 patiënten was CCL11 zelfs hoger in niet‑tumoraal leverweefsel dan in de kankeknobbels of in gezonde donorlevers. Patiënten waarvan het nabijgelegen leverweefsel meer CCL11 produceerde, hadden meer kans op gevorderde ziekte, verspreiding op afstand en terugval na operatie. In muismodellen die het korte verlies en herstel van bloedstroom tijdens een operatie nabootsen, dreef leverletsel CCL11‑waarden snel omhoog. Onder laagzuurstofcondities in het laboratorium produceerden leverondersteunende cellen zoals myofibroblasten en endotheelcellen van bloedvaten ook meer CCL11, wat suggereert dat chirurgische stress het hele leverresteel voorbereidt om een pro‑kankeromgeving te worden.
Hoe CCL11 immuunverdedigers tot omstanders maakt
Om te zien hoe CCL11 het immuunsysteem vormt, keken de auteurs naar macrofagen, veelzijdige witte bloedcellen die tumoren kunnen aanvallen of beschermen. Ze vonden dat in niet‑tumoraal leverweefsel hogere CCL11 samenhing met meer van een macrofagetype dat de marker CCR5 draagt en een zogenaamde M2‑achtige, tumorvriendelijke profiel vertoont. Bij patiënten correleerden levers rijk aan deze CCR5+ M2‑achtige macrofagen met slechtere overleving. In kweek stimuleerde toevoeging van CCL11 monocyten om dit immunosuppressieve macrofaagtype te worden, met verhoogde expressie van moleculen zoals PD‑L1 en IL‑10 en het vrijkomen van andere signalen die meer immuuncellen aantrekken en vervormen. Deze door CCL11 geconditioneerde macrofagen stimuleerden vervolgens naïeve helper‑T‑cellen om te differentiëren naar regulerende T‑cellen, een populatie die bekendstaat om het dempen van antitumorreacties. Mechanistische experimenten toonden aan dat CCL11 een keten van signalen in macrofagen activeert die eindigt in het NF‑κB‑pad en de productie van PD‑L1, waardoor kankercellen beter beschermd worden tegen immuunaanval.
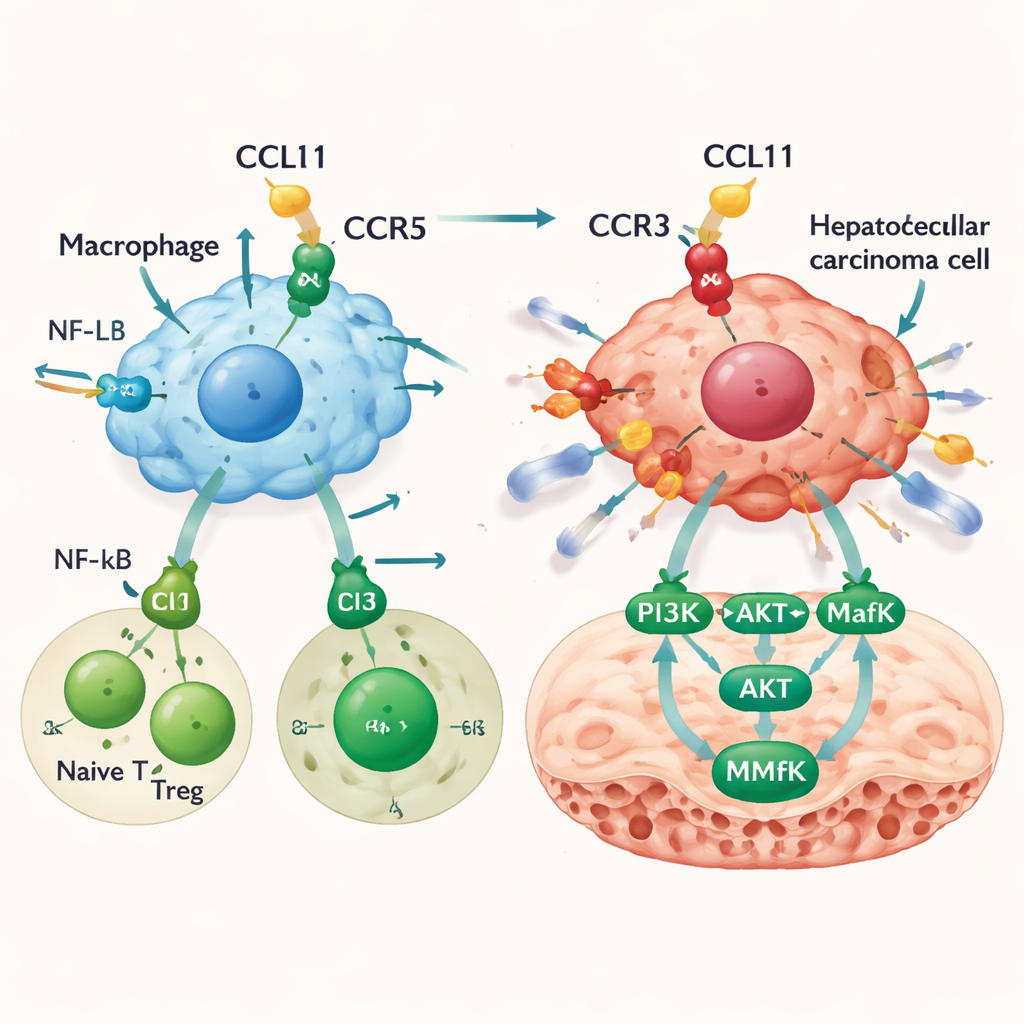
Hoe CCL11 overgebleven kankercellen invasiever maakt
CCL11 verandert niet alleen het immuunaanzicht; het werkt ook direct op leverkankercellen. Hoewel de kankercellen zelf weinig CCL11 produceren, dragen ze een van de receptoren ervan, CCR3. In laboratoriumtesten versnelde CCL11 de groei van leverkankercellen niet, maar maakte ze wel beweeglijker en invasiever door barrières heen te dringen — een kenmerk van metastatisch potentieel. Blokkeren van de CCR3‑receptor veegde dit effect grotendeels weg. Genanalyse wees op een pad waarbij CCL11–CCR3‑signaal PI3K en AKT activeert, wat vervolgens een transcriptiefactor genaamd MafK inschakelt. MafK verhoogt op zijn beurt de productie van MMP13, een enzym dat het omringende weefsel afbreekt en paden voor tumorverspreiding opent. In muismodellen verhoogde het inspuiten van CCL11 in de lever de tumormassa en leidde tot meer metastasen, samen met hogere activiteitsniveaus van het PI3K–AKT–MafK–MMP13‑pad binnen tumoren.
Van een risicosignaal naar een behandelbare kans
Omdat CCL11 zowel de immuunverdediging lijkt te onderdrukken als resterende kankercellen versterkt, testten de onderzoekers of het blokkeren ervan na de operatie de uitkomst kon veranderen. Bij muizen met levertumoren die chirurgisch werden verwijderd, reduceerde behandeling met een antilichaam dat CCL11 neutraliseert het recidiefpercentage in de lever dramatisch en verbeterde de overleving, zonder duidelijke bijwerkingen zoals gewichtsverlies. Al met al presenteren de bevindingen CCL11 als een schakelpunt dat chirurgisch letsel koppelt aan een immunosuppressieve, invasievriendelijke leveromgeving. Voor patiënten suggereert dit werk dat het meten van CCL11 na een operatie kan helpen de hoogste risico‑patiënten te identificeren, en dat geneesmiddelen die de CCL11–CCR5/CCR3‑as targeten mogelijk ooit deel kunnen worden van strategieën om te voorkomen dat leverkanker terugkeert.
Bronvermelding: Wang, J., Yeung, O.WH., Qiu, W. et al. CCL11 promotes hepatocellular carcinoma recurrence after surgery by potentiating immunosuppressive CCR5 + CD206 + M2-like macrophages and promoting tumor invasiveness. Cell Death Dis 17, 236 (2026). https://doi.org/10.1038/s41419-026-08508-4
Trefwoorden: terugkeer van leverkanker, CCL11 chemokine, tumormicro-omgeving, immuunsuppressie, kankermetastase