Clear Sky Science · nl
Fibroblasten geassocieerd met kanker bevorderen osimertinib‑resistentie in niet‑kleincellige longkankercellen via METTL1‑gemedieerde NET1 m7G‑modificatie
Waarom sommige longkankers stoppen met reageren op een “slim” middel
Gerichte middelen zoals osimertinib hebben de behandeling van veel mensen met een veelvoorkomend type longkanker veranderd en bieden vaak meer levensduur met minder bijwerkingen dan klassieke chemotherapie. Toch zijn deze voordelen voor de meeste patiënten tijdelijk: tumoren vinden uiteindelijk manieren om het middel te omzeilen. Deze studie stelt een schijnbaar eenvoudige maar belangrijke vraag: helpt het ondersteunende weefsel van de tumor — specifiek cellen die cancer‑associated fibroblasts worden genoemd — stiekem de kankercellen ontsnappen aan de werking van osimertinib?
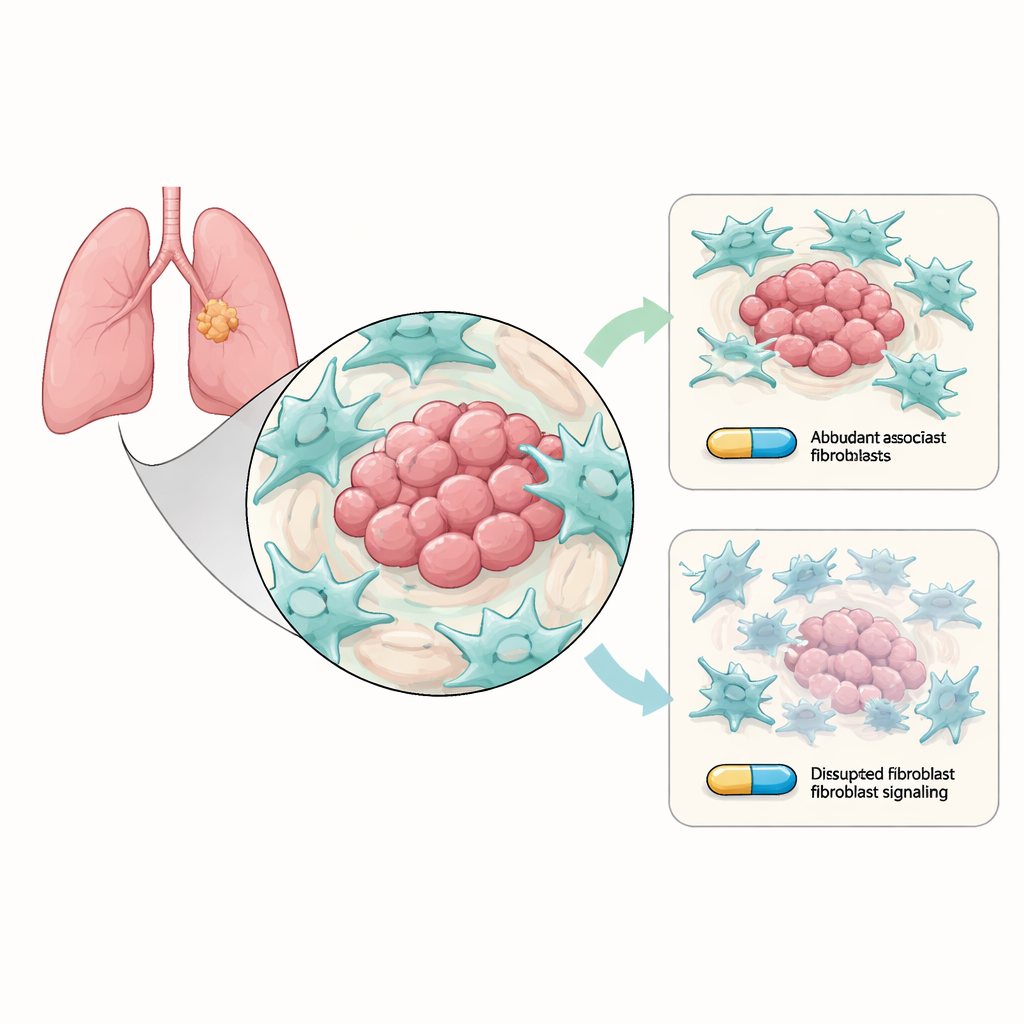
Hulpcellen die de tumor heimelijk afschermen
Niet‑kleincellige longkanker groeit binnen een drukke buurt van niet‑kankercellen, het zogeheten tumor micro‑milieu. Een van de meest talrijke bewoners zijn de cancer‑associated fibroblasts (CAFs), bindweefselcellen die de omgeving rond de tumor herschikken. De onderzoekers lieten longkankercellen met de gebruikelijke osimertinib‑gevoelige EGFR‑mutaties samen met CAFs in het lab groeien. Ze vonden dat wanneer CAFs aanwezig waren, de kankercellen moeilijker met osimertinib te doden waren: ze vormden meer kolonies, gingen minder vaak in apoptose en vertoonden sterkere “stam‑achtige” eigenschappen die samenhangen met langdurig overleven en terugkeer. Met andere woorden: hoewel het middel nog wel op de kankercellen gericht was, hielpen de omringende fibroblasten ze stilletjes om te volharden.
Een chemisch merkteken op RNA dat de spelregels verandert
Het team keek vervolgens voorbij de genen zelf naar de chemische merktekens die RNA sieren — de werkende kopieën van genetische informatie in cellen. Eén zo’n merkteken, m7G genoemd, kan beïnvloeden hoe stabiel een RNA‑molecuul is en hoe efficiënt het wordt vertaald in eiwit. Met biochemische tests en genoom‑brede mapping toonden de onderzoekers aan dat CAFs de algemene m7G‑markering op RNA’s binnen longkankercellen verhogen. Deze toename werd vooral aangedreven door een methyltransferase‑enzym genaamd METTL1, dat m7G‑merken op boodschapper‑RNA’s aanbrengt. METTL1‑niveaus waren hoger in longtumoren dan in nabijgelegen normaal weefsel en correleerden met verder gevorderde ziekte en slechtere overleving van patiënten, wat suggereert dat dit enzym meer doet dan alleen routinematige celprocessen bijsturen.
Een uitgescheiden signaal en een kwetsbare moleculaire keten
Hoe zetten CAFs METTL1 in kankercellen hoger? De studie wijst op een eiwit genaamd HMGB1 dat CAFs in hun omgeving uitscheiden. In vergelijking met kankercellen scheidden CAFs veel grotere hoeveelheden HMGB1 uit. Wanneer de onderzoekers HMGB1 aan longkankercellen toevoegden, stegen METTL1‑niveaus en m7G‑markeringen; wanneer ze HMGB1 in CAF‑geconditioneerd medium blokkeerden, verdween dit effect. Nog dieper in de keten identificeerden ze één belangrijk RNA‑doel van METTL1: NET1, een gen dat groei en beweging van cellen stimuleert. CAFs verhoogden zowel de m7G‑tagging als de hoeveelheid NET1‑RNA en NET1‑eiwit, en METTL1 bond fysiek aan NET1‑RNA om het te stabiliseren. Minder METTL1 leidde tot minder gemodificeerd NET1, zwakkere overlevingssignalen in kankercellen en grotere gevoeligheid voor osimertinib.
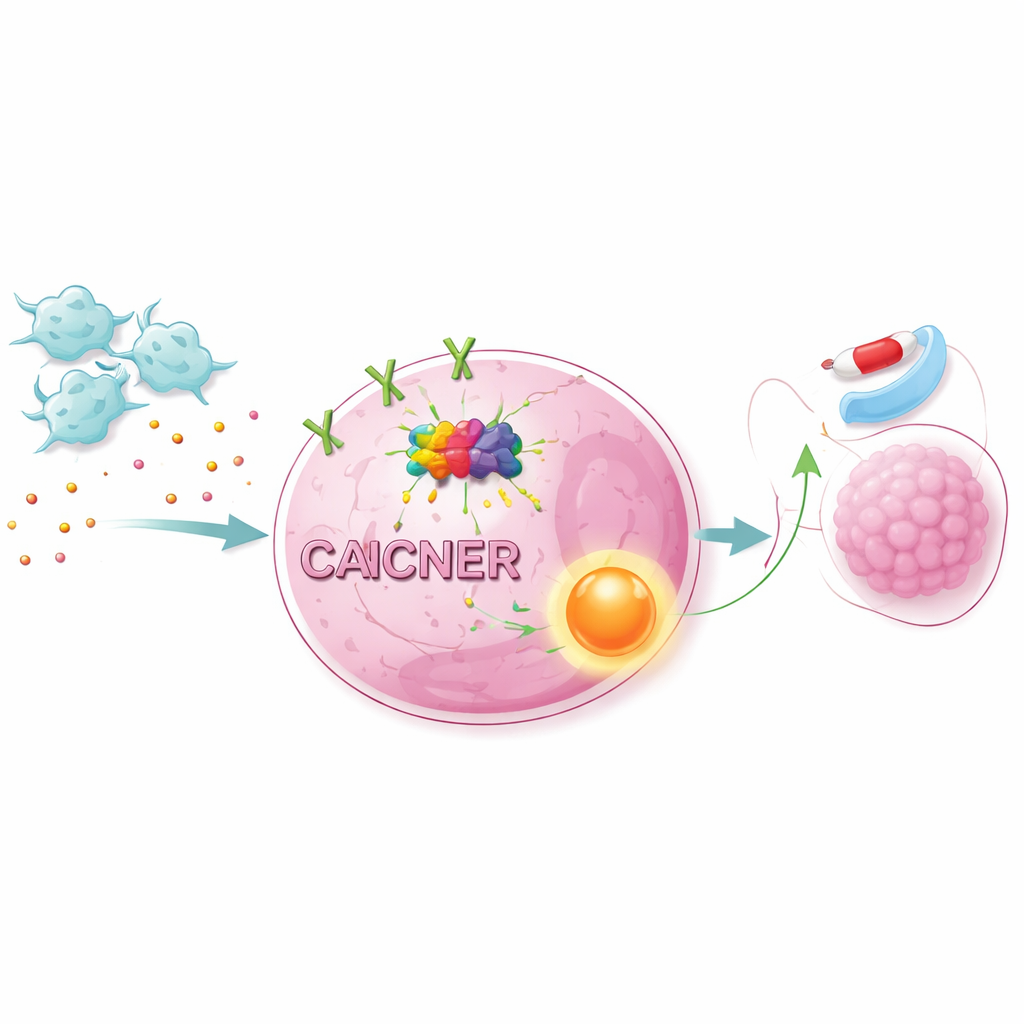
Het inschakelen van overlevingsroutes binnen kankercellen
Het versterkte NET1‑signaal stond niet op zichzelf. Door grootschalige RNA‑gegevens te combineren met pad‑analyses toonden de wetenschappers aan dat CAFs een belangrijke groeien overlevingsroute binnen cellen activeren, bekend als het AKT/NF‑κB‑pad. Het blokkeren van AKT of NF‑κB met specifieke remmers maakte longkankercellen gevoeliger voor osimertinib, zelfs in aanwezigheid van CAFs. Het veranderen van NET1‑niveaus had soortgelijke effecten: het verlagen van NET1 verzwakte de CAF‑bescherming, terwijl het verhogen van NET1 de resistentie versterkte. In muismodellen met geïmplanteerde menselijke longkankercellen lieten toegevoegde CAFs tumoren sneller groeien en minder responsief worden voor osimertinib. Het knockdown van METTL1 in de kankercellen verminderde m7G‑merken, verlaagde NET1‑expressie en padactivatie, en remde sterk het door CAFs gestimuleerde tumorgroeien.
Wat dit betekent voor toekomstige longkankerbehandeling
Voor mensen met EGFR‑gemuteerde longkanker biedt dit werk een nieuwe manier om te begrijpen waarom krachtige middelen zoals osimertinib uiteindelijk falen. In plaats van alleen nieuwe mutaties in kankercellen de schuld te geven, belicht het een moleculaire keten die buiten de tumorcel begint — met CAFs die HMGB1 uitscheiden — en loopt via METTL1, m7G‑merken op NET1, naar activering van overlevingspaden die de werking van het middel verminderen. Het onderbreken van deze keten op enig punt zou in principe de gevoeligheid voor behandeling kunnen herstellen of verlengen. Hoewel middelen die direct METTL1, HMGB1 of specifieke m7G‑gemarkeerde RNA’s targeten nog in een vroeg stadium verkeren, suggereert de studie dat het combineren van osimertinib met therapieën gericht op de ondersteunende cellen van de tumor of hun RNA‑modificerende signalen kan helpen om deze vorm van longkanker langer onder controle te houden.
Bronvermelding: Qian, Y., Gong, Z., Jia, Y. et al. Cancer-associated fibroblasts promote osimertinib resistance in non-small cell lung cancer cells via METTL1-mediated NET1 m7G modification. Cell Death Dis 17, 248 (2026). https://doi.org/10.1038/s41419-026-08505-7
Trefwoorden: osimertinib‑resistentie, niet‑kleincellige longkanker, fibroblasten geassocieerd met kanker, RNA‑methylatie, METTL1 NET1‑pad