Clear Sky Science · nl
miR-424(322)~503 belemmert de progressie van colonkanker gedreven door PTEN-tekort
Waarom deze studie belangrijk is voor colonkanker
Colonkanker blijft een van de meest voorkomende en dodelijke kankers wereldwijd, en veel patiënten krijgen ondanks chirurgie, chemotherapie en gerichte therapieën toch een gevorderde ziekte. Deze studie onderzoekt een klein stel genetische "dimmschakelaars" genaamd microRNA’s die de tumorgroei kunnen vertragen of versnellen. Door te achterhalen hoe één specifiek microRNA-cluster samenwerkt met een goed bekend tumor-suppressorgen, PTEN, helpt het werk te verklaren waarom sommige colonkankers agressiever worden en wijst het op nieuwe manieren om risico te voorspellen en therapieën te ontwerpen.
Kleine RNA-schakelaars met grote impact
MicroRNA’s zijn korte RNA-moleculen die geen eiwitten coderen maar fijnafstellen hoe honderden genen in een cel worden gebruikt. Het miR-424(322)~503-cluster, bestaande uit twee verwante microRNA’s, heeft onderzoekers verbaasd omdat het in verschillende kankers als rem of als versnellende factor kan fungeren. Bij colonkanker was zijn rol onduidelijk. De auteurs richtten zich op kankers die worden aangedreven door verlies van PTEN, een gen dat normaalgroeisignalen onder controle houdt en vaak is gewijzigd in colon-tumoren. Ze stelden een eenvoudige maar krachtige vraag: wat gebeurt er met de ontwikkeling van colonkanker wanneer zowel PTEN als dit microRNA-cluster ontbreken?
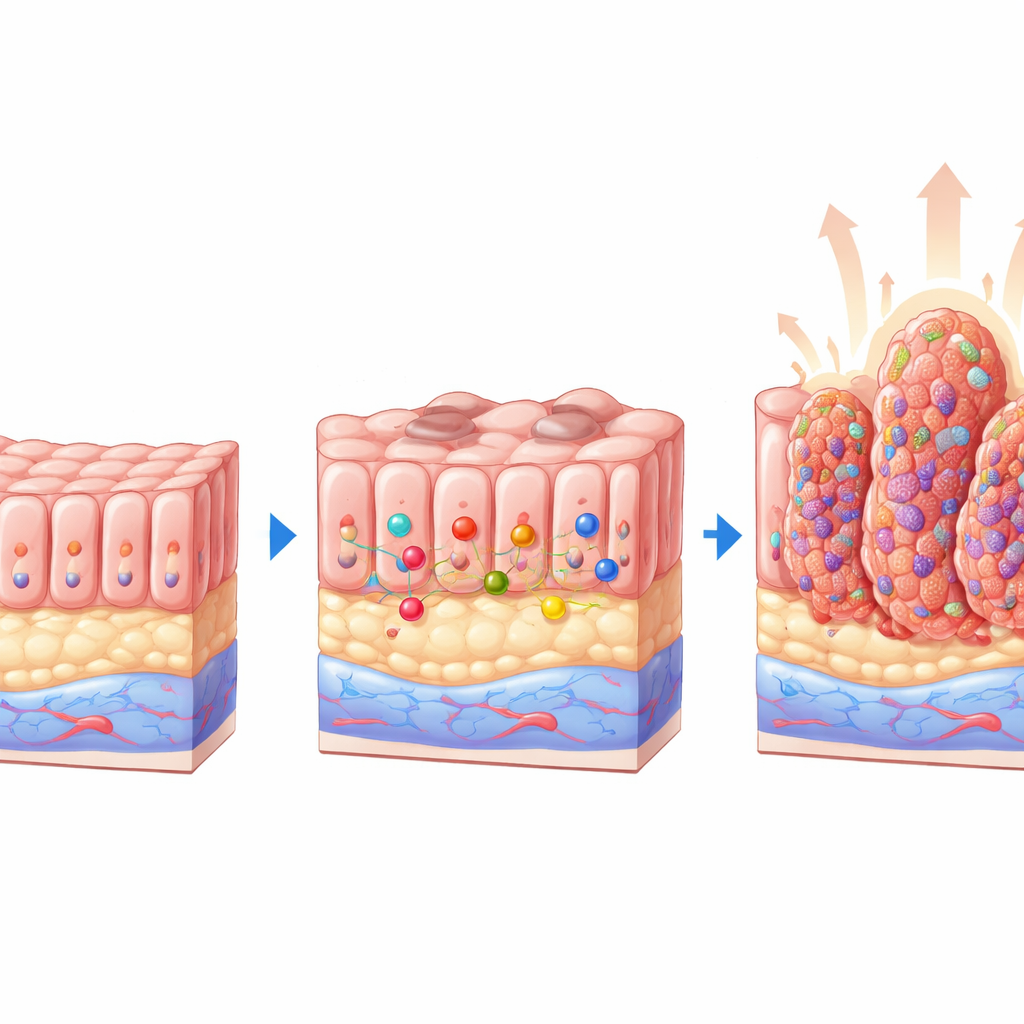
Muismodellen tonen een beschermende rol
Om dit te beantwoorden gebruikten de onderzoekers genetisch gemodificeerde muizen waarbij PTEN uitschakelbaar is in het darmslijmvlies, en kruisten deze met muizen die het miR-424(322)~503-cluster misten. Dit leverde vier groepen op: normale dieren, muizen die alleen de microRNA’s misten, muizen die alleen PTEN misten en dubbel knockout-muizen die beide misten. Na het induceren van PTEN-verlies onderzochten ze de darmen zorgvuldig. Dieren met alleen PTEN-verlies ontwikkelden meerdere kleine poliepen, veelal met vroegtijdige abnormale weefselveranderingen. In scherp contrast vertoonden muizen die zowel PTEN als het microRNA-cluster misten veel meer laesies, grotere poliepen en een hoger aandeel gevorderde afwijkingen, waaronder hooggradige dysplasie en duidelijk adenocarcinoom. Het microRNA-cluster op zichzelf veroorzaakte geen ziekte, wat aangeeft dat het verlies ervan vooral schadelijk is wanneer PTEN al ontbreekt.
Onveranderde klassieke route, verschuiving naar nieuwe daders
Colonkanker wordt vaak aangedreven door overactivatie van de Wnt/β-catenine-route, een belangrijke baan die stamcellen in de darm reguleert. Omdat dit microRNA-cluster die route in borstweefsel kan beïnvloeden, onderzochten de auteurs of dat hier ook het geval was. Tot hun verrassing veranderden de niveaus en locatie van β-catenine en zijn coreceptor LRP6 in de darm niet toen het microRNA-cluster werd verwijderd, zelfs niet in de dubbel knockout-dieren. In plaats daarvan wees grootschalige genexpressieprofilering elders heen: tumoren die zowel PTEN als de microRNA’s misten toonden sterke signaturen van weefselhermodellering, wondrespons en epitheel‑naar‑mesenchymale transitie, een programma dat gekoppeld is aan invasie en metastase. Signaleringsroutes aangedreven door MAP-kinases (ERK1/2 en p38) en door de groeifactor TGFβ waren daarbij bijzonder verrijkt.
Hoe groeisignalen ontsporen
Dieper gravend onderzochten de onderzoekers eiwitten in het darmweefsel. Ze vonden dat terwijl alleen PTEN-verlies het PI3K/AKT-pad versterkte, het toevoegen van verlies van het microRNA-cluster een verdere toename van MAPK-activiteit opleverde: meer geactiveerd JNK, p38, MKK4 en vooral ERK1/2. Deze sterk actieve signalen gingen samen met hogere niveaus van cycline D1, een belangrijke aanjager van celdeling. Tegelijkertijd stegen componenten van het TGFβ-pad die de activiteit bevorderen (SMAD3 en SMAD4), terwijl een interne remmer (SMAD7) daalde, en kankercellen toonden sterkere nucleaire SMAD2/3-kleuring, consistent met activatie van het pad. Door muizen-tumorgenexpressie te vergelijken met voorspelde microRNA-doelen identificeerde het team IGF1, een krachtige groeifactor die in MAPK-cascades voedt, als een direct doel van het miR-424(322)~503-cluster. Wanneer de microRNA’s afwezig waren, ontsnapte IGF1 aan repressie en dreef het MAPK-signaal nog hoger. Analyses van menselijke colonkanker-datasets weerspiegelden deze bevindingen: IGF1 was hoger in tumoren met lage miR-424 of miR-503, en het lange niet-coderende RNA dat deze microRNA’s herbergt, MIR503HG, evenals de microRNA’s zelf, waren coördinatief veranderd in patiëntentumoren.
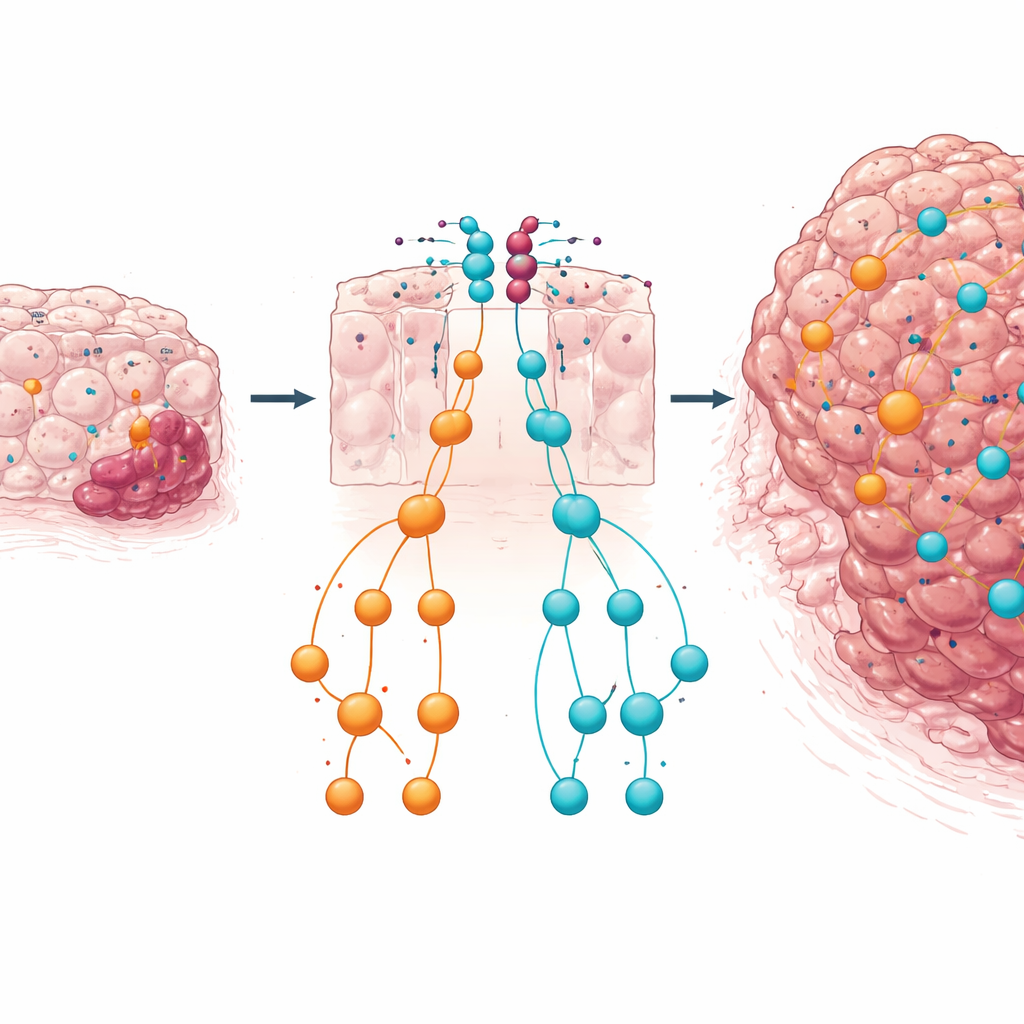
Een dubbele vangnet en wat het voor patiënten betekent
Samengevat suggereren de resultaten dat in PTEN-deficiënt darmslijmvlies het miR-424(322)~503-cluster fungeert als een tweede vangnet. Wanneer PTEN verloren gaat, worden deze microRNA’s opgehoogd, deels door signalen zoals TGFβ, en werken ze om krachtige groeiroutes zoals IGF1–MAPK en TGFβ–SMAD te remmen. Als deze microRNA-rem wordt verwijderd, lopen groei- en hermodellering-signalen ongehinderd door en versnellen ze de overgang van goedaardige poliepen naar invasieve kanker. Voor een lezer zonder specialistische kennis is de kernboodschap dat niet alle genetische veranderingen in een tumor in dezelfde richting werken: sommige vormen ingebouwde verdedigingsmechanismen. Begrijpen hoe PTEN en dit microRNA-cluster samenwerken om celgroei in balans te houden, kan helpen risicopatiënten te identificeren en inspireren tot combinatietherapieën die zowel de PI3K/AKT- als de MAPK/TGFβ‑assen in colorectale kanker aanpakken.
Bronvermelding: Vidal-Sabanés, M., Bonifaci, N., Navaridas, R. et al. miR-424(322)~503 impairs colon cancer progression driven by PTEN deficiency. Cell Death Dis 17, 254 (2026). https://doi.org/10.1038/s41419-026-08504-8
Trefwoorden: darmkanker, PTEN, microRNA, MAPK-signaaltransductie, TGF-beta