Clear Sky Science · nl
ROR1-PI3K/AKT-signaal stuurt adaptieve resistentie tegen celdelingsblokkade in TP53-gemuteerde eierstokkanker
Waarom dit onderzoek belangrijk is voor de gezondheid van vrouwen
Eierstokkanker behoort tot de dodelijkste vormen van kanker bij vrouwen, grotendeels omdat tumoren vaak resistent worden tegen chemotherapie. Deze studie stelt een cruciale vraag: wanneer krachtige middelen zijn ontworpen om kankercellen door een dodelijke delingsfout te duwen, hoe slagen die cellen er dan toch in om te overleven, en kan die ontsnappingsroute zelf worden omgezet in een kwetsbaarheid? Door eierstokkankercellen weken tot maanden te volgen onder behandeling, ontdekken de onderzoekers een centraal controlesysteem in de cellen dat bepaalt of ze blijven delen of zich terugtrekken en schade repareren—en onthullen een nieuwe manier om tumoren aan te pakken die al hebben geleerd standaardmiddelen te weerstaan. 
Twee veelgebruikte middelen, één gedeelde ontsnappingsroute
Het team richtte zich op hooggradig sereus eierstokkanker, de meest agressieve en voorkomende vorm van de ziekte, die bijna altijd mutaties draagt in het TP53-gen, de “bewaker van het genoom”. Omdat TP53 defect is, zijn deze tumoren in sterke mate afhankelijk van latere controles in de celdelingscyclus. Twee middelen die veel worden gebruikt of onderzocht in deze context benutten die zwakte: adavosertib, een experimentele WEE1-remmer die beschadigde cellen voortijdig in deling dwingt, en paclitaxel, een standaardchemotherapeuticum dat het interne skelet blokkeert dat nodig is voor de scheiding van chromosomen. In theorie zouden beide middelen kankercellen in een “mitotische catastrofe” moeten drijven—een fatale delingsfout. Toch passen tumoren zich in klinische en laboratoriumsituaties vaak aan. De onderzoekers creëerden langetermijnmodellen van resistentie door doses langzaam te verhogen over maanden, wat beter nabootst wat bij patiënten gebeurt dan korte, hoge-dosis experimenten.
Hoe kankercellen zichzelf herinrichten om te overleven
Met geavanceerde beeldvorming en “Cell Painting”—een techniek die meerdere celstructuren tegelijk kleuren—zagen de onderzoekers dat resistente cellen niet simpelweg als hun vroegere zelf uitzagen. Velen hadden meerdere kernen, gereorganiseerde interne skeletstructuren, en vormden dichter samengepakte clusters en kleinere, meer verspreide 3D-sferoïden; dit zijn kenmerken van gedeeltelijke morfologische omschakeling bekend als epitheliale–mesenchymale transitie. Deze fysieke veranderingen suggereerden dat de cellen de manier waarop ze zich bewegden, deelden en interageerden hadden herbedraad. Tegelijkertijd toonde gedetailleerde single-cell RNA-sequencing aan dat elke stof en cellijn zijn eigen patroon van veranderde genexpressie en chromosoomwijzigingen ontwikkelde. Ondanks deze genetische diversiteit verscheen een consistent thema: de activiteit van een groeien overlevingspad gecentreerd op PI3K en AKT nam toe in resistente modellen, vaak vergezeld van gerelateerde signaalroutes zoals MAPK en NF-κB.
Een cellulaire schakel tussen “snelle omzeiling” en “langzame reparatie”
Diepergravend vonden de onderzoekers dat dit PI3K/AKT-systeem werkt als een schakelaar die kankercellen tussen twee overlevingsstrategieën laat wisselen. In een “snelle-omzeiling”-modus schakelt hoge PI3K/AKT-activiteit het remmende eiwit FOXO3 uit en verzwakt het de celdelingscontroles, waardoor cellen blijven delen en de dodelijke effecten van adavosertib of paclitaxel ontwijken. In een contrasterende “langzame-reparatie”-modus is de PI3K/AKT-activiteit lager, blijft FOXO3 actief in de kern, vertragen cellen hun replicatie, schakelen DNA-reparatieprogramma’s in en pompen medicijnen efficiënter uit. Opmerkelijk was dat vroege kortdurende blootstelling aan geneesmiddelen in alle modellen een scherpe piek in PI3K/AKT-activiteit veroorzaakte; langere termijnresistentie vestigde zich vervolgens in ofwel de snelle-omzeiling- of de langzame-reparatiestatus, afhankelijk van de genetische achtergrond en eerdere signalering van de kanker. Dit toont aan dat hetzelfde centrale knooppunt zeer verschillende ontsnappingsroutes kan ondersteunen. 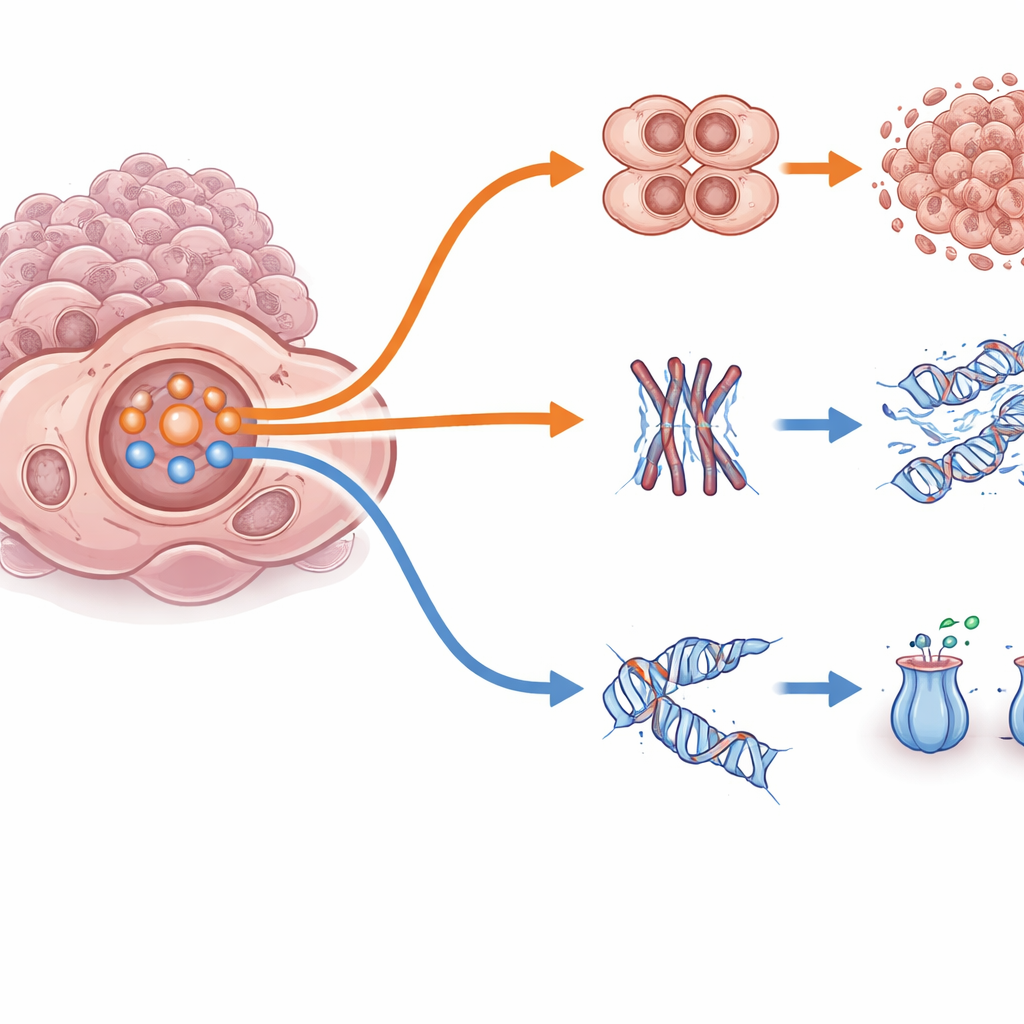
Een resistentiesignaal omzetten in een behandeldoel
Een belangrijke upstream-speler in dit knooppunt is ROR1, een receptorproteïne dat normaal gesproken schaars is in gezonde volwassen weefsels maar verhoogd voorkomt in verschillende kankers. In veel resistente eierstokkankermodellen steeg ROR1-niveau gelijktijdig met PI3K/AKT-activiteit. Het team toonde aan dat het omhoog of omlaag bijstellen van ROR1 kon beïnvloeden hoe gemakkelijk cellen resistentie tegen adavosertib of paclitaxel ontwikkelden, op een contextafhankelijke manier. Het meest belangrijk testten zij zilovertamab-vedotin, een antilichaam–medicijnconjugaat dat zich richt op ROR1 en een toxische lading afleveren. In zowel cellijnen als uit patiëntafgeleide 3D-organoïden waren ROR1-rijke, adavosertib-resistente tumoren bijzonder kwetsbaar voor dit middel, en de combinatie met adavosertib verbeterde vaak de celdood. Sommige paclitaxel-resistente modellen reageerden minder goed, waarschijnlijk omdat ze ook hun vermogen om geneesmiddelen uit te pompen hadden versterkt.
Wat dit betekent voor de toekomstige behandeling van eierstokkanker
Dit werk plaatst medicijnresistentie in TP53-gemuteerde eierstokkanker niet als een willekeurige gebeurtenis, maar als een gecoördineerde respons die wordt bestuurd door een centraal signaalschakelpunt. Door de PI3K/AKT–FOXO3-as en ROR1 als sleutelknopen te identificeren, wijst de studie op praktische strategieën: combineer mitose-gerichte middelen zoals adavosertib en paclitaxel met therapieën die het resistentieknooppunt blokkeren of ROR1 op resistente cellen exploiteren. Omdat ROR1 grotendeels afwezig is in gezonde weefsels, zouden dergelijke combinaties selectief terugkerende, medicijngeharde tumoren kunnen aanvallen terwijl normale cellen worden gespaard. Hoewel deze resultaten afkomstig zijn uit laboratoriummodellen en patiëntafgeleide culturen en nog geen afgeronde klinische studies vertegenwoordigen, bieden ze een duidelijke routekaart voor het ontwerpen van slimmer en duurzamer behandelingen voor vrouwen met hooggradig sereus eierstokkanker.
Bronvermelding: Raivola, J., Rantanen, F., Dini, A. et al. ROR1-PI3K/AKT signaling drives adaptive resistance to cell cycle blockade in TP53 mutated ovarian cancer. Cell Death Dis 17, 276 (2026). https://doi.org/10.1038/s41419-026-08501-x
Trefwoorden: eierstokkanker, medicatieresistentie, PI3K AKT-route, ROR1 antilichaamtherapie, celdelingsremmers