Clear Sky Science · nl
mTOR-gedreven onderdrukking van autophagie definieert metabolische kwetsbaarheid bij CDK4/6-remmerresistente HR+/HER2− borstkanker
Waarom dit belangrijk is voor borstkankerpatiënten
Veel vrouwen met gevorderde borstkanker leven nu langer dankzij middelen die CDK4/6-remmers worden genoemd; deze vertragen de delingssnelheid van tumoren. Helaas vinden de meeste tumoren uiteindelijk manieren om aan deze medicijnen te ontsnappen. Deze studie stelt een hoopgevende vraag: wanneer borstkanker resistent wordt tegen CDK4/6-middelen, ontstaat er dan een nieuwe zwakte die artsen zouden kunnen benutten met bestaande, relatief eenvoudige metabole geneesmiddelen zoals metformine of dichloorazijnzuur (DCA)?
Wanneer celdelingsremmers ophouden te werken
Artsen behandelen het meest voorkomende type borstkanker — hormoonreceptor-positief, HER2-negatief — vaak met hormoontherapie gecombineerd met CDK4/6-remmers zoals palbociclib of ribociclib. Deze middelen richten zich op eiwitten die cellen door de delingscyclus duwen. Na verloop van tijd passen sommige kankercellen zich echter aan en worden sterk resistent, waardoor ze blijven groeien ondanks hoge medicatiedoseringen. De onderzoekers bootsten dit probleem in het laboratorium na door borstkankercellijnen (T47D en MCF7) bloot te stellen aan toenemende hoeveelheden CDK4/6-remmers. Ze kregen twee soorten overlevenden: gedeeltelijk resistente cellen en een kleinere groep sterk resistente klonen die niet langer goed op de behandeling reageerden.
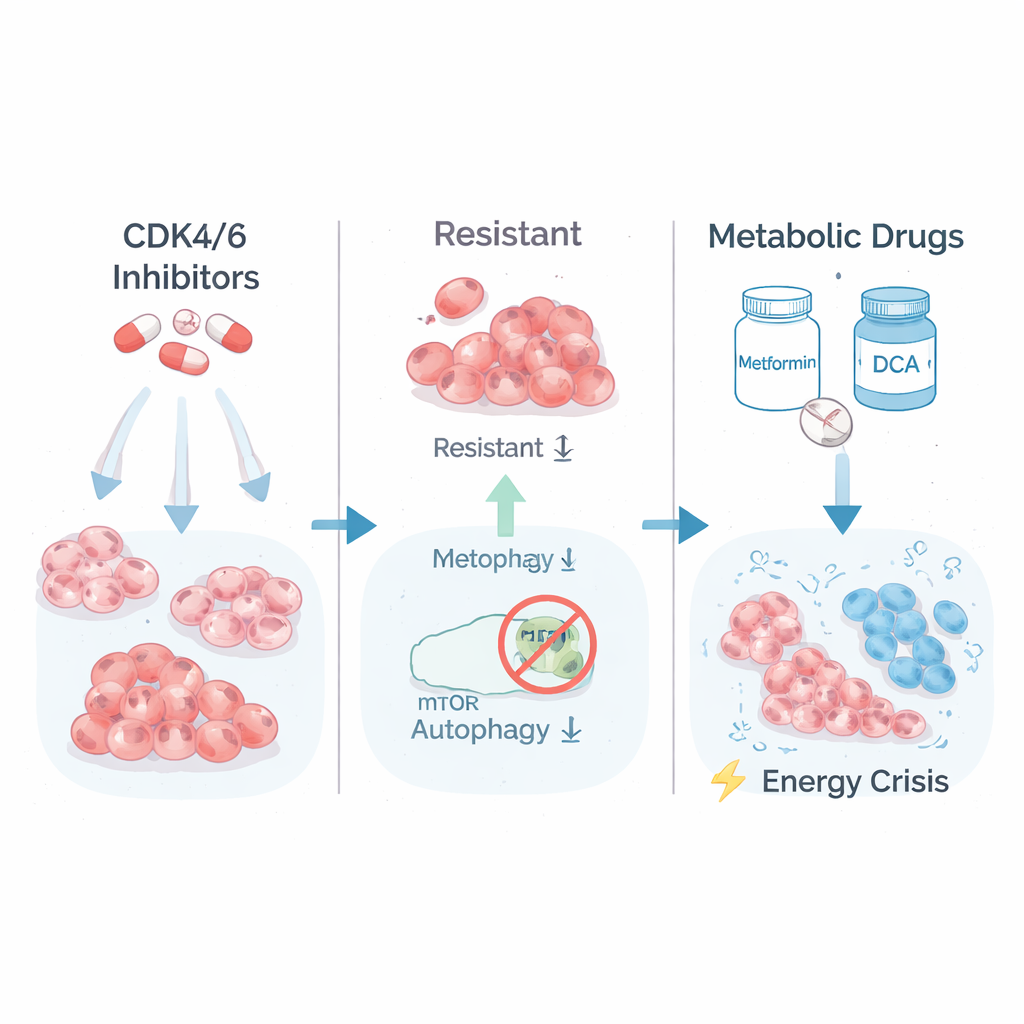
Een verborgen zwakte in het energiegebruik van tumoren
Om te begrijpen wat de sterk resistente cellen anders maakte, onderzocht het team welke genen aan- of uitgezet waren. Ze vonden dat de meest resistente cellen routes omhoog hadden geschroefd die betrokken zijn bij suikerverbranding (glycolyse) en bij groeisignalering die wordt geregeld door een eiwitcomplex genaamd mTORC1. Met andere woorden: deze cellen leefden in een hoge versnelling en verbruikten brandstof snel om te blijven groeien. De wetenschappers testten vervolgens of dit "hoge-versnelling"metabolisme tegen de cellen kon worden gebruikt. Ze behandelden de resistente en de ouderlijke cellen met metformine, een veelgebruikt diabetesmiddel dat de energiecentrales van de cel belast, en met DCA, dat cellen dwingt brandstof efficiënter te verwerken. Opmerkelijk genoeg bleken de meest medicijnresistente klonen nu het meest kwetsbaar: hun langetermijngroei in kweek stortte in onder metabole behandeling, terwijl ouderlijke en slechts gedeeltelijk resistente cellen veel minder werden aangetast.
Geblokkeerde zelfreiniging en een energiecrash
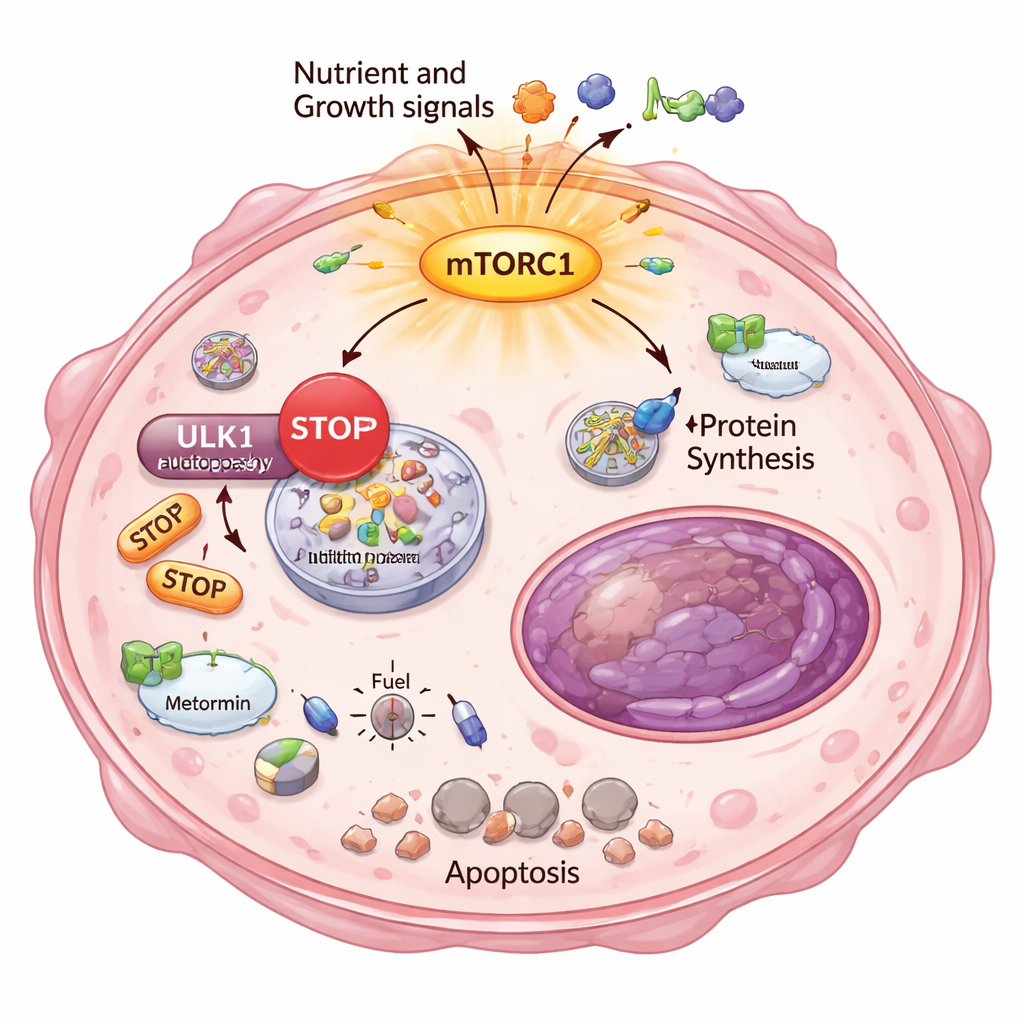
Waarom zouden deze uitwijkende kankercellen zo gevoelig zijn voor energiestress? Het antwoord lag in een ander basaal overlevingsproces: autofagie, het ingebouwde "recycling- en opruimsysteem" van de cel. Normaal gesproken, wanneer energie schaars is, breken cellen onderdelen af en hergebruiken die om te overleven. De onderzoekers toonden aan dat in de sterk resistente klonen mTORC1 overactief was en een chemische rem zette op ULK1, een belangrijke starter van autofagie. Met een gevoelige reporterassay lieten ze zien dat deze cellen autofagie niet goed konden inschakelen of opschalen, zelfs niet wanneer ze aangezet werden met metabole geneesmiddelen. Daardoor veroorzaakten metformine en DCA een ernstige energiecrisis: energielezers gingen aan, vetproductie viel stil en markers van onomkeerbare celdood verschenen — specifiek in de sterk resistente cellen.
Bewijs uit echte patiënttumoren
Laboratoriummodellen weerspiegelen niet altijd wat er bij patiënten gebeurt, dus wendde het team zich tot humane borstkankermonsters. Ze kleurden meer dan honderd kankers voor een marker van mTORC1-activiteit (gefosforyleerd 4E-BP1) en voor p62, een eiwit dat zich ophoopt wanneer autofagie geblokkeerd is. Tumoren met hoge mTORC1-activiteit hadden de neiging meer p62 te hebben, wat het idee ondersteunt dat een patroon van "overgestuurde groeisignalen plus gebrekkige recycling" bestaat in echte borstkankers, niet alleen in cellijnen. Dit suggereert dat een subset van patiënten tumoren kan hebben met dezelfde metabole zwakte die in het laboratorium werd waargenomen.
Wat dit zou kunnen betekenen voor toekomstige behandelingen
Voor een niet-specialist is de kernboodschap dat wanneer borstkankers zich ontwikkelen om krachtige CDK4/6-medicijnen te ontlopen, ze zich mogelijk ook in een metabole hoek schilderen. Door groeisignalen permanent aan te zetten en de cellulaire recycling uit te schakelen, worden deze tumoren sterk afhankelijk van een constante energietoevoer. De studie laat zien dat deze situatie benut kan worden met metabole geneesmiddelen zoals metformine en DCA, die al goed bekend zijn bij andere ziekten. Belangrijk is dat de auteurs voorstellen dat eenvoudige weefseltesten voor mTORC1-activiteit en autofagiemarkers kunnen helpen patiënten te identificeren waarvan de resistente tumoren vatbaar zijn voor dit soort metabole aanval, wat de deur opent naar meer gepersonaliseerde reddingsbehandelingen nadat CDK4/6-remmers falen.
Bronvermelding: von Wichert, L., Stroh, A., Witt, M. et al. mTOR-driven autophagy suppression defines metabolic vulnerability in CDK4/6 inhibitor-resistant HR+/HER2− breast cancer. Cell Death Dis 17, 235 (2026). https://doi.org/10.1038/s41419-026-08496-5
Trefwoorden: borstkanker, resistentie tegen CDK4/6-remmers, mTOR, autofagie, metabole therapie