Clear Sky Science · nl
Splice-switching van het oncogene BCS1L-isoform onderdrukt de progressie van eierstokkanker door verstoring van mitochondriale functie
Krachtcentrales in kankercellen
Elke cel in ons lichaam is afhankelijk van kleine krachtcentrales die mitochondriën worden genoemd. Kankercellen, die snel groeien en uitzaaien, hebben bijzonder veel energie nodig. Deze studie onthult hoe eierstokkanker één van zijn belangrijke mitochondriale helper-eiwitten herbedrukt, en laat zien dat het voorzichtig omzetten van een moleculaire "schakelaar" op deze helper tumoren kan uithongeren terwijl gezond weefsel grotendeels gespaard blijft.
Waarom tumoren leunen op hun motoren
Eierstokkankercellen, zoals veel kankers, kunnen flexibel verschillende energiebronnen aanboren. Door grote patiëntendatabanken en single-cell profielen te doorzoeken, vonden de onderzoekers dat veel eierstokkankers hun mitochondriën in een hoge versnelling laten draaien, bekend als oxidatieve fosforylering, of OXPHOS. Tumoren met deze verhoogde mitochondriale activiteit waren agressiever en kwamen vaker voor bij gevorderde ziekte. Onder de vele eiwitten die de mitochondriale energie-machinerie opbouwen, viel er één op: BCS1L, een chaperonne die helpt bij de assemblage van Complex III, een centraal knooppunt in de energiepijplijn van de cel. Tumoren met hoge OXPHOS en bepaalde tumorcelsubtypen toonden bijzonder sterke BCS1L-activiteit, wat erop wees dat kankercellen zwaar leunden op deze helper om hun motoren te laten draaien.
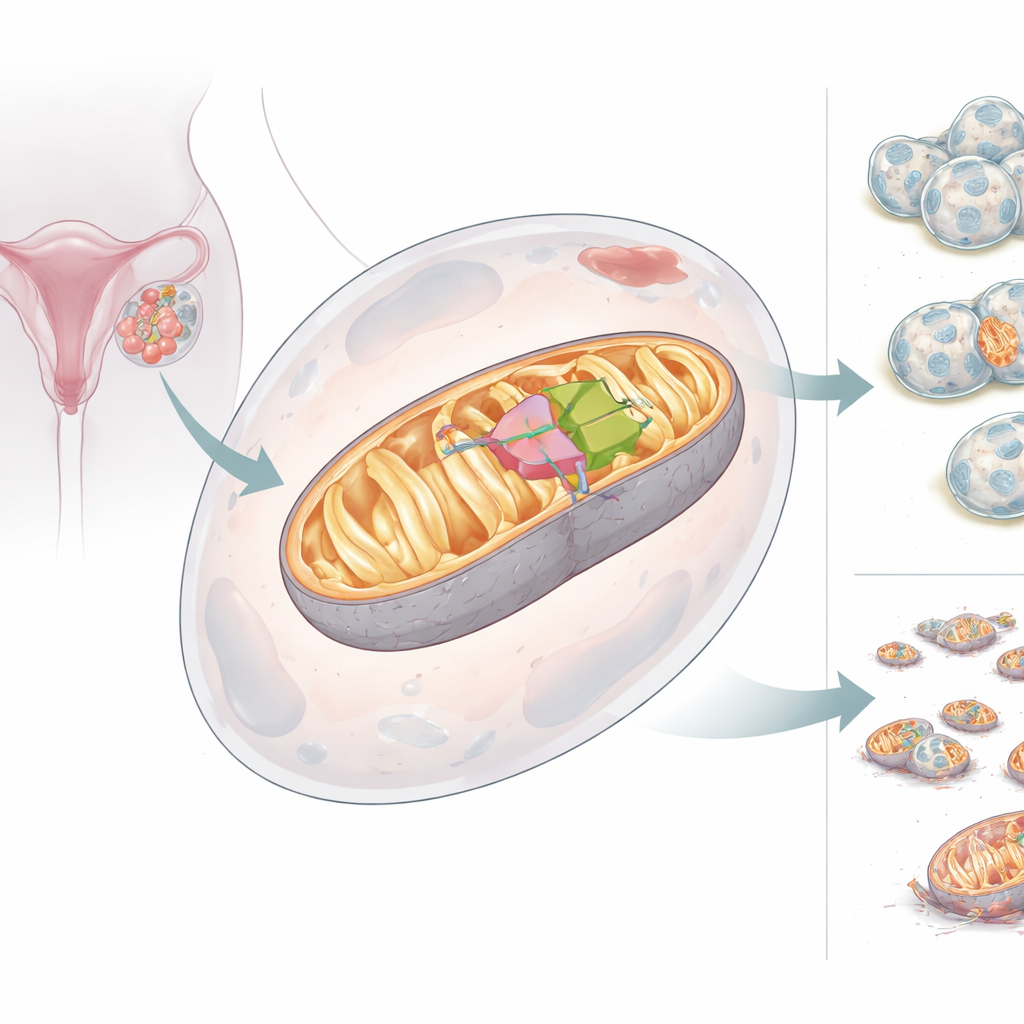
Twee gezichten van een mitochondriale helper
Het team ontdekte dat het BCS1L-gen twee versies, of isoformen, van het eiwit kan produceren. De volledige vorm, BCS1L-L, draagt een ingebouwd adreslabel dat het naar de mitochondriën stuurt, waar het een juiste assemblage van Complex III ondersteunt en een sterke energieproductie mogelijk maakt. De kortere vorm, BCS1L-S, mist een belangrijk segment en kan de mitochondriën niet bereiken; in plaats daarvan bevindt het zich in het cytosol en de celkern en draagt het niet bij aan energieproductie. In gezonde weefsels is de korte versie algemeen, maar in eierstokkankers kantelt de balans: de lange, aan mitochondriën gebonden vorm domineert. Wanneer cellen gedwongen werden meer BCS1L-L te maken, genereerden hun mitochondriën meer energie, behielden ze een sterker membraanpotentiaal, produceerden ze minder schadelijke zuurstofbijproducten en waren ze resistenter tegen celdood. Bij vermindering van BCS1L fragmenteren de mitochondriën, daalt de energieproductie, nemen schadelijke zuurstofmoleculen toe en zijn kankercellen gevoeliger voor het overlijden.
Hoe kanker het bericht herschakelt
Het produceren van de lange of korte BCS1L-versie hangt af van hoe de cel zijn RNA-bericht bewerkt, een proces dat splicing heet. De onderzoekers zochten naar eiwitten die aan het BCS1L-RNA binden en deze keuze beïnvloeden. Ze richtten zich op USP39, een splicingfactor die al in verband is gebracht met meerdere kankers. In eierstokkankercellen bindt USP39 nabij het RNA-segment dat exon 2 van BCS1L wordt en bevordert het de inclusie daarvan, waardoor de voorkeur wordt gegeven aan de lange, naar mitochondriën gerichte vorm. Wanneer USP39 werd stilgelegd, sloegen cellen dit segment vaker over, wat verschuiving naar de korte BCS1L-S-vorm veroorzaakte. Deze verschuiving verzwakte Complex III, verminderde mitochondriale respiratie en ATP-productie, verhoogde oxidatieve stress en veroorzaakte celdood in kankercellen. Het herstellen van BCS1L-L in deze cellen redde een groot deel van hun mitochondriale functie en overleving, wat aantoont dat USP39 een kritieke mitochondriale schakel grotendeels via BCS1L aanstuurt.
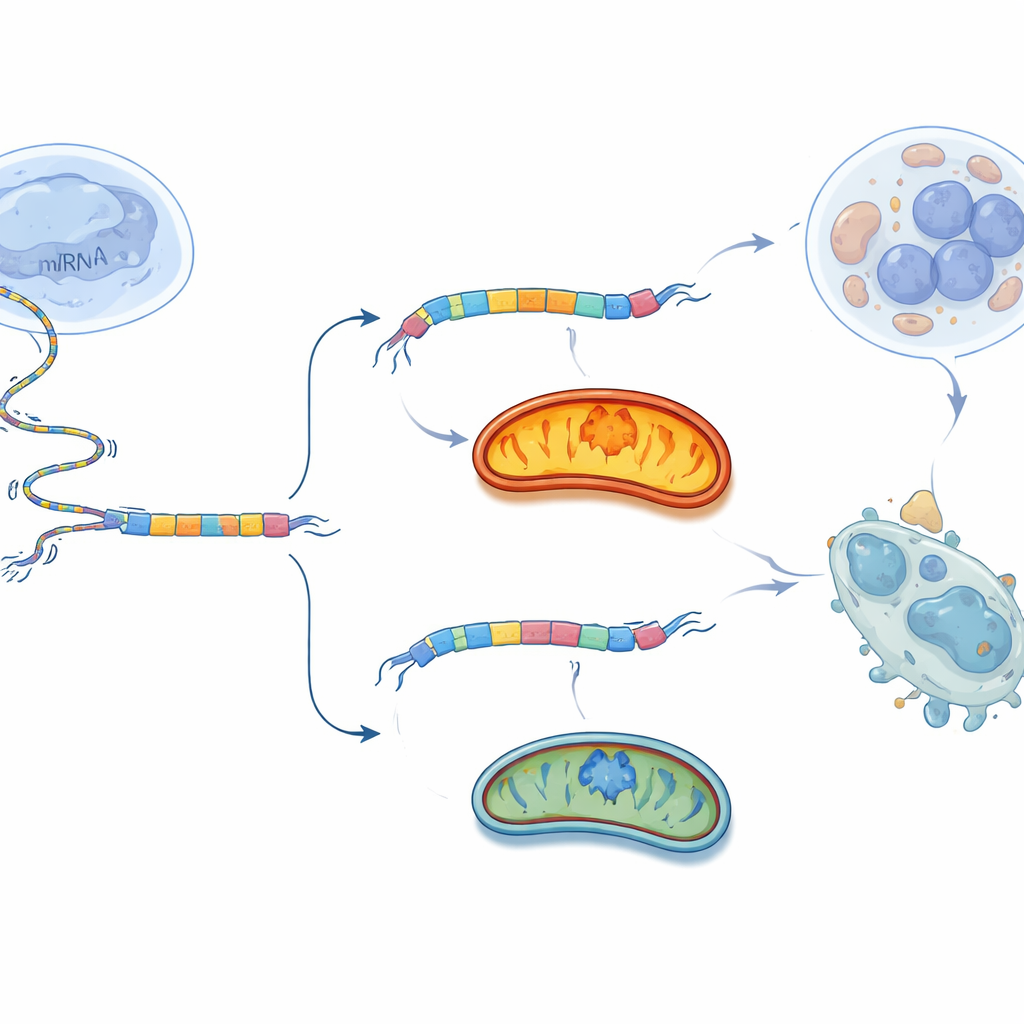
De schakel tegen de tumor zetten
In plaats van mitochondriën algemeen te blokkeren, wat veel weefsels zou kunnen schaden, probeerde het team een meer chirurgische tactiek: het bijsturen van de splicingkeuze van BCS1L zelf. Ze ontwierpen korte stukjes genetisch materiaal, antisense-oligonucleotiden (ASO's), die net rond exon 2 van het BCS1L-RNA binden. Deze ASO's werken als kleine wasknijpers, ze veranderen hoe het splicingmachinerie het bericht leest en moedigen de cel aan exon 2 over te slaan. In in-vitro gekweekte eierstokkankercellen verminderde de beste ASO sterk de lange BCS1L-L-vorm en verhoogde de korte BCS1L-S-vorm. Als gevolg daalden mitochondriale respiratie en ATP-productie, stegen de schadelijke zuurstofniveaus en gingen veel meer cellen geprogrammeerd ten onder. Wanneer dezelfde ASO in muismodellen met eierstokkankertumoren werd geïnjecteerd, vertraagde de tumorgroei en wogen de tumoren minder, met een veel sterker effect op kankercellen dan op normale fibroblasten.
Wat dit voor patiënten zou kunnen betekenen
In eenvoudige bewoordingen laat dit werk zien dat veel eierstokkankers afhankelijk zijn van een "turbo"-versie van een mitochondriaal helper-eiwit om hun groei van brandstof te voorzien. Een splicingfactor, USP39, kantelt het RNA-bewerkingssysteem van de cel zodat meer van deze turboversie wordt gemaakt, waardoor de krachtcentrales van de tumor in topconditie blijven. Door precies ontworpen ASO's te gebruiken om de splicingkeuze terug te draaien naar de zwakkere versie, kunnen onderzoekers selectief de mitochondriën van kankercellen verzwakken, hun dood veroorzaken en de meeste normale cellen minder geraakt laten. Hoewel het afleveren van zulke ASO-geneesmiddelen naar tumoren een grote uitdaging blijft, wijst deze studie op de BCS1L-splice-schakelaar als een veelbelovend en zeer specifiek aangrijpingspunt voor de behandeling van eierstokkanker.
Bronvermelding: Xu, M., Wang, Z., Yang, S. et al. Splice-switching of the oncogenic BCS1L isoform suppresses ovarian cancer progression by disrupting mitochondrial function. Cell Death Dis 17, 293 (2026). https://doi.org/10.1038/s41419-026-08495-6
Trefwoorden: eierstokkanker, mitochondriën, RNA-splicing, BCS1L, antisense-oligonucleotiden