Clear Sky Science · nl
NSD2 remt de expressie van PD-L1 via oxidatieve fosforylering om immuursurveillance bij hepatocellulair carcinoom te regelen
Waarom dit leverkankerverhaal ertoe doet
Hepatocellulair carcinoom, de meest voorkomende vorm van leverkanker, wordt vaak laat gediagnosticeerd en is resistent tegen veel behandelingen. Immunotherapie‑medicijnen die het PD‑L1 “onzichtbaarheidsmantel” op tumorcellen blokkeren, helpen sommige patiënten, maar niet de meeste. Deze studie onthult een onverwachte speler, een eiwit genaamd NSD2, dat de koppeling vormt tussen hoe leverkankercellen energie maken en hoe zichtbaar ze zijn voor het immuunsysteem. Inzicht in deze koppeling kan wijzen op nieuwe manieren om huidige therapieën te versterken en bepalen welke patiënten waarschijnlijk baat hebben.
Een verrassende rol voor een bekend kanker‑eiwit
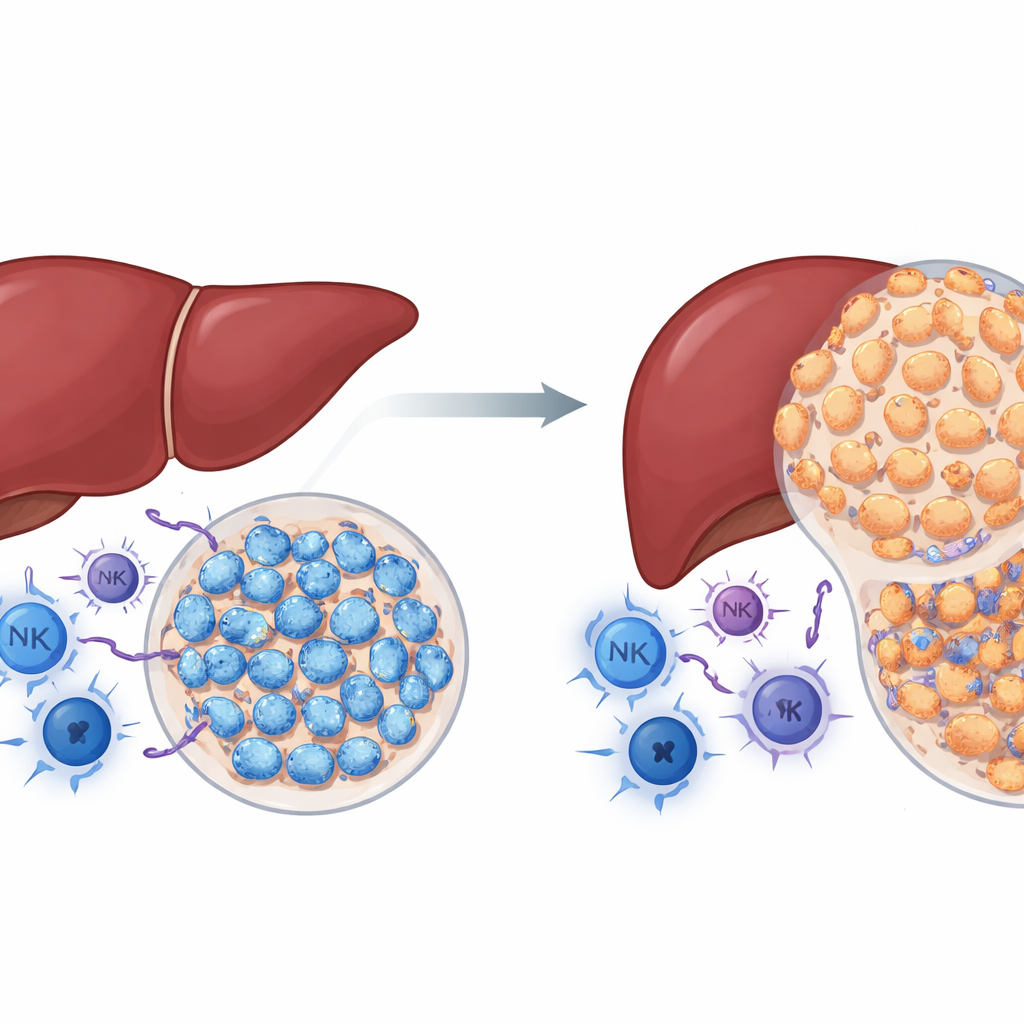
NSD2 is een enzym dat histonen modificeert, de eiwitten waar DNA omheen gewikkeld zit. In veel kankers wordt NSD2 gezien als een aanjager van tumorgroei. De auteurs vroegen zich af of dat ook het geval is bij leverkanker. Met genetisch gemodificeerde muizen waarin NSD2 specifiek in levercellen is aangezet, behandelden ze dieren met een chemische stof die betrouwbaar levertumoren induceert. Tegen de verwachtingen in ontwikkelden muizen met extra NSD2 veel minder en kleinere tumoren dan normale muizen, en hun lever toonde minder schade, littekenvorming en celproliferatie. Tegelijkertijd bevatten tumoren uit NSD2‑overexpressieve leverweefsels meer kankervijandige immuuncellen, waaronder helper‑ en killer‑T‑cellen en natural killer‑cellen. Deze bevindingen suggereren dat NSD2, binnen een intact immuunsysteem, zich minder als een gaspedaal en meer als een rem op leverkanker gedraagt.
Energiecentrales en brandstofgebruik in tumorcellen
Om te begrijpen hoe NSD2 tumoren remt, kaartte het team genactiviteit in leverweefsel in. Ze vonden dat overexpressie van NSD2 genen die betrokken zijn bij oxidatieve fosforylering sterk dempte — het proces waarmee mitochondriën, de cel’s “krachtcentrales”, energie genereren met behulp van zuurstof. Vervolgexperimenten in muis‑ en menselijke leverkanker‑cellijnen toonden dat het verhogen van NSD2 de expressie van veel oxidatieve‑fosforyleringsgenen verlaagde, zuurstofverbruik en ATP‑productie reduceerde, en het mitochondriale membraanpotentiaal deed dalen, een teken van verminderde mitochondriale activiteit. Tegelijkertijd verbruikten deze cellen minder glucose maar verschoven ze niet naar meer glycolyse, wat wijst op een netto vermindering van energieopbrengst. Verlies van NSD2 gaf de tegengestelde effecten, met versterkte mitochondriale kracht en brandstofgebruik.
Hoe NSD2 energie en immuunzichtbaarheid herbedraadt
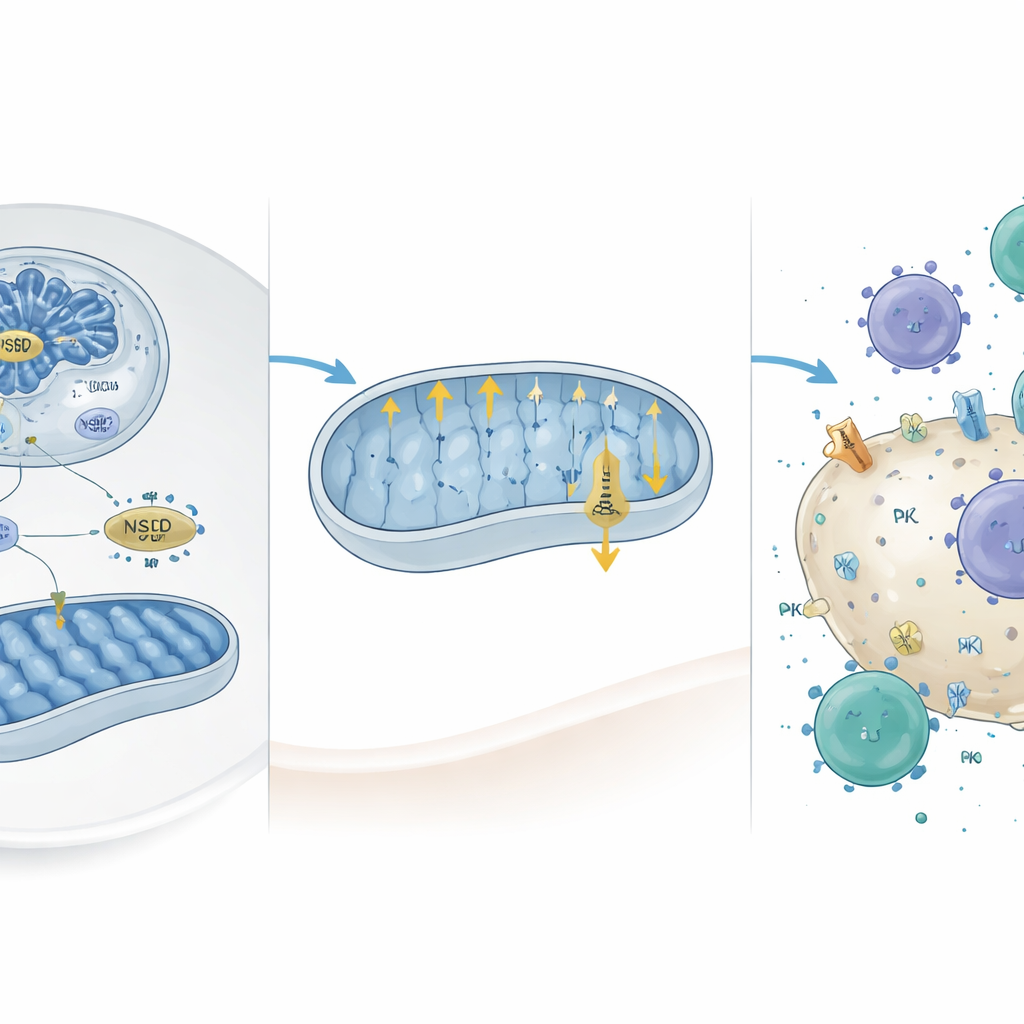
Dieper gravend combineerden de onderzoekers genoom‑wijde chromatinekaarten met genexpressiegegevens en identificeerden ze een set genen die direct werden geactiveerd wanneer NSD2 aanwezig is. Twee hiervan, Camk2d en Prkce, staan bekend als remmers van mitochondriale activiteit. NSD2 verhoogde een specifieke histonmarkering (H3K36me2) bij hun promotors, waardoor hun expressie toenam. Het herintroduceren van deze genen in NSD2‑deficiënte leverkankercellen verminderde mitochondriaal zuurstofgebruik en ATP‑productie, wat bevestigt dat ze fungeren als downstream remmen van oxidatieve fosforylering onder NSD2. Belangrijk is dat eerder werk suggereerde dat sterk actieve mitochondriën gunstig zijn voor hoge PD‑L1‑niveaus op tumorcellen. In overeenstemming daarmee vonden de auteurs dat NSD2‑overexpressie PD‑L1‑niveaus verlaagde, terwijl verlies van NSD2 PD‑L1 op leverkankercellen en in tumoren verhoogde.
Het schild verlagen en de immuunaanval wekken
De functionele impact van deze moleculaire verschuivingen werd getest in muizen die leverinjecties kregen met kankercellen die zo waren gemanipuleerd dat ze NSD2 konden winnen of verliezen. Cellen zonder NSD2 vormden snel grotere tumoren, drukten meer PD‑L1 uit en werden door minder T‑cellen en natural killer‑cellen infiltreren, vooral minder geactiveerde killer‑T‑cellen. Toen de onderzoekers chemisch complex V van de mitochondriën blokkeerden, een sleutelcomponent van oxidatieve fosforylering, daalden PD‑L1‑niveaus in NSD2‑deficiënte cellen weer naar normaal en konden immuuncellen tumorceldood beter induceren. Evenzo verminderde het overexpressen van Camk2d of Prkce in NSD2‑ontbrekende cellen, of het behandelen van tumoren met een PD‑L1‑blokkerend antilichaam, de tumorgrootte en herstelde de infiltratie door immuuncellen. In patiëntendatasets werd lage NSD2‑expressie gekoppeld aan slechtere overleving maar, intrigerend genoeg, aan een betere respons op PD‑L1‑gerichte therapie, wat suggereert dat NSD2‑status kan helpen voorspellen wie baat heeft bij zulke geneesmiddelen.
Wat dit betekent voor toekomstige zorg bij leverkanker
Voor de algemene lezer is de kernboodschap dat deze studie NSD2 herdefinieert als een tumorreminter in leverkanker, althans in aanwezigheid van een werkend immuunsysteem. Door de zuurstofgebaseerde energieproductie van de cel terug te schroeven, verlaagt NSD2 indirect PD‑L1 op tumorcellen, verwijdert een deel van hun onzichtbaarheidsmantel en maakt het mogelijk dat immuuncellen ze herkennen en aanvallen. Deze nieuw beschreven NSD2–energie–PD‑L1‑keten suggereert twee praktische ideeën: ten eerste kunnen patiënten wiens tumoren NSD2 missen bijzondere kandidaten zijn voor PD‑L1‑blokkerende middelen; en ten tweede kan het combineren van middelen die mitochondriale energieproductie remmen met immunotherapie een krachtige combinatechniek tegen leverkanker bieden.
Bronvermelding: Zhang, W., Feng, W., Ma, C. et al. NSD2 inhibits the expression of PD-L1 via oxidative phosphorylation to control immune surveillance in hepatocellular carcinoma. Cell Death Dis 17, 284 (2026). https://doi.org/10.1038/s41419-026-08490-x
Trefwoorden: hepatocellulair carcinoom, NSD2, oxidatieve fosforylering, PD-L1, tumorimmunotherapie