Clear Sky Science · nl
SNRPD2-gemedieerde regulatie van DDX39B-splicing bevordert de progressie van endometriumkanker door de activering van CTSC-cryptische exonen te onderdrukken
Waarom verborgen boodschappen in kankergenen ertoe doen
Endometriumkanker, een veelvoorkomende baarmoederkanker, neemt wereldwijd toe, en toch hebben veel patiënten met gevorderde ziekte nog weinig effectieve opties. Deze studie onthult hoe een subtiel proces in cellen — de manier waarop zij genetische boodschappen knippen en plakken — endometriumtumoren kan aanzetten tot groei en verspreiding. Door een kwetsbaar "bedradingsschema" bloot te leggen waarop kankercellen vertrouwen, wijst het werk op nieuwe manieren om tumoren uit te schakelen met precieze genetische geneesmiddelen.
Een groeiende kanker die nieuwe antwoorden nodig heeft
Endometriumkanker is nu in veel westerse landen de meest voorkomende gynaecologische kanker, met een gestage toename van gevallen en sterfgevallen zowel in het Westen als in China. Chirurgie, bestraling, chemotherapie, hormoontherapie en immunotherapie worden allemaal toegepast, maar ze zijn verre van perfect. Het verwijderen van de baarmoeder betekent verlies van vruchtbaarheid, hormonale behandelingen falen vaak, en agressieve tumoren komen veelal terug. Deze uitdagingen hebben onderzoekers ertoe aangezet dieper in kankercellen te kijken naar moleculaire zwakke plekken die met meer gerichte therapieën aangetast kunnen worden.
Het splicingmachinerie van de cel als zwakke schakel
Om te functioneren worden onze genen eerst gekopieerd naar lange RNA-moleculen die in een proces dat splicing heet, moeten worden ingekort en aan elkaar genaaid. Gespecialiseerde eiwitmachines, spliceosomen genoemd, bepalen welke stukken blijven en welke worden weggegooid, en bewerken daarmee effectief het script dat cellen gebruiken om eiwitten te maken. Het team richtte zich op een spliceosoomcomponent genaamd SNRPD2, onderdeel van een familie van “Sm”-eiwitten die helpen bij de assemblage van de splicingmachinerie. Door grote kanker-gen- en eiwitdatabases te doorzoeken en monsters van patiënten te onderzoeken, vonden ze dat SNRPD2-niveaus opvallend hoger zijn in endometriumtumoren dan in normaal baarmoederslijmvlies, en dat patiënten van wie de tumoren meer SNRPD2 hebben, doorgaans slechter af zijn.
Een hoofdredacteur uitschakelen vertraagt tumoren
Om te testen of SNRPD2 louter een toeschouwer is of een actieve dader, zetten de onderzoekers het gen uit in endometriumkankercellijnen die in het laboratorium werden gekweekt. Toen SNRPD2 werd stilgelegd, deelden cellen zich langzamer, vormden ze minder kolonies en waren ze minder in staat te bewegen en door membranen heen te dringen — gedragingen die samenhangen met metastase. Toen deze gewijzigde cellen in muizen werden geïmplanteerd, waren de resulterende tumoren veel kleiner en toonden ze minder cellen in actieve deling. Belangrijk is dat het team antisense-oligonucleotiden ontwierp — korte, medicijnachtige stukjes synthetisch DNA — die specifiek op het RNA van SNRPD2 gericht zijn. In een patiënt-afgeleid xenograftmodel, waarin menselijke tumorfragmenten groeien in immuundeficiënte muizen, verlaagden deze antisensemiddelen scherp zowel SNRPD2-niveaus als de tumorgrootte, wat suggereert dat SNRPD2 op een klinisch relevante manier gekneed kan worden.
Een keten van drie stappen van splicingfout naar kankergroei
Door in de genetische data te duiken vroegen de onderzoekers hoe verlies van SNRPD2 RNA-boodschappen door het hele genoom herschakelt. Ze ontdekten dat wanneer SNRPD2 afneemt, een belangrijke RNA-verwerkende enzym, DDX39B, begint te haperen. Normaal helpt DDX39B bij het verwijderen van een bepaald intron — een RNA-segment dat eruit geknipt moet worden — uit zijn eigen boodschap. Zonder voldoende SNRPD2 blijft dat intron zitten, waardoor een foutieve versie van DDX39B-RNA ontstaat die de cel snel afbreekt. Lagere DDX39B heeft vervolgens een kettingreactie op een ander gen, CTSC, dat codeert voor een eiwitafbrekend enzym dat bekendstaat om het ondersteunen van tumorgroei en -verspreiding. Onder gezonde omstandigheden wordt een verborgen “cryptisch” exon in CTSC-RNA genegeerd, waardoor cellen volwaardige, actieve CTSC-eiwitten kunnen maken. Bij verminderde DDX39B wordt dit cryptische exon per ongeluk opgenomen, waardoor voortijdige stopcodes in het RNA worden ingevoegd. De misvormde CTSC-boodschap wordt afgebroken voordat er veel eiwit geproduceerd kan worden, en kankercellen verliezen een deel van hun agressieve vermogen.
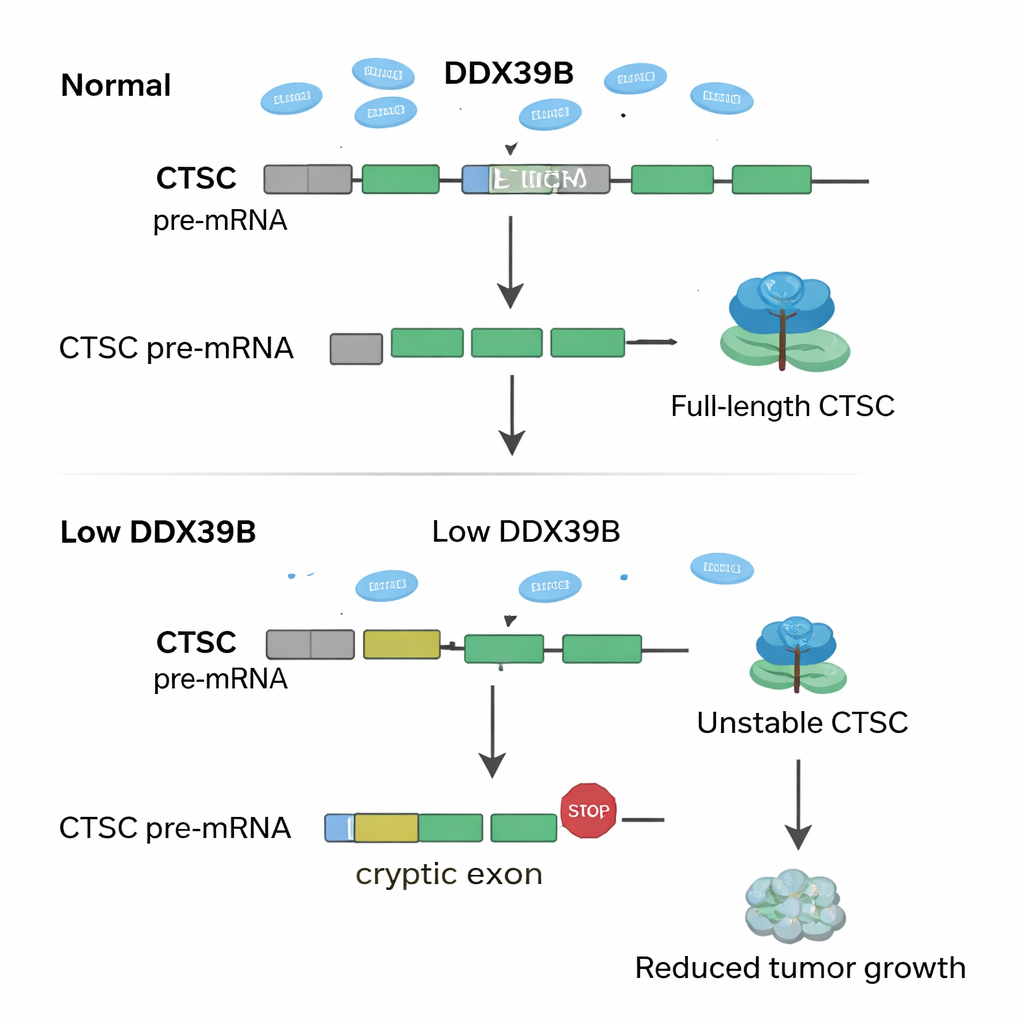
Wat dit betekent voor toekomstige behandelingen
Simpel gezegd onthullen de auteurs een relaisstelsel — SNRPD2 → DDX39B → CTSC — dat endometriumkankercellen exploiteren om te gedijen. Hoge SNRPD2 houdt DDX39B overvloedig; DDX39B voorkomt op zijn beurt dat CTSC schadelijke cryptische exonen gebruikt, waardoor volwaardige CTSC-eiwitten behouden blijven die tumoren helpen groeien en verspreiden. Wanneer SNRPD2 wordt geblokkeerd stort deze keten in, dalen de CTSC-niveaus en verzwakken tumoren. Voor niet-specialisten is het kernidee dat kankercellen afhankelijk zijn van zeer precieze RNA-bewerking, en zelfs kleine geforceerde “fouten” hun groei selectief kunnen vergiftigen. Het richten op SNRPD2 met antisensemiddelen, of het rechtstreeks forceren van cryptisch exongebruik in CTSC, zou nieuwe, meer op maat gemaakte therapieën voor patiënten met endometriumkanker kunnen bieden.
Bronvermelding: Li, Y., Chen, Z., Liu, Y. et al. SNRPD2-mediated regulation of DDX39B splicing promotes endometrial cancer progression by suppressing the activation of CTSC cryptic exons. Cell Death Dis 17, 239 (2026). https://doi.org/10.1038/s41419-026-08489-4
Trefwoorden: endometriumkanker, RNA-splicing, SNRPD2, DDX39B, CTSC