Clear Sky Science · nl
DNMT2 remt de progressie van anaplastisch schildklierkanker door de productie van 5’tiRNAGly-GCC te verlagen
Waarom deze verborgen RNA-chemie ertoe doet
Anaplastisch schildklierkanker is een van de dodelijkste vormen van kanker bij mensen en veroorzaakt vaak de dood binnen enkele maanden, ondanks chirurgie, bestraling en chemotherapie. Deze studie onthult een verrassende boosdoener diep in kankercellen: kleine chemische markeringen op transfer-RNA, de moleculen die helpen bij de eiwitsynthese. De auteurs tonen aan dat wanneer een bepaald enzym, DNMT2, verloren raakt of verminderd is, schildkliertumoren sneller groeien, gemakkelijker uitzaaien en resistenter worden tegen het veelgebruikte chemotherapie middel doxorubicine. Nog intrigerender is dat ze een klein RNA-fragment identificeren dat ontstaat wanneer DNMT2 laag is en aantonen dat het blokkeren van dit fragment een nieuwe behandelingsstrategie zou kunnen worden.
Een beschermend enzym dat verdwijnt
Transfer-RNA’s (tRNA’s) vervoeren normaal gesproken aminozuren naar het eiwitproducerende moleculaire machinerie van de cel, en hun stabiliteit hangt af van tere chemische versieringen. DNMT2 is een enzym dat zo’n markering toevoegt, een methylgroep, op specifieke plaatsen op tRNA. In veel kankers is DNMT2 verhoogd en werd gedacht dat dit tumoren helpt, maar hier is het tegenovergestelde het geval. Door grote patiëntendatasets en tumormonsters te analyseren, vonden de onderzoekers dat DNMT2-niveaus significant lager zijn in anaplastisch schildklierkankerweefsel dan in normaal schildklierweefsel. Patiënten wier tumoren meer DNMT2 hadden, leefden doorgaans langer zonder dat hun kanker verslechterde, wat suggereert dat DNMT2 in deze ziekte meer als een rem dan als een versneller functioneert.
Hoe laag DNMT2 agressief gedrag voedt
Om te zien wat DNMT2 daadwerkelijk doet in kankercellen, manipuleerde het team de niveaus ervan in anaplastische schildklierkankercellijnen gekweekt in schalen en in muismodellen. Wanneer DNMT2 werd verminderd, vermenigvuldigden de cellen zich sneller, drongen ze gemakkelijker door membranen en vormden ze meer kolonies — allemaal kenmerken van een agressieve tumor. Deze cellen werden ook minder gevoelig voor doxorubicine, een standaardmedicijn voor deze kanker. In muizen groeiden tumoren met minder DNMT2 groter en zaaiden ze gemakkelijker naar de longen, terwijl het verhogen van DNMT2-expressie het tegenovergestelde effect had. De onderzoekers herleidden deze veranderingen deels tot activering van een cellulair programma dat bekendstaat als epitheel–mesenchymale transitie, dat kankercellen beweeglijker en invasiever maakt.
Van beschadigd tRNA tot schadelijke kleine fragmenten
Dieper graven liet zien dat DNMT2 een methylmerk plaatst op een specifieke positie (genoemd C38) op slechts drie typen tRNA. Zonder deze bescherming worden de tRNA’s kwetsbaarder voor knippen door een ander enzym, angiogenine. Die knip produceert een kort RNA-stuk afgeleid van tRNA-Gly-GCC, aangeduid als 5’tiRNAGly-GCC. Met sequencing- en biochemische testen vonden de auteurs dat wanneer DNMT2 laag is, dit fragment zich ophoopt, vooral afkomstig van het glycine-transporterende tRNA. In proefbuisexperimenten beschermde het toevoegen van de methylmarkering het tRNA sterk tegen doorsnijden, wat bevestigt dat DNMT2 deze moleculen normaal bewaakt tegen het versnipperen tot kleinere, potentieel schadelijke stukjes.
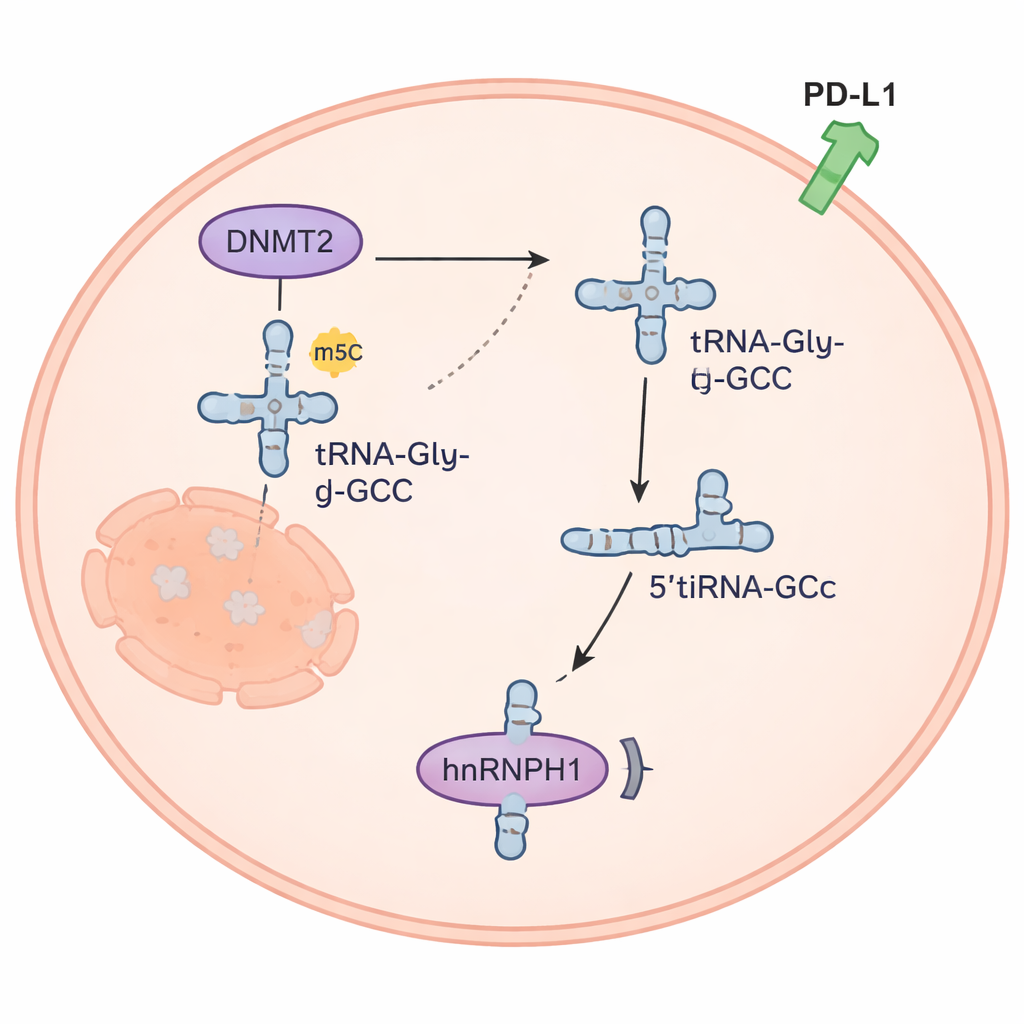
Een piepklein RNA-fragment herprogrammeert kankersignalen
Het 5’tiRNAGly-GCC-fragment bleek meer te zijn dan moleculair puin. Het kwam overvloedig voor in anaplastische schildklierkankercellen maar schaars in normale schildkliercellen. Wanneer de onderzoekers het kunstmatig opvoerden, deelden kankercellen zich sneller, drongen ze meer binnen en werden ze resistenter tegen doxorubicine; het verlagen van het fragment had het tegengestelde effect. In muizen vertraagde een chemisch ontworpen remmer van 5’tiRNAGly-GCC de tumor groei, en de combinatie van deze remmer met doxorubicine werkte nog beter dan één van beide behandelingen afzonderlijk. Het team ontdekte dat 5’tiRNAGly-GCC bindt aan een eiwit genaamd hnRNPH1, waardoor de hoeveelheid daarvan in cellen afneemt. Omdat hnRNPH1 normaal helpt de niveaus van het immuungerelateerde eiwit PD-L1 onder controle te houden, leidt het verlies van hnRNPH1 tot een stijging van PD-L1 — een verandering die tumoren kan helpen aan immuunaanvallen te ontsnappen en samenhangt met ophoping van regulerende T-cellen rond tumoren.
Wat dit betekent voor toekomstige behandelingen
In eenvoudige bewoordingen onthult de studie een kettingreactie: wanneer DNMT2 laag is, verliezen bepaalde tRNA’s een beschermend merk, worden ze in kleine fragmenten geknipt, en één van die fragmenten (5’tiRNAGly-GCC) schakelt een eiwit uit dat PD-L1 onderdrukt. Het resultaat is een agressievere, medicijnresistente en immuunontwijkende kanker. In plaats van te proberen DNMT2 direct te verhogen — wat in andere weefsels riskant kan zijn — stellen de auteurs voor het schadelijke RNA-fragment zelf te richten. Hun muisexperimenten met een 5’tiRNAGly-GCC-remmer, vooral gecombineerd met doxorubicine, leveren vroege aanwijzingen dat het onderbreken van dit microscopische RNA-circuit mogelijk kan helpen één van de dodelijkste vormen van schildklierkanker te temmen.
Bronvermelding: Zhou, R., Li, B., Cao, M. et al. DNMT2 inhibits anaplastic thyroid cancer progression by downregulating 5’tiRNAGly-GCC production. Cell Death Dis 17, 240 (2026). https://doi.org/10.1038/s41419-026-08488-5
Trefwoorden: anaplastisch schildklierkanker, DNMT2, tRNA-fragmenten, chemoresistentie, PD-L1