Clear Sky Science · nl
HIF2α-geïnduceerde lysyl oxidase beschermt een succesvolle zwangerschap door collageen te herbouwen aan de foeto-maternale grens
Waarom de baarmoeder zich moet voorbereiden op een nieuw leven
Voordat een zwangerschap kan standhouden, moet een vroeg embryo iets bijzonders doen: zich ingraven in de wand van de baarmoeder en een levensondersteunend systeem opbouwen, de placenta. Dit artikel onderzoekt hoe het moederweefsel zich geruisloos herschikt om het embryo te verwelkomen, met aandacht voor hoe lage zuurstofniveaus en een weinig bekend enzym het baarmoederslijmvlies klaarstomen. Inzicht in deze fijn afgestemde wisselwerking kan verklaren waarom sommige zwangerschappen zeer vroeg mislukken en nieuwe wegen aanwijzen om onvruchtbaarheid en zwangerschapscomplicaties te voorkomen.
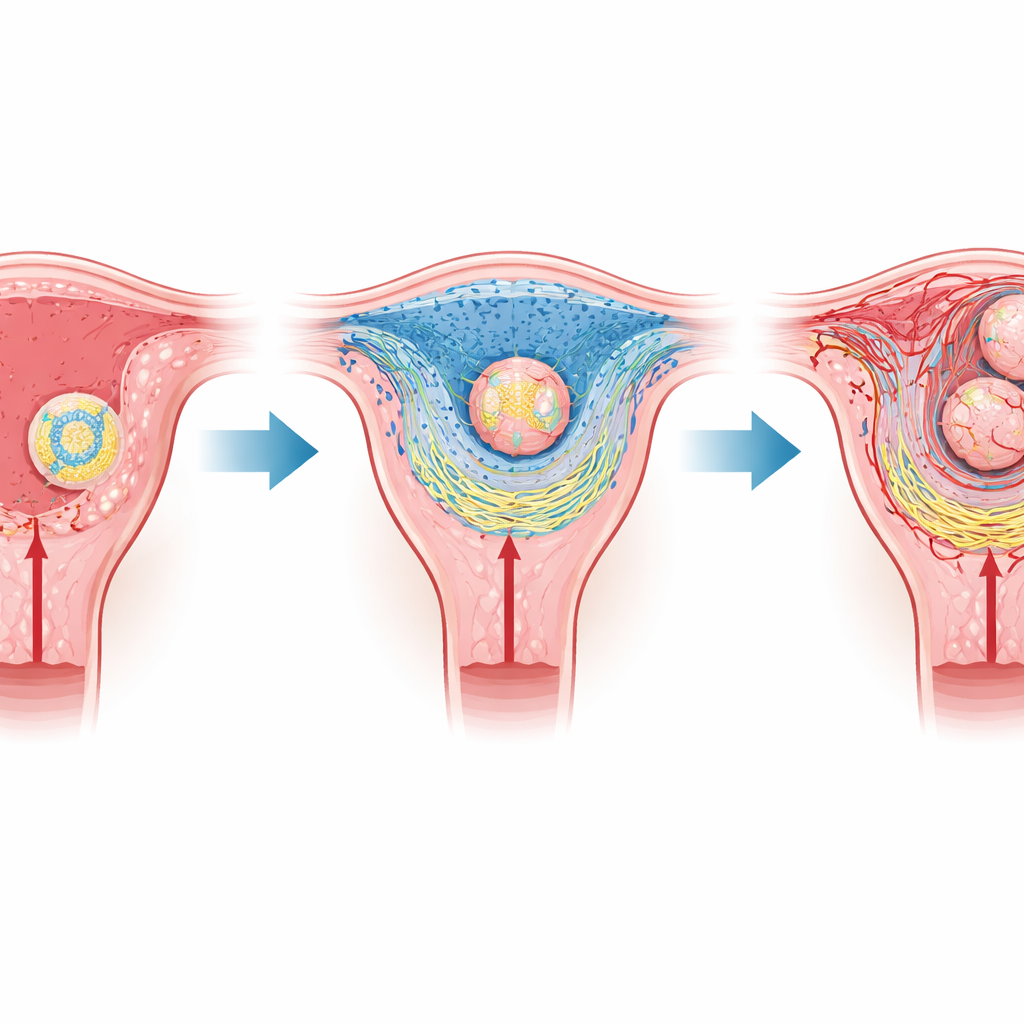
Een kwetsbare ontmoeting tussen moeder en embryo
Bij zoogdieren zoals muizen en mensen draait de vroegste fase van de zwangerschap om implantatie, wanneer het embryo zich aanhecht aan en vervolgens het baarmoederslijmvlies binnendringt. Het embryo is omgeven door een laag gespecialiseerde cellen die later de placenta zullen vormen, terwijl het moederweefsel transformeert tot een kussentjesachtige laag, het decidua. Dicht bij het embryo ligt een dunne zone die de primaire deciduale zone wordt genoemd; die bevat geen bloedvaten en heeft daardoor weinig zuurstof. Eerder werk toonde aan dat dit vanzelf lage-zuurstofgebied helpt om de implantatie te triggeren, maar hoe zo’n eenvoudige fysieke toestand hele weefsels kan herorganisatie ren, was nog niet goed begrepen.
Lage zuurstof als een verborgen schakelaar
De auteurs gebruikten een krachtige techniek, ruimtelijke transcriptomica, die genactiviteit direct in weefselslices in kaart brengt, om muizenbaarmoeders te bestuderen tijdens de dagen waarin embryo’s zich hechten en binnendringen. Ze concentreerden zich op een eiwit genaamd HIF2α, dat wordt geactiveerd bij lage zuurstof en als een genetische schakelaar fungeert. Bij normale muizen toonden cellen in de primaire deciduale zone sterke activiteit van genen gerelateerd aan hypoxie en aan de aanleg van het omringende skeletmateriaal, waaronder collageen dat de extracellulaire matrix vormt. Toen HIF2α alleen uit de baarmoeder werd verwijderd, leek de algemene verdeling van celtypen verrassend normaal. Maar bij hoge resolutie bleek het collageennetwerk gedesorganiseerd, opende het epitheliale oppervlak zich niet goed en hadden embryonale cellen moeite om het moederweefsel te penetreren.
Een enzym dat het skelet verbindt
Dieper gravend identificeerde het team een sleutelspeler stroomafwaarts van HIF2α: lysyl oxidase, of Lox, een enzym dat collageenvezels chemisch met elkaar verbindt en helpt weefsel te verstevigen en te stabiliseren. Bij normale zwangerschappen stegen de Lox-niveaus scherp rond de embryo’s precies op het moment dat ze begonnen binnen te dringen. In baarmoeders zonder HIF2α viel de Lox-expressie terug en leken collageenvezels gefragmenteerd in plaats van een dicht netwerk te vormen. Om het belang van Lox rechtstreeks te testen, maakten de onderzoekers muizen waarin Lox alleen in de baarmoeder werd uitgeschakeld. Deze vrouwtjes raakten minder vaak drachtig, droegen minder embryo’s en vertoonden vaak tekenen van embryoverlies en bloedingen later in de zwangerschap, hoewel de vroegste stappen van aanhechting en weefselverdikking aanvankelijk normaal leken.
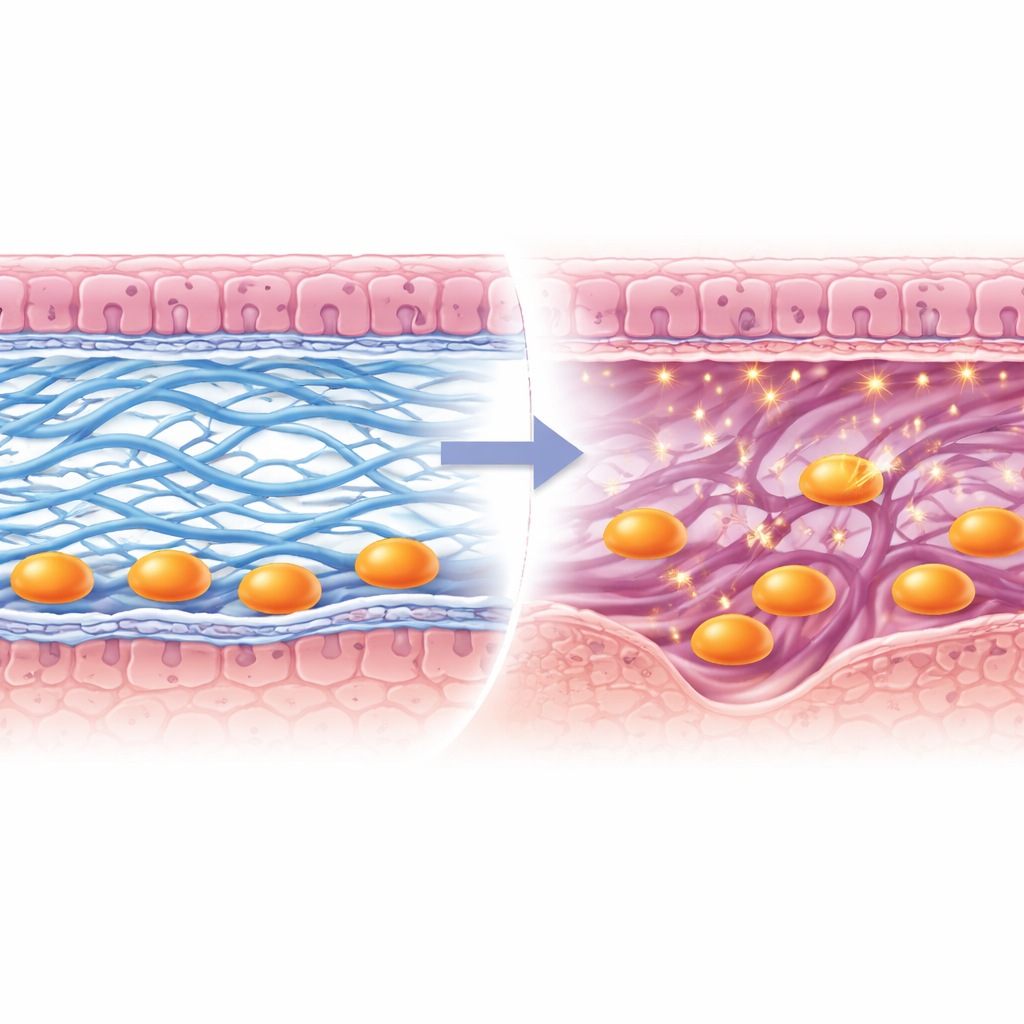
Een pad openen voor de placenta
Gedetailleerde beeldvorming liet zien wat er misging wanneer Lox ontbrak. Een dun eiwitrijk blad, het basaalmembraan, dat normaal afbreekt om embryonale cellen door te laten, bleef grotendeels intact. Collageen type I-vezels in het onderliggende stroma vormden geen robuuste, continue bundels, terwijl collageen type IV in het basaalmembraan niet adequaat werd geruimd nabij binnendringende cellen. Hierdoor bleven trofoblastcellen—de door het embryo afkomstige pioniers die de placenta bouwen—gevangen aan het oppervlak in plaats van zich een weg te banen in de moederlaag. Het team vond ook dat een collageensnijdend enzym, Mmp9, in deze trofoblasten niet werd geactiveerd, wat hun voortgang verder belemmerde. In de loop van de tijd ontwikkelden de placentale structuren zich slecht, groeiden embryo’s abnormaal en daalde de kans op een succesvolle zwangerschap.
Wat dit betekent voor zwangerschapsgezondheid
Samengevat schetsen de bevindingen een keten van gebeurtenissen waarin lage zuurstof in de vroege implantatiezone HIF2α activeert, dat op zijn beurt Lox verhoogt. Lox herschikt en verknopt vervolgens collageenvezels en helpt het basaalmembraan af te breken, terwijl het ook enzymen zoals Mmp9 mogelijk maakt een pad schoon te maken. Deze remodellering biedt zowel een structureel skelet als een open doorgang voor trofoblastcellen om binnen te dringen en de placenta op te bouwen. Voor een geïnteresseerde lezer is de kernboodschap dat een succesvolle zwangerschap niet alleen afhangt van gezonde embryo’s en hormonen, maar ook van het stille herinrichten van de weefselaanpak van de moeder. Verstoring van deze hypoxie–HIF2α–Lox-route kan ten grondslag liggen aan sommige gevallen van onverklaarde onvruchtbaarheid, miskraam en aandoeningen geassocieerd met slechte placentainvasie, en suggereert nieuwe diagnostische markers en therapeutische doelwitten om vroege zwangerschap te ondersteunen.
Bronvermelding: Aikawa, S., Shimizu-Hirota, R., Sakashita, A. et al. HIF2α-induced lysyl oxidase safeguards successful pregnancy by remodelling collagens at the feto-maternal interface. Cell Death Dis 17, 250 (2026). https://doi.org/10.1038/s41419-026-08485-8
Trefwoorden: embryo-implantatie, uteriene extracellulaire matrix, lysyl oxidase, trofoblastinvasie, placentale ontwikkeling