Clear Sky Science · nl
Richten op mitochondriale fosfatase PGAM5 verlicht ferroptose en acute pancreatitis door NRF2-gemedieerde FSP1-expressie te verhogen
Waarom gestreste cellen en pijnlijke alvleesklieren ertoe doen
Wanneer cellen te hard worden belast, kunnen ze op manieren afsterven die het hele lichaam schaden. Een dergelijke vorm van celdood, ferroptose genoemd, wordt aangedreven door ijzer en uit de hand lopende chemische reacties die de vetten in celmembranen oxideren. Dit proces is in verband gebracht met orgaanschade, waaronder een pijnlijke en soms dodelijke aandoening die acute pancreatitis wordt genoemd. De studie achter dit artikel onthult een belangrijke schakel binnen de mitochondriën — de energiecentrales van de cel — die ferroptose kan aan- of uitzetten, en toont aan hoe het blokkeren van deze schakel de alvleesklier in een muismodel kan beschermen.
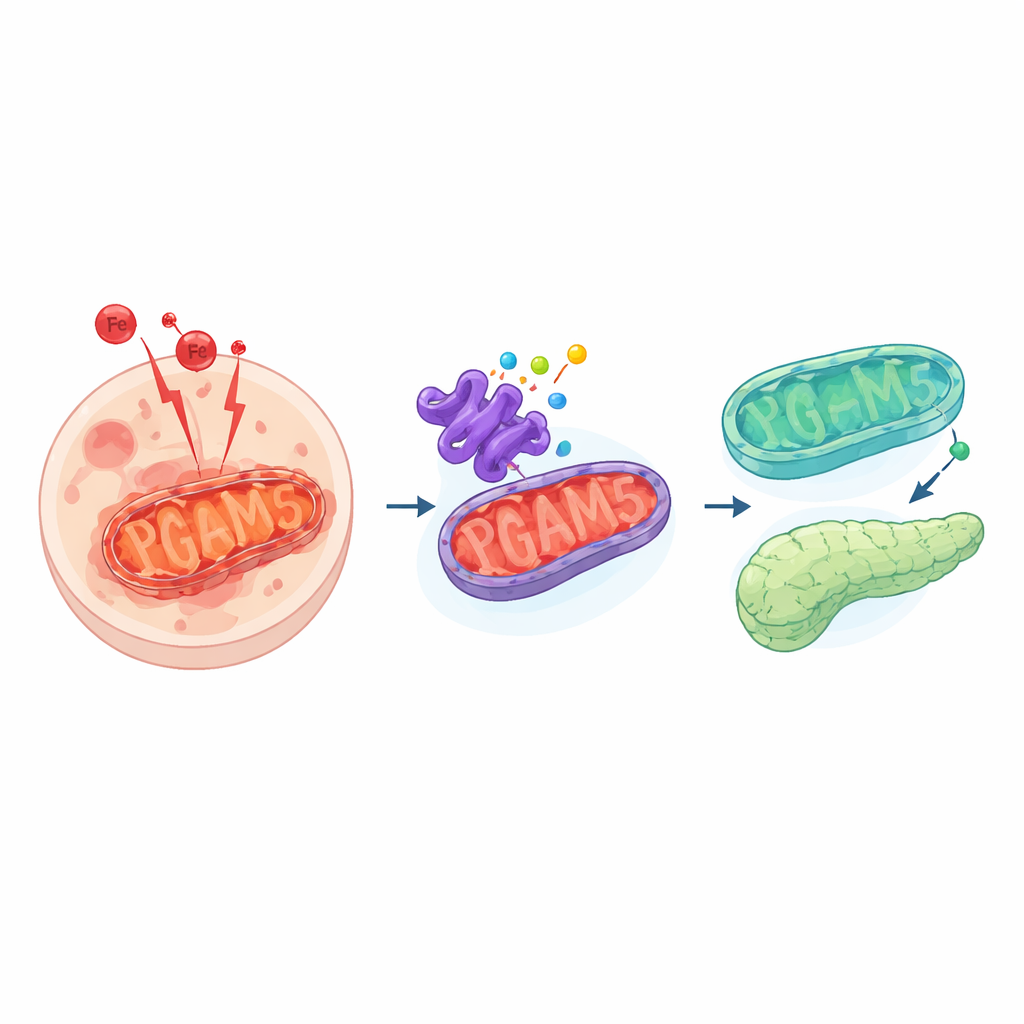
Een gevaarlijke vorm van celdood
Ferroptose verschilt van meer bekende vormen van celdood zoals apoptose. In plaats van een nette zelfvernietiging ondergaan cellen bij ferroptose een storm van ijzer-gedreven reacties die kwetsbare vetten in hun membranen laten oxideren. Dit creëert toxische bijproducten en gaten in membranen die de cel uiteindelijk doden. Gewoonlijk houden cellen dit onder controle met beschermende systemen die deze reactieve moleculen ontgiften. Wanneer die systemen falen of overweldigd raken, kan ferroptose schade door weefsels heen verspreiden en bijdragen aan ziekten variërend van kanker tot orgaanfalen.
Een mitochondriale schakel in het vizier
De onderzoekers richtten zich op een eiwit genaamd PGAM5, dat aan de binnenzijde van mitochondriën zit en fungeert als een signaalhub. PGAM5 helpt de mitochondriale vorm te reguleren, reageert op stress en beïnvloedt hoe cellen omgaan met oxidatie. Verrassend genoeg werden de cellen, wanneer het team PGAM5 ofwel verminderde of juist meer van het eiwit liet produceren, moeilijker te doden door ferroptose. Chemische remming van PGAM5, genetische knockdown en overexpressie verminderden allemaal de ophoping van schadelijke lipidebijproducten en beperkten celdood veroorzaakt door een ferroptose-inducerend middel. Dit toonde aan dat het systeem precies is afgesteld: zowel te weinig als te veel PGAM5 duwen cellen naar een meer beschermde toestand.
Het inschakelen van een inwendige schild
Verder onderzoek toonde aan dat de invloed van PGAM5 verloopt via een beschermende as met twee andere spelers: NRF2 en FSP1. NRF2 is een hoofdregelaar die, wanneer actief in de kern, een breed scala aan antioxidantverdedigingen inschakelt. FSP1 is een van zijn downstream verdedigingsmiddelen die helpt een vetoplosbaar antioxidant te regenereren en zo lipoïdodatie aan het celmembraan voorkomt. Wanneer PGAM5-niveaus werden gewijzigd, verhoogden cellen zowel het boodschapper-RNA als het proteïnegehalte van NRF2, en NRF2 bewoog makkelijker van het cytoplasma naar de kern. Daar verhoogde het de productie van FSP1. Het blokkeren van FSP1 of NRF2 maakte de bescherming ongedaan en herstelde de gevoeligheid voor ferroptose, wat laat zien dat deze PGAM5–NRF2–FSP1-keten essentieel is voor de waargenomen weerbaarheid.
Energiestress als de verborgen boodschapper
De studie onthulde ook hoe mitochondriale stress in deze beschermende respons wordt vertaald. Het verstoren van PGAM5 verstoorde de mitochondriale balans en verschuift de energiestatus van de cel: de verhouding van lagere-energie moleculen (AMP en ADP) tot hoogenergetisch ATP steeg, wat een signaal voor energiestress afgeeft. Dit activeerde op zijn beurt het energie-sensorenzym AMPK. Geactiveerde AMPK modificeerde NRF2 direct op een manier die zijn binnenkomst in de kern bevorderde, waardoor de FSP1-productie verder werd verhoogd. Wanneer AMPK uit het systeem werd verwijderd, stapelde NRF2 zich niet langer in de kern op, vielen FSP1-niveaus terug en gaven cellen opnieuw toe aan ferroptose. Zo verbindt PGAM5 de mitochondriale toestand met een bredere energie- en antioxidantrespons die cellen beschermt tegen ijzer-gedreven celdood.
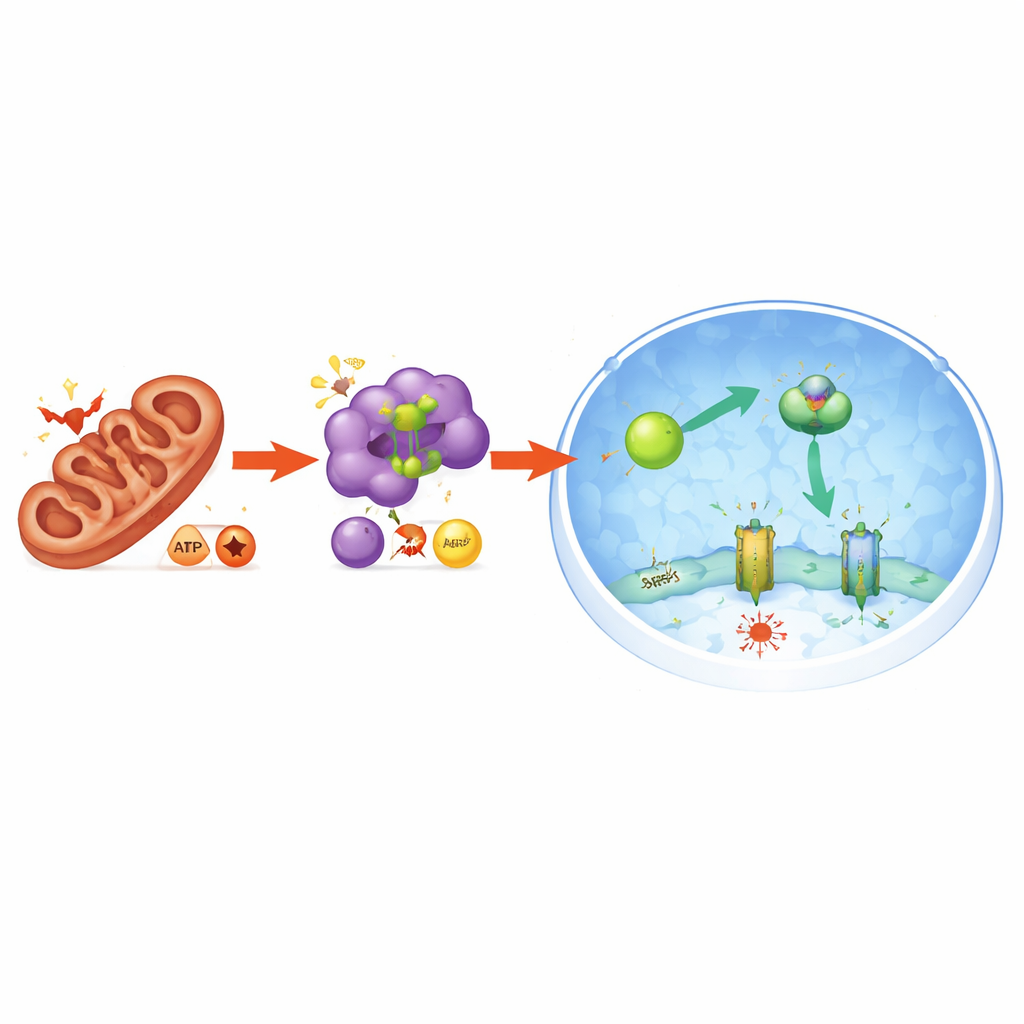
De alvleesklier beschermen in levende dieren
Om te testen of dit mechanisme van belang is in een heel orgaan, gebruikten de wetenschappers een muismodel van acute pancreatitis dat wordt opgewekt door hoge doses van het aminozuur arginine. In dit model vertoont de alvleesklier uitgebreide schade, verhoogde niveaus van bloedenzymen die weefselschade aangeven, en een toename van ontstekingsmoleculen. Markers van lipideperoxidatie — een kenmerk van ferroptose — stegen ook scherp in de alvleesklier. Het behandelen van muizen met een PGAM5-remmend middel verlichtte deze symptomen: de bloedmarkers van schade daalden, het pancreatisch weefsel zag er onder de microscoop gezonder uit en ontstekingssignalen namen af. Tegelijkertijd vielen de ferroptose-markers terug, terwijl AMPK-activiteit, NRF2 en FSP1-niveaus in de alvleesklier toenamen, overeenkomend met de beschermende route die in kweekcellen werd gezien.
Wat dit betekent voor toekomstige behandelingen
Samengevat identificeert het werk PGAM5 als een centraal controlepunt dat mitochondriale stress, de energiestatus van de cel en een krachtig antioxidantprogramma koppelt dat ferroptose blokkeert. Door de activiteit van PGAM5 terug te draaien, activeren cellen AMPK en NRF2, verhogen ze FSP1 en weerstaan ze beter ijzer-gedreven lipideschade. Bij muizen vermindert deze strategie pancreatische schade bij acute pancreatitis. Voor de algemene lezer is de boodschap dat onderzoekers een nieuw intern "stroomonderbreker" hebben gevonden die een destructieve vorm van celdood kan voorkomen. Hoewel er nog veel moet gebeuren voordat dit klinisch toepasbaar is, zou het richten op PGAM5 of zijn downstreampartners nieuwe wegen kunnen openen om aandoeningen te behandelen waarbij ferroptose en mitochondriale falen een schadelijke rol spelen.
Bronvermelding: Ma, S., Qin, J., Luan, J. et al. Targeting mitochondrial phosphatase PGAM5 alleviates ferroptosis and acute pancreatitis by upregulating NRF2-mediated FSP1 expression. Cell Death Dis 17, 252 (2026). https://doi.org/10.1038/s41419-026-08484-9
Trefwoorden: ferroptose, mitochondriën, acute pancreatitis, oxiderende stress, cecdood