Clear Sky Science · nl
UBE3A-gemedieerde ubiquitinatie van mH2A1 activeert TERT-transcriptie om weerstand tegen veroudering te bevorderen bij alvleesklierkanker
Waarom dit onderzoek belangrijk is voor patiënten
Alvleesklierkanker behoort tot de dodelijkste vormen van kanker, deels omdat tumorcellen uitzonderlijk goed zijn in het omzeilen van de ingebouwde verouderingsrem van het lichaam. Deze studie onthult een verborgen moleculair “sabotagecircuit” dat alvleesklierkankercellen helpt jong te blijven, te blijven delen en resistent te zijn tegen behandeling. Door dit circuit te begrijpen wijzen de onderzoekers op een nieuwe manier om deze cellen in veroudering te duwen en ze vervolgens selectief te verwijderen, wat de deur opent naar slimmere combinatietherapieën.
Veroudering als de natuurlijke tumorrem van het lichaam
Alle cellen dragen een interne klok die hen uiteindelijk doet stoppen met delen, een proces dat bekendstaat als senescentie. In vroege alvleesklierlaesies kan deze klok de tumorgroei vertragen door voorstadia van kankercellen permanent met pensioen te sturen. Veel kankerbehandelingen werken ook deels door tumorcellen naar deze verouderde toestand te dwingen. Als deze senescente cellen echter niet worden opgeruimd, kunnen ze ontsteking aanwakkeren en bijdragen aan terugkeer van de kanker. Dat heeft geleid tot een nieuw behandelidee: duw eerst kankercellen in senescentie en elimineer die verouderde cellen daarna met “senolytische” geneesmiddelen die speciaal toxisch voor hen zijn.
Een kankerbevorderend enzym in de schijnwerpers
Om genen te vinden die alvleesklierkankercellen helpen senescentie te weerstaan, doorzocht het team grote patiëntendatasets en valideerde hun bevindingen vervolgens in tumorstalen en kweeklijnen. Ze richtten zich op een eiwit genaamd UBE3A, een enzym dat andere eiwitten markeert voor afbraak. UBE3A-niveaus waren veel hoger in alvleeskliertumoren dan in aangrenzend normaal weefsel, en patiënten met meer UBE3A hadden doorgaans grotere, meer gevorderde tumoren en een slechtere overleving. In kweekcellen versnelde toegenomen UBE3A de groei, verminderde klassieke markers van cellulaire veroudering en verlaagde de ontstekingssecreties die typisch zijn voor senescente cellen. Het uitschakelen van UBE3A had het omgekeerde effect en verminderde in muismodellen scherp de tumorgroei en levermetastasen. 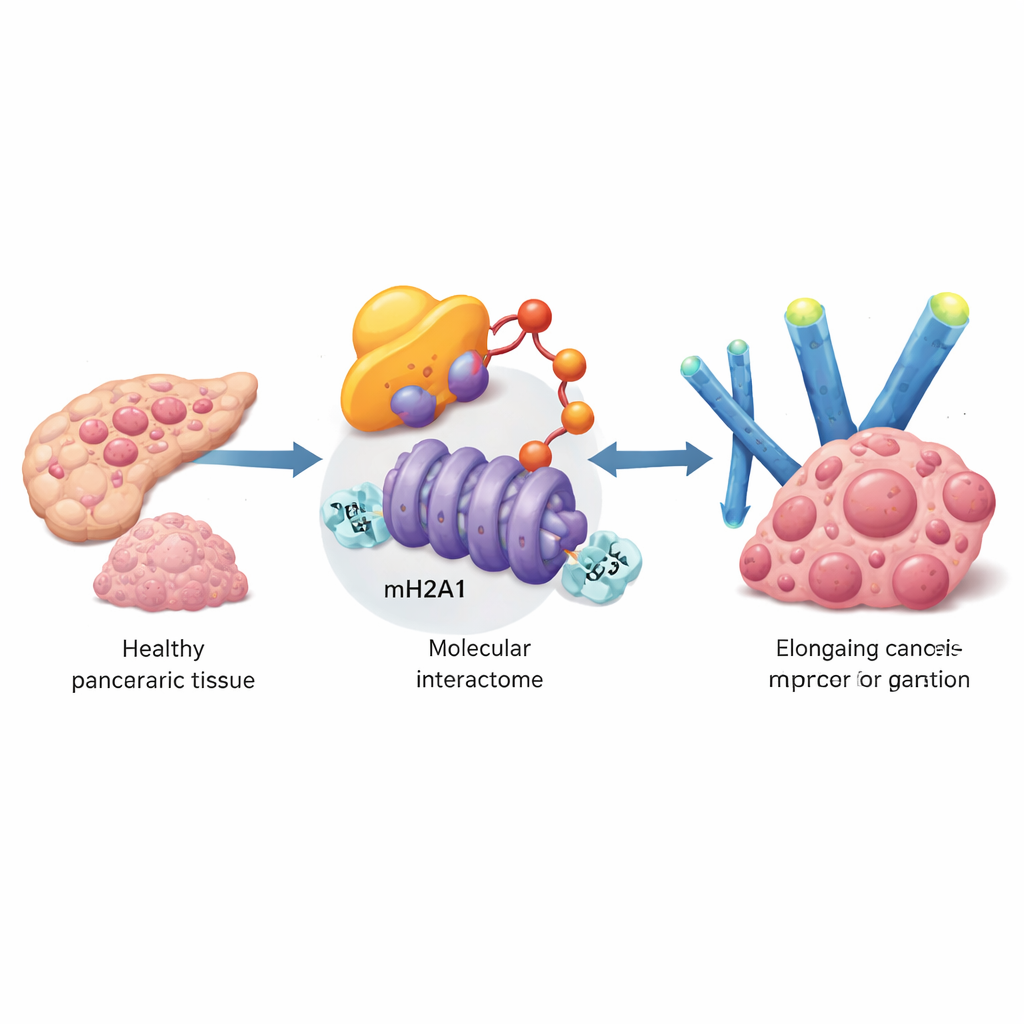
Hoe kankercellen een chromatinerem wissen
Dieper gravend onderzochten de onderzoekers welke moleculen UBE3A aanpakt. Met geavanceerde massaspectrometrieschermen vonden ze dat UBE3A bindt aan en chemisch markeert een speciaal histonvariant genaamd macroH2A1 (mH2A1), die helpt het DNA compact te houden en meestal fungeert als een rem op genactiviteit. UBE3A bevestigt een keten van “vernietig mij”-labels op mH2A1 op een specifieke plaats, waardoor het door het proteïneafbraakmechanisme van de cel wordt versnipperd. In alvleeskliertumoren waren de mH2A1-niveaus lager waar UBE3A hoog was, en het herstellen van mH2A1 keerde UBE3A’s vermogen om senescentie te blokkeren en tumorgroei te stimuleren teniet. Dit onthult een cruciale stap: alvleesklierkankercellen verwijderen een beschermend chromatinemerk door UBE3A te gebruiken om mH2A1 te elimineren.
Telomerase ontgrendelen om cellen jong te houden
De volgende vraag was welke genen vrijkomen wanneer mH2A1 wordt verwijderd. Door RNA-sequencing te combineren met kaarten van DNA-bindingsplaatsen identificeerde het team het telomerasegen TERT als een centraal doelwit. Telomerase onderhoudt de beschermende uiteinden van chromosomen, waardoor cellen kunnen blijven delen in plaats van senescent te worden. De studie toont aan dat mH2A1 normaal gesproken aanwezig is op een enhancerregio binnen het TERT-gen, waar het een ander enzym, EZH2, aantrekt om een repressief chemisch merkteken op nabijgelegen histonen aan te brengen. Deze combinatie houdt TERT onderdrukt en laat telomeren verkorten. Wanneer UBE3A mH2A1 vernietigt, valt het repressieve complex uiteen, wordt de enhancer actief, schakelt TERT aan, blijven telomeren behouden en verkrijgen alvleesklierkankercellen weerstand tegen veroudering. Mutante vormen van UBE3A die geen eiwitten kunnen markeren, of mutante mH2A1 die niet gemarkeerd kan worden, doorbreken dit circuit en herstellen de senescentierem.
Combinatie van senescentie-inductie met senolytische opruiming
Ten slotte testten de onderzoekers of deze route therapeutisch kan worden benut. Het stilleggen van UBE3A duwde alvleesklierkankercellen richting senescentie en vergrootte hun afhankelijkheid van anti-sterfte-eiwitten uit de BCL-2-familie — een bekende kwetsbaarheid van senescente cellen. Het team combineerde vervolgens UBE3A-remming met ABT-263, een senolytisch middel dat deze overlevingsproteïnen target. In gekweekte cellen zorgde de combinatie ervoor dat veel meer kankercellen geprogrammeerde celdood ondergingen dan bij één van beide behandelingen alleen. In muismodellen krompen tumoren met gereduceerde UBE3A nog verder toen dieren ABT-263 kregen, en markeringsstoffen voor celproliferatie in de tumoren daalden sterk. 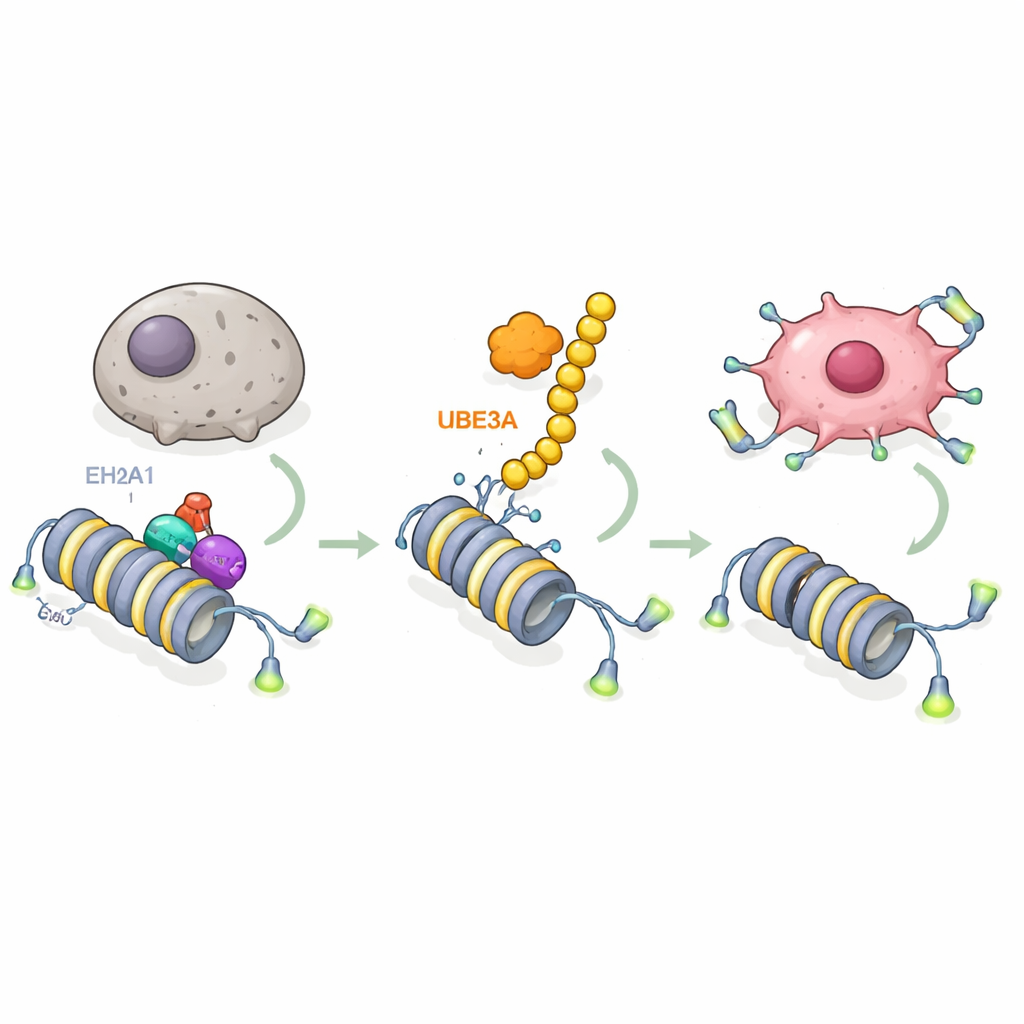
Wat dit betekent voor toekomstige behandeling
Dit werk onthult een gedetailleerde keten van gebeurtenissen waarmee alvleesklierkankercellen voorkomen dat ze oud worden: UBE3A vernietigt de chromatinerem mH2A1, wat op zijn beurt de repressie van het telomerasegen TERT opheft en helpt telomeren te behouden, zodat cellen blijven delen. Door UBE3A te richten, zouden artsen het natuurlijke verouderingsprogramma van de cel weer in kunnen schakelen en vervolgens senolytische geneesmiddelen zoals ABT-263 kunnen gebruiken om deze kwetsbare, verouderde kankercellen selectief te elimineren. Hoewel meer studies nodig zijn om dit mechanisme naar patiëntbehandelingen te vertalen, biedt de UBE3A–mH2A1–TERT-as een veelbelovend nieuw aanknopingspunt voor een van de meest therapieresistente vormen van kanker.
Bronvermelding: Ren, L., Lu, R., Fei, X. et al. UBE3A-mediated mH2A1 Ubiquitination activates TERT transcription to promote senescence resistance in pancreatic cancer. Cell Death Dis 17, 274 (2026). https://doi.org/10.1038/s41419-026-08480-z
Trefwoorden: alvleesklierkanker, cellulaire veroudering, telomerase, ubiquitine-ligase, senolytische therapie