Clear Sky Science · nl
Een kleine-molecuulremmer van ARF GTPase-eiwit 1 beperkt de groei en uitzaaiing van lever- en dikkedarmkankercellen
Waarom dit onderzoek ertoe doet
Lever- en dikkedarmkankers behoren tot de dodelijkste tumoren en bestaande behandelingen laten vaak tumoren krimpen ten koste van zware bijwerkingen. Deze studie onderzoekt een nieuw type middel dat niet simpelweg snelgroeiende cellen vergiftigt, maar in plaats daarvan in kankercellen binnendringt en een eiwitelijk “regelcentrum” uiteenrijt waarop die cellen vertrouwen om te groeien en zich te verspreiden. Door zich te richten op dat centrum probeert de experimentele verbinding de tumorgroei te vertragen terwijl gezond weefsel wordt gespaard.
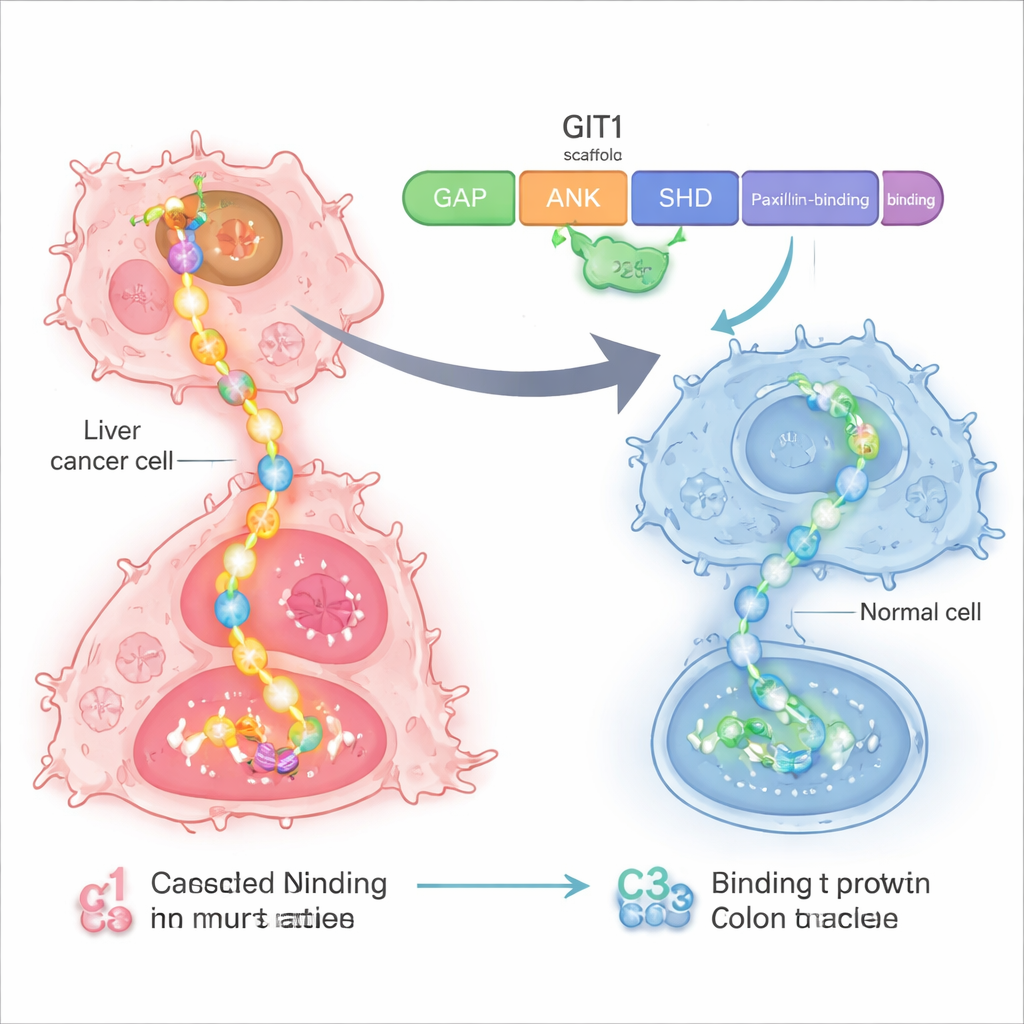
Een kwetsbaar regelcentrum in kankercellen
De onderzoekers concentreerden zich op een eiwit genaamd GIT1, dat fungeert als een scaffold of stroomverdeler binnen cellen. In lever- en dikkedarmkankers worden GIT1 en het partner-eiwit MAT2B te veel geproduceerd. Samen assembleren ze verschillende onderdelen van een belangrijk groeipad dat bekendstaat als RAS–RAF–MEK–ERK, een keten van signalen die cellen aanzet tot delen en migreren. Eerder werk toonde aan dat wanneer GIT1 en MAT2B in overvloed aanwezig zijn, lever- en dikkedarmtumoren sneller groeien en zich makkelijker verspreiden, en dat vermindering van deze eiwitten de kankergroei vertraagt. Dit maakte het GIT1–MAT2B-scaffold tot een aantrekkelijk doelwit voor een meer precieze therapie.
Een klein molecuul ontwerpen zonder blauwdruk
Een belangrijke uitdaging was dat de driedimensionale kristalstructuur van GIT1 niet beschikbaar is, dus het team kon de vorm van het eiwit niet eenvoudig ‘opzoeken’. In plaats daarvan gebruikten ze computermodellering om de structuur te voorspellen van een regio van GIT1 die bestaat uit ankyrinherhalingen, gelegen nabij waar MAT2B en andere signaaleiwitten zich hechten. Vervolgens screenden ze in silico een grote bibliotheek van kleine moleculen tegen dit model om te zien welke mogelijk aan dat gebied zouden binden. Van de negen kandidaten die in cellen werden getest, stak één molecuul — genoemd verbinding 3 (C3) — er bovenuit. C3 bond specifiek aan GIT1, maar niet aan zijn nauwe verwant GIT2, en verminderde de activiteit van het ERK-groepssignaal in meerdere kankercellijnen.
Kankercellen stoppen met delen en verspreiden
Wanneer lever- en dikkedarmkankercellen werden behandeld met C3, vertraagde hun groei en bij hogere doses overleden veel cellen, terwijl niet-kankercellen uit lever en nier grotendeels onaangetast bleven. C3 zorgde ervoor dat kankercellen stagneerden bij de grens tussen de G2- en M-fasen van de celcyclus, de controlepunt net voor en tijdens mitose wanneer een cel zich in twee deelt. De verbinding verminderde ook sterk het vermogen van kankercellen om kolonies te vormen en over een schaaltje te migreren — twee laboratoriummaten die verband houden met tumorhergroei en uitzaaiing. Op moleculair niveau verzwakte C3 de interacties tussen GIT1, MAT2B en de RAF–MEK–ERK-signaaleiwitten, wat leidde tot lagere MEK- en ERK-activiteit en minder van de celcyclusstimulator cycline D1.
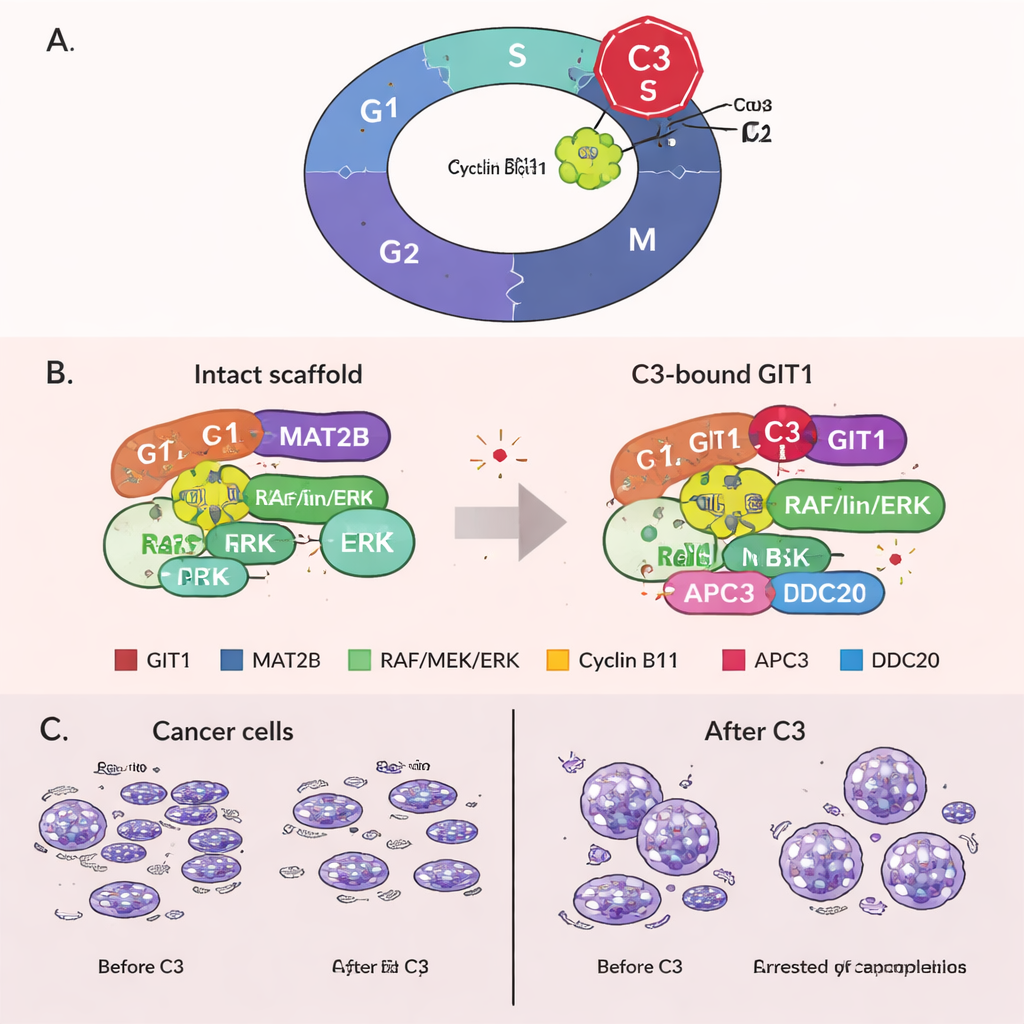
Cellen vergrendelen in mitose door een nieuw ontdekte rol van GIT1
Onverwacht ontdekten de onderzoekers een nieuwe rol voor GIT1 in de laatste stappen van de celdeling. Ze vonden dat GIT1 bindt aan cycline B1, een eiwit dat cellen helpt de mitose in te gaan, en ook aan onderdelen van een eiwitmachine genaamd het anafase-promoterend complex (APC/C), die normaal gesproken cycline B1 markeert voor afbraak zodat cellen de mitose kunnen verlaten. Behandeling met C3 versterkte de verbinding tussen GIT1 en cycline B1 maar verzwakte de verbindingen tussen GIT1, cycline B1 en APC/C-componenten. Als gevolg werd cycline B1 niet langer efficiënt afgebroken, bleef het op een hoog niveau en raakten cellen vast in de mitose. Dit verlengde arrest is bekend als een trigger voor celdood en biedt een tweede manier waarop C3 kankercellen kan doden. Belangrijk is dat wanneer GIT1 experimenteel werd verminderd, C3 veel van zijn vermogen verloor om cycline B1 te verhogen, de celcyclus te blokkeren en groei te onderdrukken, wat aantoont dat de effecten echt GIT1-afhankelijk zijn.
Veelbelovende resultaten in diermodellen
De onderzoekers gingen vervolgens naar muismodellen om te onderzoeken of C3 in levende organismen zou werken. In immuuncompetente muizen met geïmplanteerde colorectale tumoren vertraagden injecties van C3 direct in de tumoren de groei sterk zonder duidelijke toxiciteit voor belangrijke organen. In twee aanvullende modellen — humane dikkedarmkankercellen die in de lever van immuundeficiënte muizen groeiden, en muizendikkedarmkankercellen die in immuuncompetente muizen naar de lever waren uitgezaaid — verminderde C3 gegeven via intraperitoneale injectie de tumorlast en tekenen van uitzaaiing. Bloedtesten en weefselonderzoeken suggereerden dat de behandelingen goed werden verdragen, en farmacokinetische studies toonden aan dat de medicijnniveaus in het bloed enkele uren na toediening hoog genoeg bleven.
Wat dit kan betekenen voor toekomstige kankerbehandelingen
Voor niet-specialisten is de kernboodschap dat de onderzoekers een manier hebben gevonden om kanker aan te pakken, niet door een enkel gemuteerd enzym te richten, maar door een multi-eiwitassemblage te verstoren waarop kankercellen vertrouwen voor zowel groeisignalen als correcte celdeling. Hun kleine molecuul, C3, bindt specifiek aan GIT1, herschikt zijn netwerk van partners, dempt een belangrijk groeipad en houdt kankercellen gevangen in een dodelijke opstopping tijdens de mitose. Hoewel C3 nog een experimenteel onderzoeksinstrument is en nog geen medicijn voor patiënten, toont het werk aan dat het richten op scaffold-eiwitten zoals GIT1 een nieuw pad kan openen voor de behandeling van lever- en dikkedarmkankers met grotere precisie en mogelijk minder bijwerkingen.
Bronvermelding: Peng, H., Chhimwal, J., Fan, W. et al. A small molecule inhibitor of ARF GTPase protein 1 limits liver and colon cancer cell growth and metastasis. Cell Death Dis 17, 238 (2026). https://doi.org/10.1038/s41419-026-08477-8
Trefwoorden: leverkanker, dikkedarmkanker, gerichte therapie, celcyclusarrest, steunproteïne