Clear Sky Science · nl
Het lot van melanoomacellen herschakelen: TRPM8-modulatoren veroorzaken apoptose en versterken NK-celcytotoxiciteit
Waarom het “koude‑sensor” tegen huidkanker keren belangrijk is
Melanoom is een gevaarlijke vorm van huidkanker die vaak leert zowel medicijnen als het immuunsysteem te ontwijken. Deze studie onderzoekt een onverwachte kwetsbaarheid in melanoomacellen: een eiwit genaamd TRPM8, vooral bekend als de sensor die zenuwcellen koud of menthol laat waarnemen. De onderzoekers tonen aan dat zorgvuldig ontworpen geneesmiddelen die TRPM8 blokkeren melanoomacellen kunnen dwingen zichzelf te vernietigen en ze tegelijkertijd makkelijker herkenbaar maken voor natural killer‑(NK) immuuncellen. Deze dubbele werking wijst op een nieuwe benadering om hardnekkig, gevorderd melanoom te behandelen.
Een verborgen schakelaar op melanoomacellen
Door grote kankerdatabases te doorzoeken en melanoomacellen van patiënten in het laboratorium te bestuderen, vond het team dat TRPM8 veel overvloediger is in metastatisch melanoom dan in normale huid, inclusief gezonde melanocyten en dermale fibroblasten. Met beeldvorming lieten ze zien dat TRPM8 zowel aan het celoppervlak als op interne membranen zit, waardoor het op strategische plaatsen staat om celgedrag te beïnvloeden. Toen ze een reeks nieuwe TRPM8‑gerichte moleculen toepasten, staken twee verbindingen (genoemd 4 en 9) consequent bovenuit: ze verminderden de overleving van melanoomacellen sterk in de tijd terwijl normale huidcellen grotendeels onaangetast bleven. Genetische tests bevestigden dat wanneer TRPM8 werd verwijderd, deze middelen hun dodelijke werking verloren, en wanneer TRPM8 werd verhoogd, melanoomacellen nog gevoeliger werden, wat bewijst dat het effect afhankelijk is van dit specifieke kanaal. 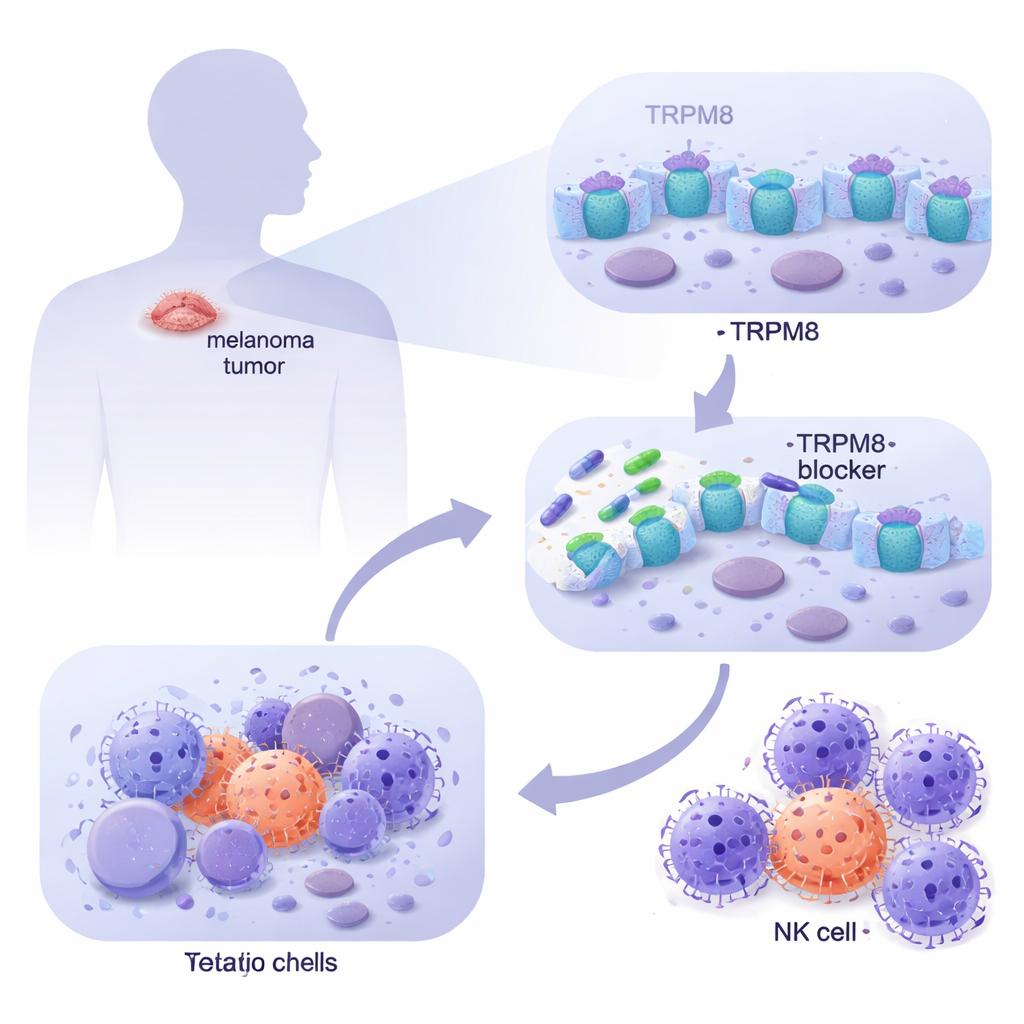
Kankercellen in een energiecrisis dwingen
In tegenstelling tot klassieke TRPM8‑activatoren zoals menthol, die een toestroom van calcium in cellen veroorzaken, gaven deze nieuwe blokkers geen calciumveranderingen. In plaats daarvan veroorzaakten ze een golf van oxidatieve stress in melanoomacellen. De verbindingen verhoogden snel reactieve zuurstofsoorten, met name in mitochondriën, de energiecentrales van de cel. Deze oxidatieve uitbarsting deed de mitochondriën hun elektrische lading verliezen, fragmenteren en cytochroom c lekken—een cruciale stap in het activeren van het interne “zelfmoord”‑programma van de cel. Anti‑oxidanten die deze reactieve moleculen opvingen, redden de cellen grotendeels, wat laat zien dat de redox‑verstoring geen bijverschijnsel is maar de motor van celdood. Standaard markers van celdood zoals caspase‑3‑activatie en PARP‑splitsing bevestigden verder dat de cellen geprogrammeerde apoptose ondergingen in plaats van willekeurige schade.
Overlevingssignalen uitschakelen en een bewaker wekken
De oxidatieve klap zette een bredere stressreactie in gang. De middelen activeerden ATM, een sensor van DNA‑schade, en leidden tot de ophoping en activatie van p53, een bekende tumorrepressor die beslist of een beschadigde cel zichzelf repareert of sterft. Tegelijk verzwakten de verbindingen een van de belangrijkste overlevingsroutes van melanoom: de PI3K–AKT‑route. Normaal gesproken interageert TRPM8 fysiek met PI3K‑componenten om AKT in zijn actieve, groei‑bevorderende vorm te houden. Na behandeling viel deze samenwerking uiteen en nam de AKT‑activiteit af, waardoor de balans verder naar celdood kantelde. Belangrijk is dat deze veranderingen uitgesproken waren in melanoomacellen maar niet in niet‑kankercellen, wat wijst op een therapeutisch venster waarin de tumor hard wordt getroffen terwijl gezond weefsel gespaard blijft.
Tumoren zichtbaarder maken voor immuun “aanvalsploegen”
Het gevaar van melanoom zit ook in zijn talent om aan immuuncontrole te ontsnappen. De onderzoekers vroegen daarom wat er gebeurt met tumorcellen die lage doses van de TRPM8‑blokkers over langere perioden overleven. Ze ontdekten dat deze achterblijvende cellen meer van een oppervlaktevlaggetje genaamd ULBP1 begonnen te tonen, dat fungeert als een noodsignaal dat herkend wordt door NKG2D‑receptoren op NK‑cellen. Andere verwante signalen veranderden niet, wat wijst op een selectief effect. In driedimensionale melanoom‑sferoïden die echte tumoren beter nabootsen, verminderde voorafbehandeling met TRPM8‑blokkers niet alleen de structuren en verhoogde de celdood, maar maakte ze ook veel kwetsbaarder voor NK‑celaanvallen. Wanneer ULBP1 of NKG2D met antilichamen werd geblokkeerd, verdween deze extra killing grotendeels, wat aantoont dat de verbeterde immuunclearing via deze specifieke handdruk tussen tumor en NK‑cellen verloopt. 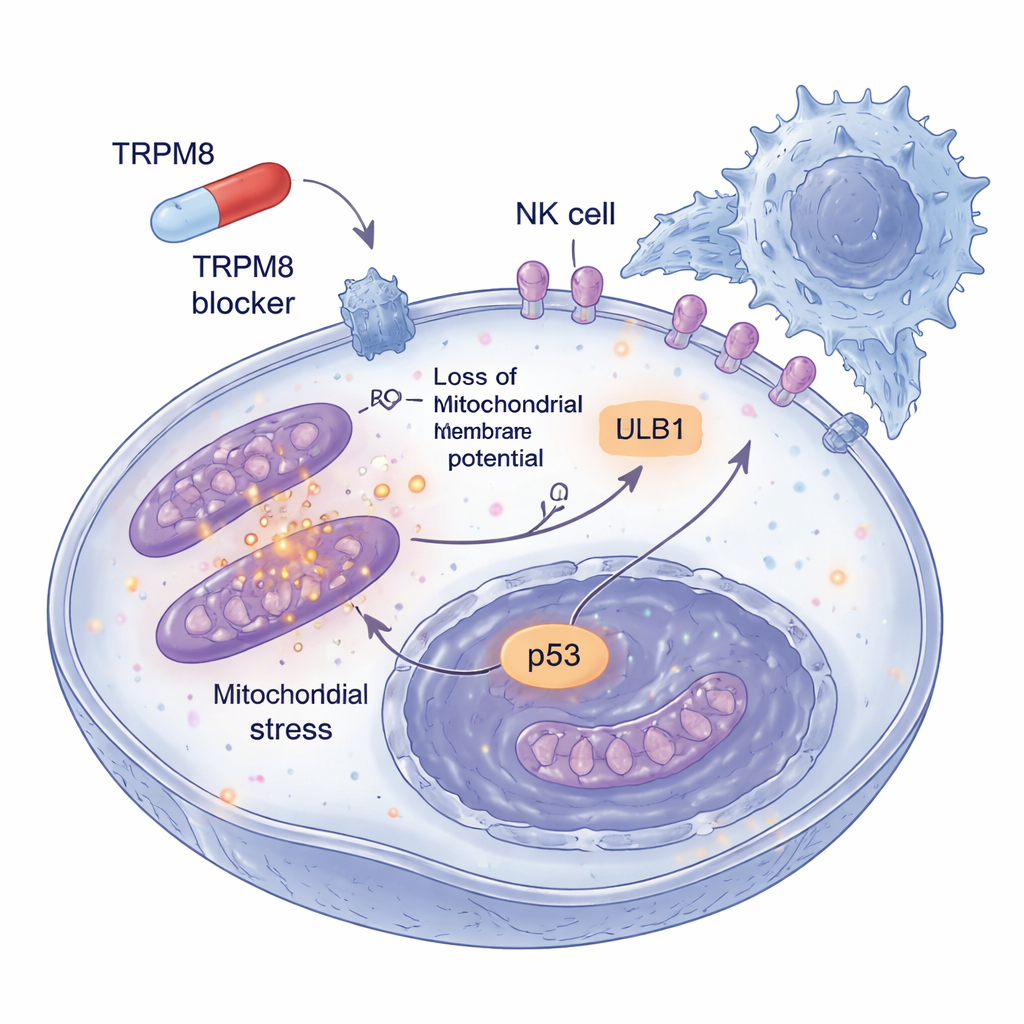
Wat dit kan betekenen voor toekomstige melanoomzorg
In eenvoudige bewoordingen: het blokkeren van de TRPM8‑“koude‑sensor” verandert het in een therapeutische hefboom: het drijft melanoomacellen in een fatale mitochondriale en DNA‑crisis en markeert ze tegelijkertijd voor vernietiging door NK‑cellen. Omdat de middelen normale huidcellen sparen en NK‑cellen zelf niet schaden, bieden ze een veelbelovende basis voor nieuwe behandelingen. De auteurs suggereren dat TRPM8‑blokkers gecombineerd kunnen worden met bestaande immunotherapieën om gevorderd, medicijnresistent melanoom op twee fronten aan te pakken: tumorcellen direct doden en overlevenden makkelijker vindbaar en vernietigbaar maken voor het immuunsysteem.
Bronvermelding: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
Trefwoorden: melanoom, TRPM8, mitochondriën, oxiderende stress, natural killer-cellen