Clear Sky Science · nl
Lactylatie-gestuurde TRIM29 veroorzaakt invasief gedrag en lymfeknoopmetastasen bij maagkanker via de hnRNPA1-gemedieerde Wnt/β-catenine-route
Waarom dit onderzoek ertoe doet
Maagkanker behoort tot de dodelijkste vormen van kanker, grotendeels omdat het vroeg uitzaait naar nabijgelegen lymfeklieren, waardoor genezing door chirurgie bemoeilijkt wordt. Deze studie onthult hoe een chemische wijziging die samenhangt met het tumormetabolisme een eiwit genaamd TRIM29 activeert, waardoor kankercellen omliggend weefsel binnendringen, nieuwe lymfevaten vormen en weerstand tegen chemotherapie ontwikkelen. Inzicht in deze keten van gebeurtenissen wijst op nieuwe manieren om de verspreiding van maagkanker te vertragen of zelfs te blokkeren.
Een gevaarlijke samenwerking in maagtumoren
De onderzoekers begonnen met het vergelijken van maagkankermonsters met aangrenzend gezond weefsel van 100 patiënten, evenals met grote openbare gendatabanken. Ze vonden dat TRIM29, een eiwit dat eerder in verband is gebracht met immuunregulatie en andere kankers, consequent verhoogd was in tumorcellen. Patiënten van wie de tumoren meer TRIM29 bevatten, hadden een grotere kans op tumorinvasie in lymfevaten en bloedvaten en hadden een slechtere algehele overleving. Deze patronen suggereerden dat TRIM29 niet alleen aanwezig is, maar actief bijdraagt aan het agressievere gedrag van maagkanker.
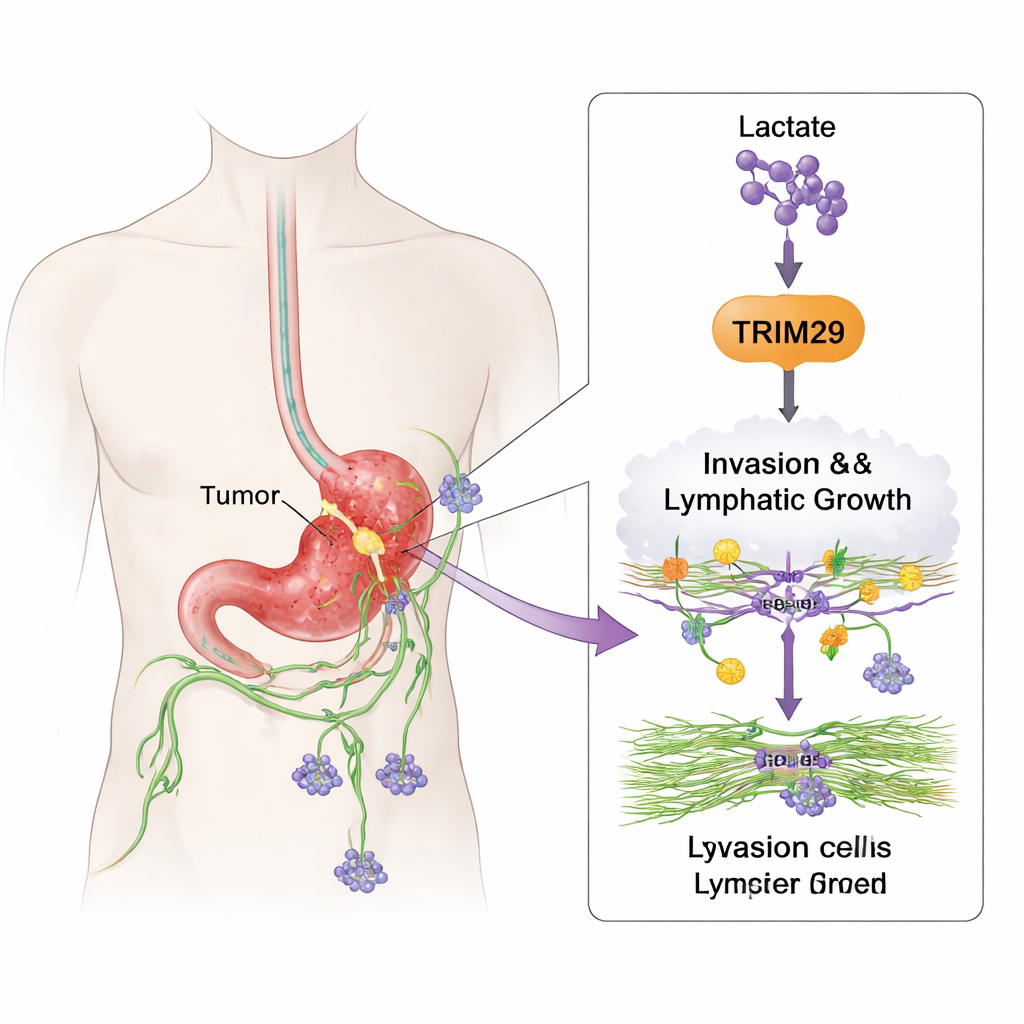
Hoe kankercellen leren reizen
Om te onderzoeken wat TRIM29 daadwerkelijk doet, veranderde het team de niveaus ervan in maagkanker-cellijnen. Wanneer ze TRIM29 verminderden, werden de cellen merkbaar minder mobiel en minder in staat om door 3D-gels te dringen die lichaamsweefsel nabootsen. Verhoogde TRIM29 had het omgekeerde effect en maakte cellen invasiever. De onderzoekers bestudeerden ook lymfeendotheelcellen, de cellen die lymfevaten bekleden. TRIM29-rijke kankercellen stimuleerden deze vatcellen om uit te lopen en buisachtige structuren te vormen, een teken van nieuwe lymfevatgroei (lymfangiogenese). In muismodellen produceerden tumoren met hoge TRIM29 meer lever- en lymfeknoopmetastasen, terwijl tumoren met gereduceerd TRIM29 minder uitzaaiden en minder lymfevaten vormden.
Moleculaire overdracht: het beschermen van een sleutelregelaar
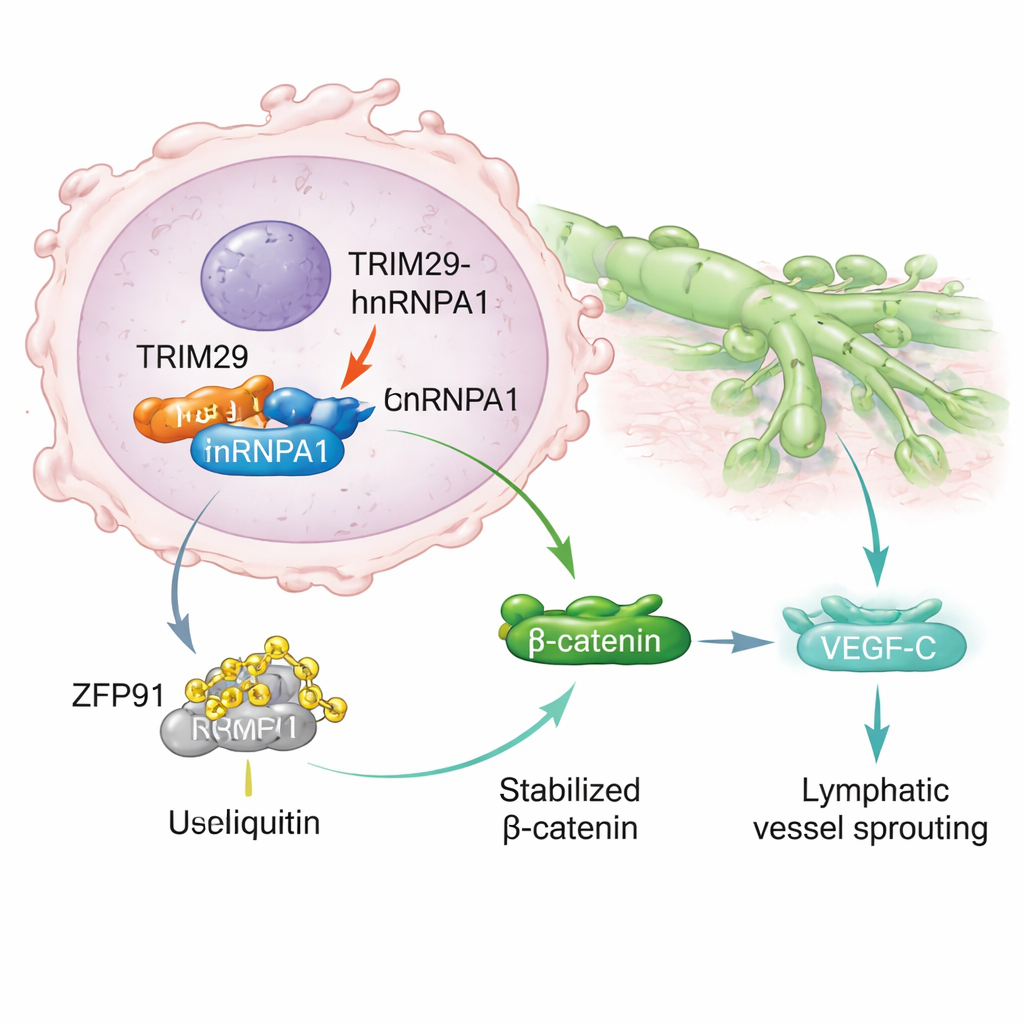
Dieper gravend ontdekten de wetenschappers dat TRIM29 fysiek bindt aan een ander eiwit, hnRNPA1, dat bekendstaat om zijn invloed op genbewerking en in verband is gebracht met tumormetastase. Normaal gesproken kan hnRNPA1 worden gemarkeerd voor afbraak door een ander eiwit, een enzym genaamd ZFP91, via het cellulaire afvalverwerkingssysteem. TRIM29 verstoort dit proces door met ZFP91 te concurreren om binding aan hnRNPA1. Wanneer TRIM29 overvloedig aanwezig is, beschermt het hnRNPA1 tegen markering en afbraak. Hierdoor wordt hnRNPA1 stabieler en hoopt het zich op in kankercellen, wat een signaalketen in gang zet die eindigt in activatie van de Wnt/β-catenine-route, een bekende stimulator van tumorgroei en -migratie. Dit verhoogt op zijn beurt de productie van VEGF‑C, een molecuul dat nieuwe lymfevaten stimuleert en de kankercellen meer “wegen” geeft om te ontsnappen.
Kanker voeden met lactaat
De studie koppelt dit invasieve gedrag ook aan hoe tumoren suiker verwerken. Snelgroeiende tumoren vertrouwen vaak op een stofwisselingsvorm die grote hoeveelheden lactaat produceert, een bijproduct dat vroeger als afval werd gezien. Hier tonen de auteurs aan dat lactaat histoneiwitten die DNA verpakken chemisch kan modificeren, specifiek op een plaats genaamd H3K9. Deze “lactylatie” fungeert als een aan-schakelaar voor het TRIM29-gen en verhoogt de activiteit ervan. Wanneer ze de lactaatproductie verlaagden met metabole geneesmiddelen, daalden TRIM29-niveaus; wanneer ze lactaat verhoogden, steeg TRIM29. Maagkankergeweven van patiënten toonden hogere niveaus van deze H3K9-lactylatie, die correleerde met meer TRIM29, meer verspreiding naar lymfeklieren en slechtere overleving. In wezen helpt het veranderde metabolisme van de tumor een agressiever genetisch programma vast te leggen.
Nieuwe manieren om chemotherapie te versterken
Lymfevaten doen meer dan kankercellen vervoeren; ze kunnen ook chemotherapiemedicijnen uit tumoren afvoeren. Met patiënt-afgeleide tumortransplantaten in muizen testten de onderzoekers of het blokkeren van TRIM29 en lymfevatgroei de werking van 5‑fluorouracil (5‑FU), een standaardmedicijn bij maagkanker, kon verbeteren. Het remmen van TRIM29 of het blokkeren van lymfangiogenese maakte elk afzonderlijk 5‑FU effectiever in het verkleinen van tumoren en het verminderen van celdeling. De combinatie van beide strategieën gaf de sterkste respons, wat wijst op een potentiële manier om bepaalde vormen van medicijnresistentie bij gevorderde ziekte te overwinnen.
Wat dit voor patiënten betekent
Dit werk schetst een stap-voor-stap overzicht: maagtumoren produceren overtollig lactaat, dat TRIM29 activeert; TRIM29 beschermt vervolgens hnRNPA1, stabiliseert een groeipad en verhoogt de vorming van lymfevaten en de uitzaaiing naar lymfeklieren. Klinisch identificeren hoge TRIM29-niveaus en bijbehorende lactylatiemerkers patiënten met een hoger risico op agressieve ziekte. In de toekomst zouden geneesmiddelen die lactaatsignaalgeving verminderen, TRIM29 blokkeren of de groei van lymfevaten voorkomen, gecombineerd kunnen worden met bestaande chemotherapie om te voorkomen dat maagkanker uitzaait en om behandelingen effectiever te maken.
Bronvermelding: Hua, R., Yu, J., Niu, Y. et al. Lactylation-drived TRIM29 induces invasive behavior and lymph node metastasis in gastric cancer via hnRNPA1-mediated Wnt/β-catenin pathway. Cell Death Dis 17, 222 (2026). https://doi.org/10.1038/s41419-026-08468-9
Trefwoorden: metastase bij maagkanker, TRIM29, lactaat en lactylatie, lymfangiogenese, Wnt beta-catenine-route