Clear Sky Science · nl
KIF20A remt TRIM21‑afhankelijke ubiquitinatie van DHX9 om SOX2‑stabiliteit te versterken, waardoor OSCC‑stamcelkenmerken en ferroptose‑weerstand toenemen
Waarom dit onderzoek belangrijk is voor patiënten met mondkanker
Orale plaveiselcelcarcinoom, een veelvoorkomende vorm van mondkanker, recidiveert vaak en is behandelresistent. Veel mislukkingen van chirurgie, chemotherapie en bestraling zijn terug te voeren op een kleine, hardnekkige populatie van "kanker‑stamcellen" die de tumor kunnen laten hergroeien en weerstand bieden tegen celdood. Deze studie onthult een cruciaal moleculair circuit dat deze cellen helpt overleven en weerstand bieden tegen een nieuwere vorm van celdood genaamd ferroptose, en wijst op een medicatiestrategie die de standaardchemotherapie mogelijk effectiever kan maken.
Een verborgen aandrijver in mondtumoren
De onderzoekers begonnen met het vergelijken van tumorweefsel van patiënten met omliggend gezond weefsel. Ze vonden dat het eiwit KIF20A consequent veel hoger was in kankercellen. Bij analyse van grotere patiëntendatasets bleek dat mensen met tumoren met hogere KIF20A‑niveaus doorgaans een kortere overleving hadden, wat suggereert dat dit eiwit verband houdt met agressieve ziekte. 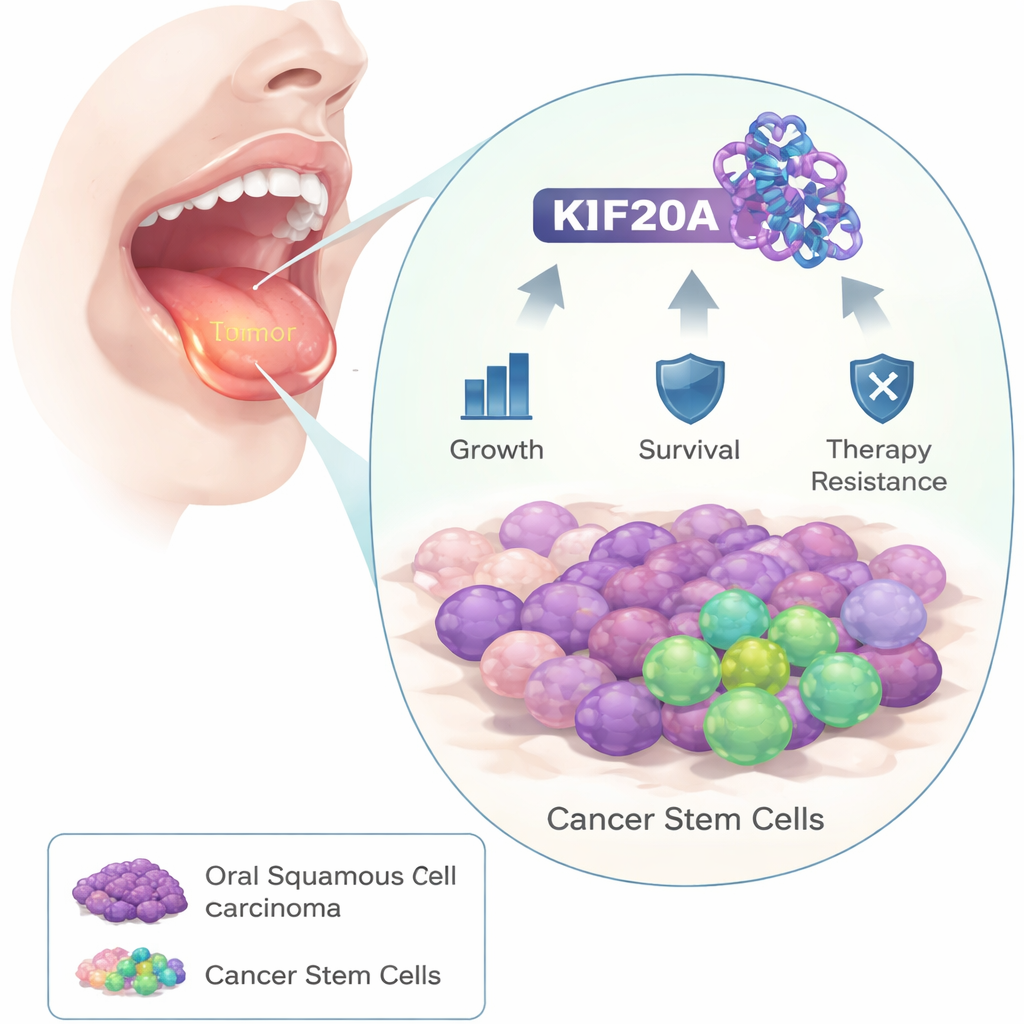
Hoe KIF20A een belangrijke RNA‑helper beschermt
Om te begrijpen wat KIF20A precies doet, gebruikte het team eiwit‑mappingtechnieken om naar interactiepartners in kankercellen te zoeken. Een centrale partner die naar voren kwam was DHX9, een eiwit dat RNA‑moleculen beheert en beïnvloedt hoe lang bepaalde boodschappen in de cel blijven bestaan. De wetenschappers ontdekten dat KIF20A zich bindt aan DHX9 en voorkomt dat het wordt gemarkeerd voor afbraak door een ander eiwit, de E3‑ligase TRIM21, die normaal gesproken DHX9 met ubiquitineketens tagt om het naar het eiwitafbraakmechanisme te sturen. Door deze tagging te blokkeren remt KIF20A de afbraak van DHX9 en verhoogt het de hoeveelheid, vooral in het cytoplasma van de cel, waar DHX9 op specifieke RNA‑doelen kan werken.
Van RNA‑stabiliteit naar kanker‑stamcellen en ferroptose‑weerstand
Met stabieler DHX9 komt een andere cruciale speler in zicht: SOX2, een meesterregelaar die cellen helpt in een stam‑achtige staat te blijven en behandeling te weerstaan. De studie toont aan dat DHX9 het RNA‑bericht van SOX2 beschermt tegen afbraak, waardoor er meer SOX2‑eiwit kan worden geproduceerd. In orale kankercellen leidde extra KIF20A tot hogere DHX9‑ en SOX2‑niveaus, meer vorming van tumorsferen in kweek, en een groter aandeel cellen dat stamcelmarkers tot expressie bracht — aanwijzingen voor versterkte "kanker‑stemheid." KIF20A maakte de cellen ook minder kwetsbaar voor ferroptose, een door ijzer aangedreven, lipide‑gerelateerde celdood die wordt onderzocht als manier om resistente kankercellen te doden. Wanneer KIF20A werd uitgeschakeld, krompen tumoren in muismodellen makkelijker en namen markers van ferroptose toe, wat aangeeft dat de tumoren die beschermende barrière hadden verloren.
Een moleculair circuit met een drugbaar zwak punt
Door deze stukken samen te voegen, stellen de auteurs een KIF20A–DHX9–SOX2‑as voor: KIF20A stabiliseert DHX9, DHX9 stabiliseert SOX2‑RNA, en SOX2 onderhoudt op zijn beurt kanker‑stamcellen en blokkeert ferroptose. Dit circuit voedt ook de PI3K–AKT‑route, een belangrijke groeien overlevingsweg in veel vormen van kanker. 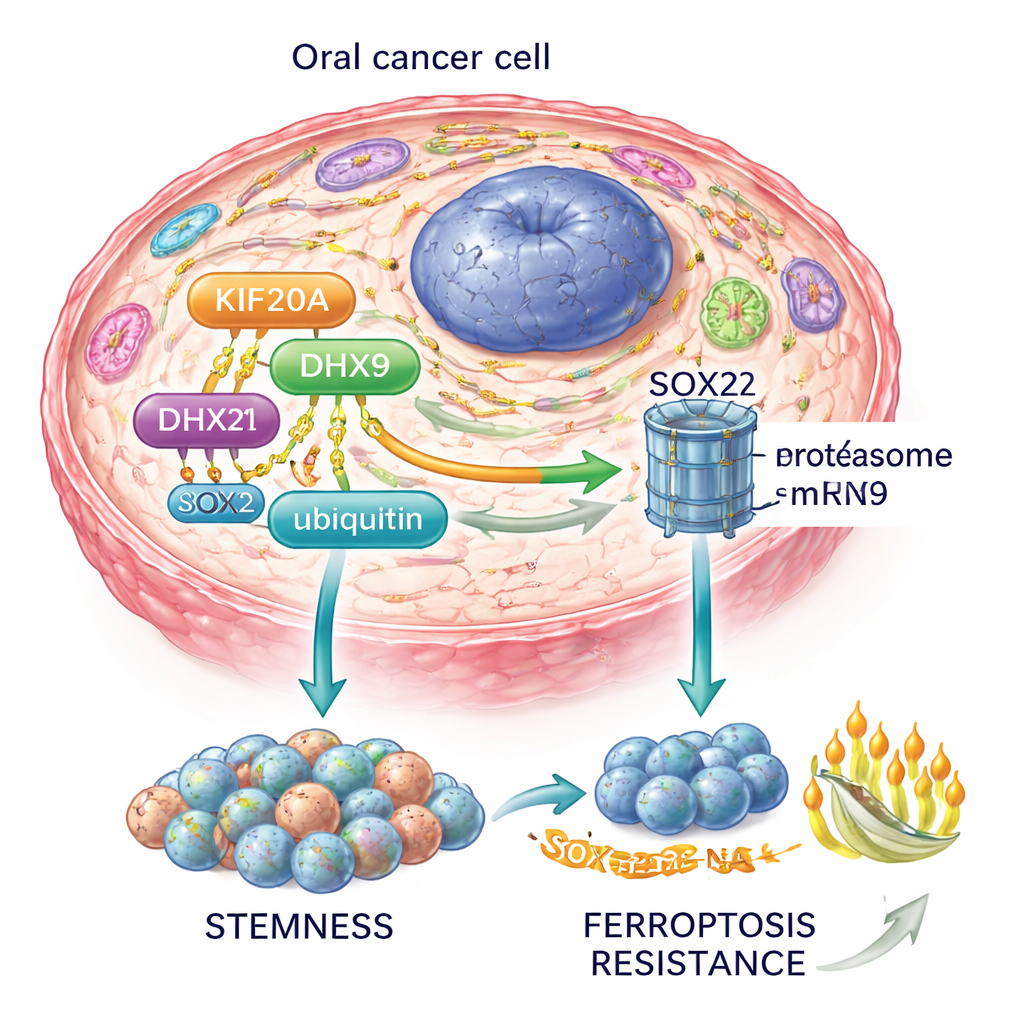
Een kandidaatmiddel om resistente tumoren te verzwakken
Om naar een behandeling toe te werken doorzochten de onderzoekers grote geneesmiddel‑gen‑databanken op verbindingen die voorspeld werden het KIF20A‑gerelateerde genpatroon tegen te werken. Ze identificeerden ENMD‑2076, een orale multitarget‑kinaseremmer die al in andere kankers is getest. In orale kankercellen met hoge KIF20A verlaagde ENMD‑2076 KIF20A‑, DHX9‑ en SOX2‑niveaus, dempte signalering gerelateerd aan stamcelkenmerken en remde de groei. Gecombineerd met het standaardchemotherapeuticum cisplatine gaf ENMD‑2076 een sterker antikanker‑effect dan elk van de middelen alleen, zowel in celkweken als in muizen, zonder duidelijke toename van toxiciteit.
Wat dit betekent voor toekomstige therapieën
Voor niet‑specialisten is de conclusie dat deze studie laat zien hoe één overactief eiwit, KIF20A, mondtumoren helpt een kleine populatie "zaad"‑cellen levend en beschermd te houden tegen een veelbelovende vorm van celdood. Door deze keten in kaart te brengen — van KIF20A naar DHX9 naar SOX2 — belichten de onderzoekers nieuwe doelwitten voor geneesmiddelen en tonen ze aan dat een bestaand experimenteel middel, ENMD‑2076, deze as kan verzwakken en cisplatine effectiever kan maken in modellen. Hoewel vervolgonderzoek nodig is om veiligheid en voordelen bij patiënten te bevestigen, ondersteunen de bevindingen een toekomst waarin blokkering van dit circuit kan helpen relapse te voorkomen en medicijnresistentie bij orale kanker te overwinnen.
Bronvermelding: Zhang, Z., Li, Y., Hu, J. et al. KIF20A inhibits TRIM21-dependent ubiquitination of DHX9 to boost SOX2 stability, enhancing OSCC stemness and ferroptosis resistance. Cell Death Dis 17, 218 (2026). https://doi.org/10.1038/s41419-026-08467-w
Trefwoorden: orofaryngeaal plaveiselcelcarcinoom, kanker‑stamcellen, ferroptose, KIF20A, SOX2