Clear Sky Science · nl
Selenomethionine als een dubbelwerkende ferroptose-remmer: door seleniumvoorziening aangedreven GPX4-biosynthese voorbij transsulfuratie en door reductieve capaciteit gemedieerde ROS-afvang onafhankelijk van GPX4-activiteit
Waarom het beschermen van onze cellen tegen een „roestachtige" dood ertoe doet
Cellen in ons lichaam kunnen op vele manieren sterven, en een van de nieuwere en meest intrigerende vormen heet ferroptose — een soort door ijzer aangedreven, „roestachtige" beschadiging van celmembranen. Dit proces wordt nu gekoppeld aan ziekten variërend van nierschade tot neurodegeneratie. Het spoorelement selenium, dat veel mensen kennen uit voedingssupplementen, blijkt een sleutelrol te spelen bij het stoppen van deze gevaarlijke vorm van celdood. Deze studie onderzoekt hoe een veelvoorkomend seleniumhoudend aminozuur, selenomethionine, cellen kan beschermen tegen ferroptose via niet één maar twee verschillende beschermende strategieën.
Een nieuwe verdediger gevonden in een grote zoektocht naar geneesmiddelen
Om kleine moleculen te vinden die ferroptose kunnen blokkeren, screenden de onderzoekers duizenden verbindingen afkomstig van door de FDA goedgekeurde geneesmiddelen en natuurlijke producten. Ze gebruikten een chemische stof genaamd RSL3 om ferroptose op te wekken in humane kankercellijnen en hielden vervolgens celdood en de ophoping van beschadigde, geoxideerde vetten in celmembranen bij. Onder alle kandidaten bleek selenomethionine een sterke beschermer: het verminderde zowel lipidebeschadiging als celdood in verschillende celtypen en in twee belangrijke ferroptosemodellen — één aangedreven door directe remming van GPX4 (met RSL3) en een ander door uitputting van cystine, een bouwsteen voor het antioxidant glutathion. Deze resultaten plaatsten selenomethionine als een brede en robuuste ferroptose-remmer. 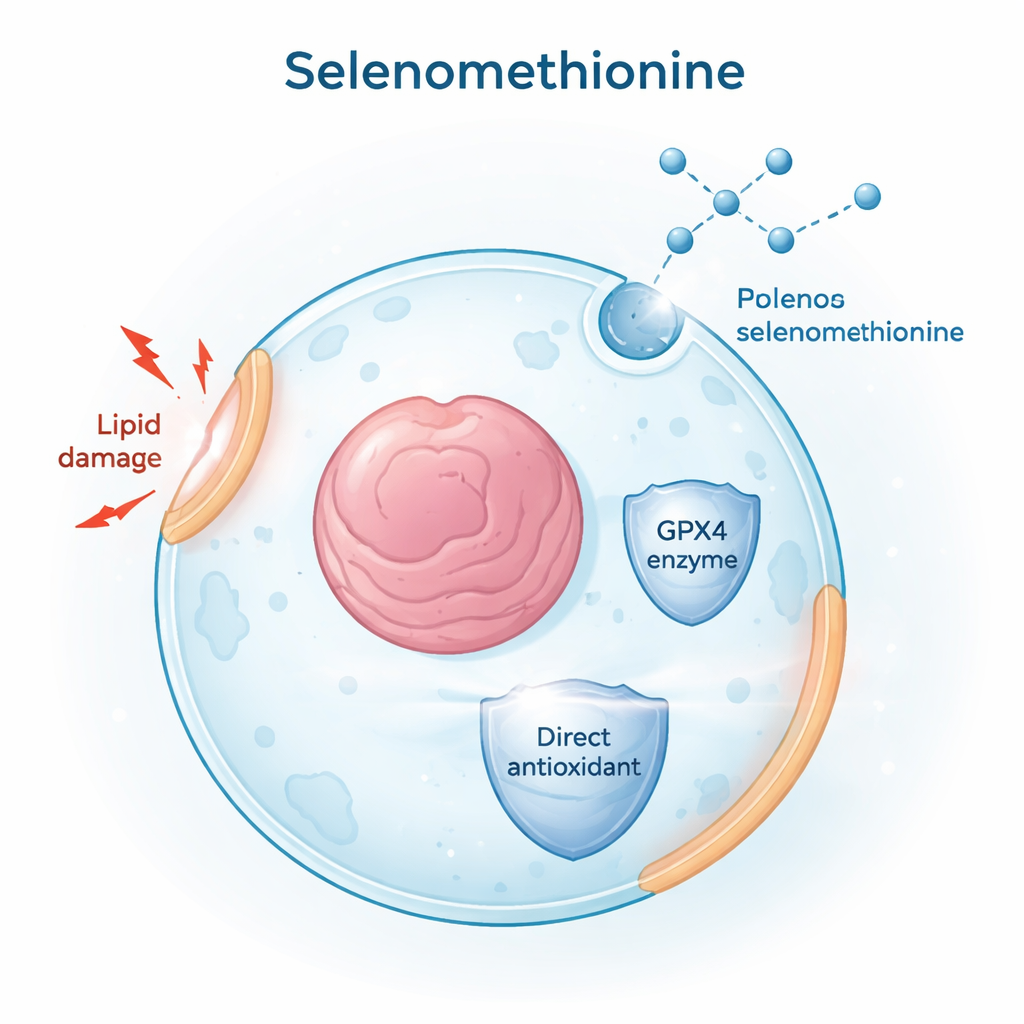
Seleniumlevering voor een sleutelenzym dat beschermt
Een kernbescherming tegen ferroptose in cellen is een enzym dat GPX4 heet en afhankelijk is van selenium om te functioneren. Het team wilde bepalen of selenomethionine simpelweg deze route voedt of meer doet. Ze volgden hoe selenium uit selenomethionine omgezet kan worden in vormen die geschikt zijn voor de opbouw van GPX4, zelfs wanneer een gebruikelijke route, de transsulfuratie-pathway, verzwakt of geblokkeerd is. Met genetische knockdowns en chemische remmers van enzymen in deze zwavel–seleniumroutes vonden ze dat selenomethionine nog steeds GPX4-niveaus verhoogde en cellen beschermde. Dit toonde aan dat cellen meerdere metabole routes kunnen aanboren om selenium uit selenomethionine te halen en de GPX4-productie gaande te houden, zelfs in weefsels waar de klassieke route zwak is.
Bescherming die niet afhankelijk is van het gebruikelijke enzym
Verrassend genoeg bleef selenomethionine beschermen tegen ferroptose toen de onderzoekers GPX4 volledig uit cellen verwijderden met CRISPR-genbewerking. Het verlaagde nog steeds membraanlipidebeschadiging en celdood, wat aangeeft dat GPX4 niet het volledige verhaal is. Aanvullende experimenten wezen erop dat een deel van deze bescherming voortkomt uit het inbouwen van selenomethionine in nieuwgesynthetiseerde eiwitten, maar dat dit slechts een deel van het effect verklaart. De auteurs richtten zich vervolgens op de chemische reactiviteit van selenomethionine zelf. Ze vonden dat het direct reactieve zuurstofsoorten (ROS), waaronder waterstofperoxide, kan neutraliseren en wordt omgezet in een geoxideerde „sulfoxide"-vorm. Massaspectrometrie bevestigde dit product, en het toedienen van de sulfoxide-versie aan cellen verminderde ook ferroptose, wat impliceert dat cellen het kunnen recyclen terug naar actieve selenomethionine in een redoxcyclus.
Van celcultuur naar het beschermen van nieren in levende dieren
Om te testen of deze mechanismen van belang zijn in een heel organisme, gebruikte het team een muismodel van acute nierschade veroorzaakt door het chemotherapeuticum cisplatine, een aandoening waarvan bekend is dat ferroptose betrokken is. Muizen die met cisplatine werden behandeld vertoonden gewichtsverlies, opgezwollen nieren, slechtere nierfunctie en hoge niveaus van ferroptosemerken. Wanneer de dieren selenomethionine kregen, verbeterden veel van deze problemen: het lichaamsgewicht herstelde, nierzwelling nam af, bloedwaarden voor nierfunctie normaliseerden, ontstekingssignalen daalden en chemische merkers van lipidebeschadiging namen af. Nierweefsel toonde ook hogere GPX4-niveaus en minder structurele schade. Deze voordelen waren vergelijkbaar met die gezien bij ferrostatine-1, een bekend experimenteel ferroptoseblokker. 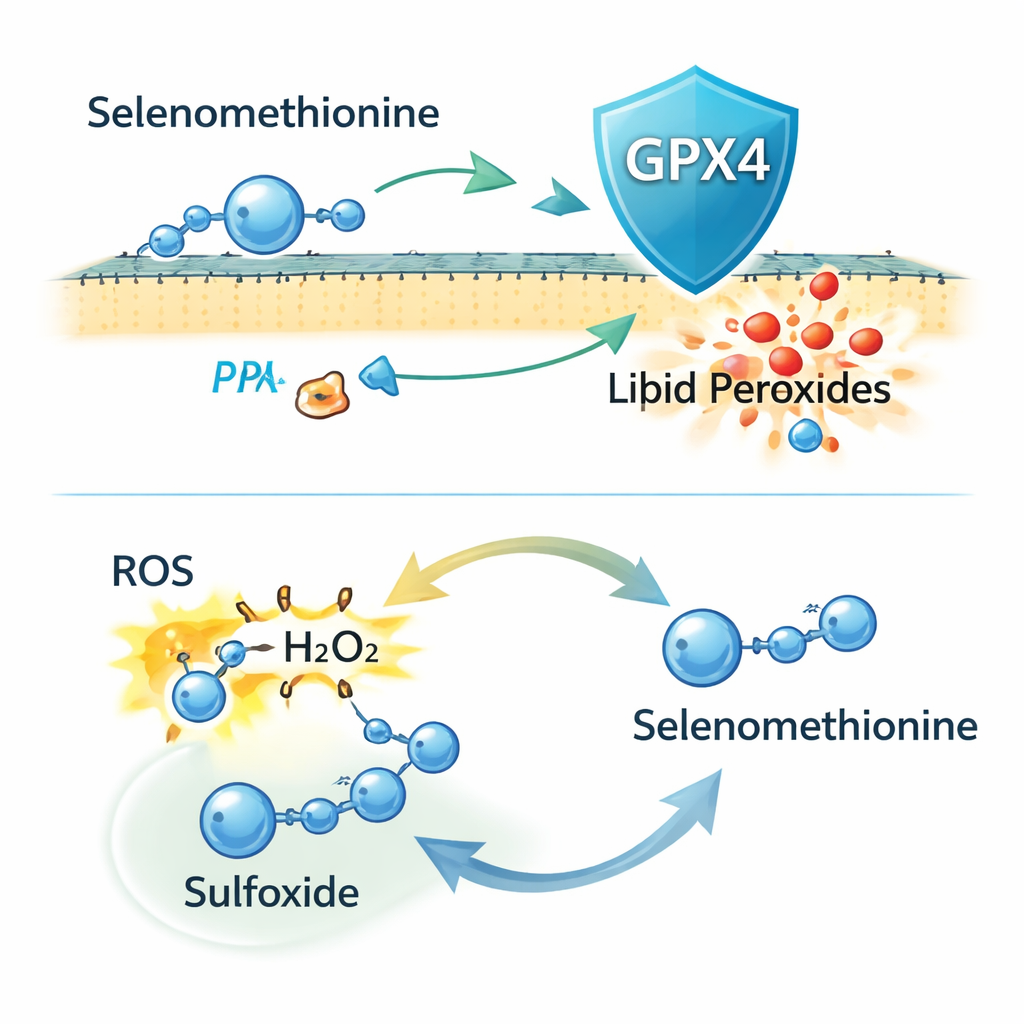
Wat dit betekent voor toekomstige therapieën
In gewone bewoordingen suggereert dit werk dat selenomethionine fungeert als een tweevoudige brandblusser tegen een ijzer-gedreven „roesten" van celmembranen. Enerzijds levert het selenium zodat cellen meer van het GPX4-enzym kunnen opbouwen, dat fungeert als een intern opruimteam voor beschadigde vetten. Anderzijds kan selenomethionine zelf schadelijke oxidanten absorberen en worden gerecycled, wat een GPX4-onafhankelijke back-upbescherming biedt. Gezamenlijk maken deze eigenschappen selenomethionine een veelbelovende kandidaat voor het voorkomen of behandelen van ziekten waarin ferroptose een centrale rol speelt, zoals geneesmiddel-geïnduceerde nierschade en mogelijk andere aandoeningen die worden aangedreven door ongecontroleerde oxiderende stress.
Bronvermelding: Xia, C., Sun, X., Shao, J. et al. Selenomethionine as a dual-mechanism ferroptosis inhibitor: selenium-supply-driven GPX4 biosynthesis beyond transsulfuration and reductive-capacity-mediated ROS scavenging independent of GPX4 activity. Cell Death Dis 17, 224 (2026). https://doi.org/10.1038/s41419-026-08466-x
Trefwoorden: ferroptose, selenium, selenomethionine, oxiderende stress, acute nierschade