Clear Sky Science · nl
Het chaperonine-onderdeel TRiC Cct3 is vereist voor axonaal transport, myelinisatie en verfijning van neuromusculaire junctions
Wanneer zenuwbedrading misgaat
Onze hersenen en lichamen vertrouwen op lange, kabelachtige zenuwvezels om signalen snel en betrouwbaar te geleiden. Veel zenuwen zijn omhuld met isolerende myeline en hun uiteinden moeten precieze contacten met spieren vormen. Dit artikel onderzoekt wat er gebeurt wanneer een belangrijke cellulaire “hulp” bij eiwitvouwing, genaamd Cct3, uitvalt. Met behulp van zebravissen en menselijk weefsel laten de auteurs zien hoe dit ene onderdeel van een groot chaperon-machinet de myeline, zenuw–spierverbindingen en het interne transportsysteem dat zenuwcellen levend en functioneel houdt, kan ontregelen.
Een cellulaire kleermaker voor het bouwen van zenuwen
In elke cel moeten nieuw gemaakte eiwitten in de juiste vorm worden gevouwen, net zoals een pak zorgvuldig op maat wordt gemaakt. Het TRiC-complex, waar het subunit Cct3 deel van uitmaakt, is een van de grote “kleermakers” en helpt ongeveer 10% van alle cellulaire eiwitten — vooral de structurele eiwitten actine en tubuline — correct te vouwen. Deze bouwstenen vormen het interne skelet van de cel en de sporen waarlangs vitaal vrachtvervoer plaatsvindt. Bij patiënten met defecte versies van CCT3 en gerelateerde genen tonen hersenscans verminderd wit materiaal (de myeline-rijke bedrading van de hersenen) en problemen in de perifere zenuwen en spieren. De auteurs wilden begrijpen hoe het verlies van Cct3 de ontwikkeling en functie van zenuwen verstoort.
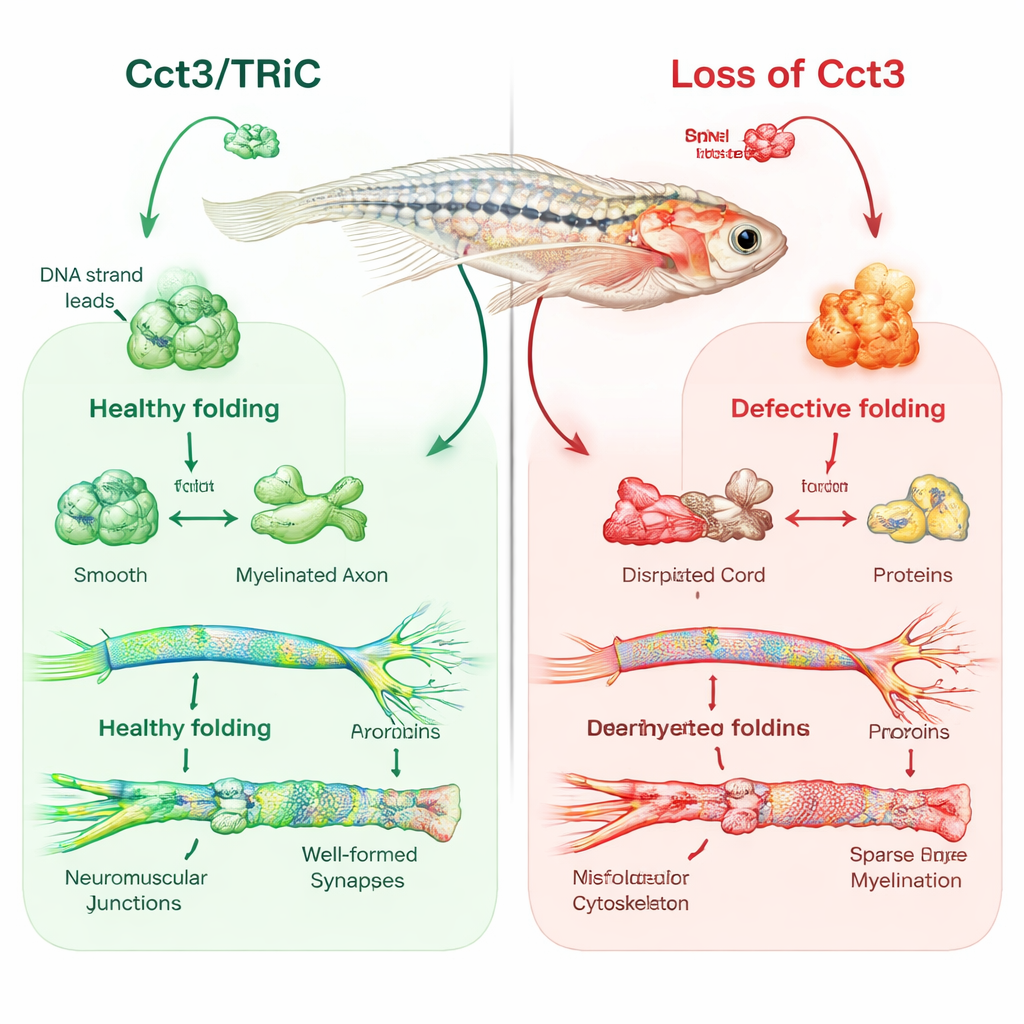
Zebravissen als venster op zenuwisolatie
Het team gebruikte CRISPR/Cas9-genbewerking om zebravissen te maken zonder functioneel cct3. Deze kleine vissen hadden kleinere hersenen en ogen, vochtophoping rond het hart, zwakke reacties op aanraking en overleden binnen enkele dagen. Wanneer de onderzoekers normaal cct3 herstelden door het injecteren van messenger-RNA, verbeterden veel van deze afwijkingen, wat bevestigt dat het verlies van Cct3 de hoofdoorzaak was. Met focus op myeline gebruikten ze fluorescerende markers en elektronenmicroscopie om de isolerende lagen rond zenuwen te visualiseren. Bij normale vissen wikkelden myeline-vormende cellen in de hersenen en perifere zenuwen axonen in nette, gelaagde scheden tegen dag vier van de ontwikkeling. Daarentegen hadden cct3-mutanten veel minder myelinerende cellen en vrijwel geen correcte myeline om veel axonen, ondanks dat die axonen er aan de oppervlakte normaal gevormd uitzagen.
Kwetsbare steunende cellen en gespannen zenuw–spierverbindingen
Om te achterhalen waarom myeline ontbrak, onderzochten de auteurs Schwann-cellen en aanverwante neurale-kamcellen — de ondersteunende cellen die perifere zenuwen omhullen. Bij normale vissen strekten deze cellen lange, slanke uitlopers uit en verfijnden ze hun vorm terwijl ze myeline-segmenten vormden. In mutanten raakten ze bol, kortten hun uitlopers in en fragmentariseerden. Hun kernen bouwden zich op een manier af die typisch is voor geprogrammeerde celdood, en een belangrijke doodsmarker (geactiveerde Caspase 3) verscheen, wat aantoonde dat veel van deze cellen vroegtijdig afstierven. Tegelijkertijd faalde bij de neuromusculaire junctions, waar zenuwen spieren ontmoeten, het verfijningspatroon van receptor-‘hotspots’ op spieren. In plaats van vele kleine, precieze clusters hadden mutanten minder, grotere receptorvlekken, wat doet denken aan de vereenvoudigde synaptische plooien die gezien zijn bij een menselijke patiënt met een CCT3-mutatie.
Gebroken interne sporen en vertraagd vrachtverkeer
Aangezien TRiC helpt bij het vouwen van actine en tubuline, keken de auteurs nauw naar het interne framingsysteem van motoraxonen. Ze ontdekten dat de totale tubuline-niveaus sterk waren verminderd in mutanten en dat het aantal normale microtubuli — de holle buizen die als sporen voor transport dienen — dramatisch afnam in zowel centrale als perifere zenuwen. Chemische “tags” op tubuline die belangrijk zijn voor stabiele, transportklare microtubuli waren ook zwaar veranderd. Met behulp van live-imaging van gloeiende mitochondriën en endosomen binnen motoraxonen volgden ze hoe deze ladingen bewogen. Bij gezonde vissen reisden organellen snel en gericht langs het axon. Bij mutanten raakten veel organellen vast of wiebelden ze alleen heen en weer, wat overeenkomt met beschadigde sporen en verstoord transport.
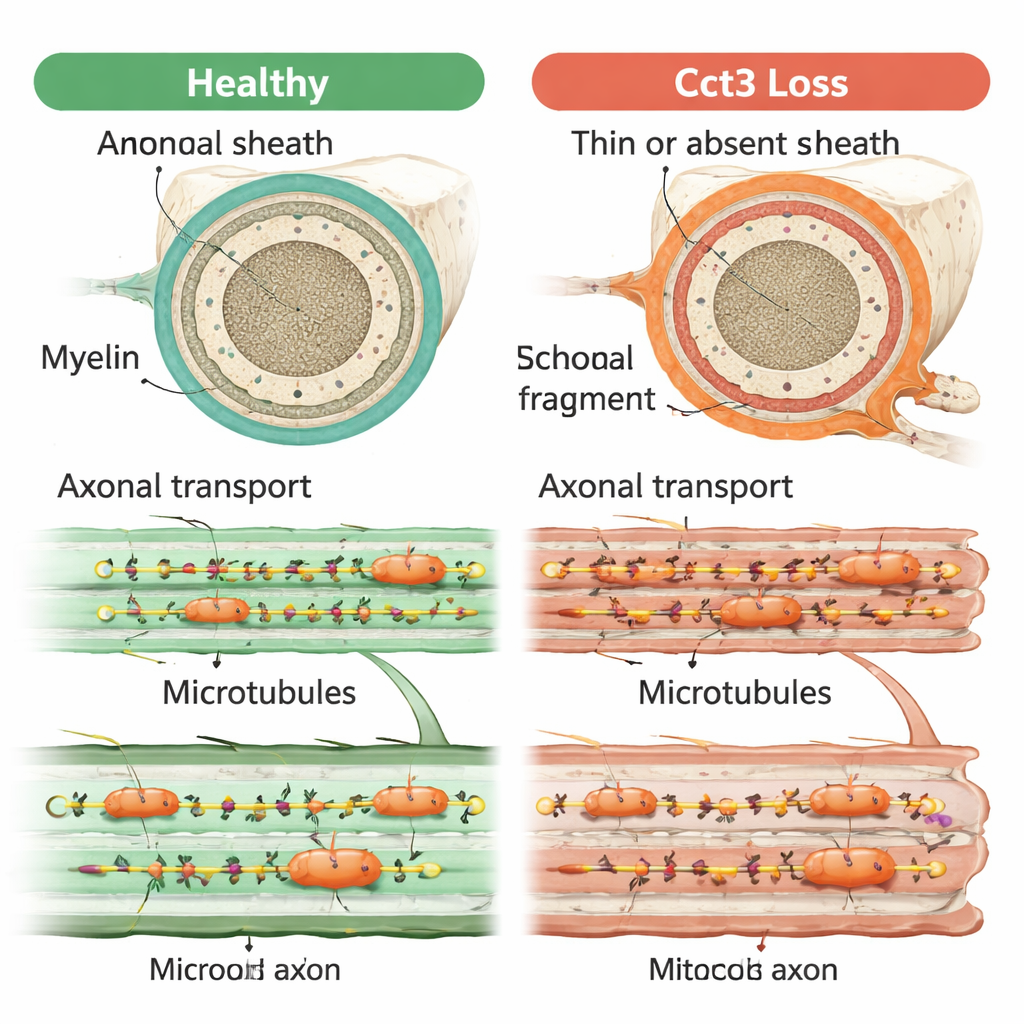
Een kernprobleem achter veel symptomen
Alles bij elkaar laten de bevindingen zien dat Cct3 essentieel is voor meerdere onderling verbonden aspecten van zenuwgezondheid: het ondersteunt het overleven van myeline-vormende ondersteunende cellen, maakt correcte myeline-omstrengeling mogelijk en staat maturing neuromusculaire junctions toe om fijn afgesteld te raken. Al deze rollen zijn terug te voeren op zijn taak bij het vouwen en in stand houden van de eiwitten die het cytoskelet en de microtubule-sporen voor axonaal transport bouwen. Wanneer die sporen falen, kunnen belangrijke signalen en materialen niet naar de juiste plaatsen langs de zenuw worden gebracht, wat waarschijnlijk zowel de communicatie met myeline-vormende cellen als de vorming van zenuw–spiercontacten ondermijnt. Dit werk suggereert dat aangetast axonaal transport de gemeenschappelijke draad kan zijn die de uiteenlopende hersen- en zenuwproblemen in TRiC-gerelateerde aandoeningen verbindt.
Bronvermelding: Zhang, X., Zajt, K.K., Palaz, T. et al. The chaperonin TRiC component Cct3 is required for axonal transport, myelination, and neuromuscular junction refinement. Cell Death Dis 17, 221 (2026). https://doi.org/10.1038/s41419-026-08465-y
Trefwoorden: myelinisatie, axonaal transport, neuromusculaire junction, moleculaire chaperonnes, zebravismodel