Clear Sky Science · nl
Verstoorde BDNF-TrkB‑trafficking en -signalering in basale voorhersenneuronen bij het syndroom van Down
Waarom deze hersenstudie ertoe doet
Mensen met het syndroom van Down worden ouder dan ooit, maar lopen ook een sterk verhoogd risico om halverwege hun leven dementie te ontwikkelen die lijkt op Alzheimer. Deze studie kijkt diep in individuele hersencellen om te begrijpen waarom bepaalde neuronen zo kwetsbaar zijn. Door te volgen hoe deze cellen een sleutelmolecuul dat als “voedingsstof” voor de hersenen fungeert verplaatsen en erop reageren, ontdekken de onderzoekers een verkeersopstopping binnenin neuronen die geheugenverlies zou kunnen verklaren en richting nieuwe behandelingsstrategieën wijst.
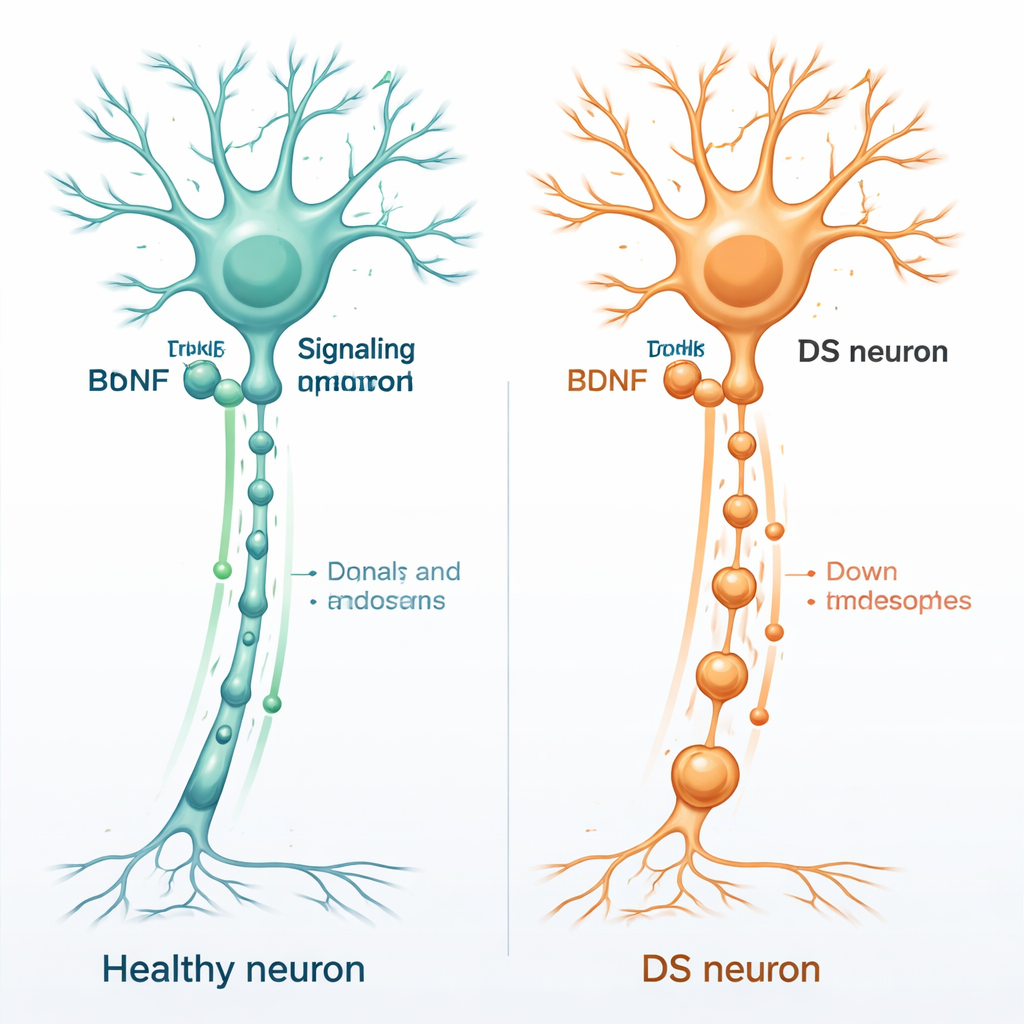
Hersenvoedsel en de gezondheid van zenuwcellen
Gezonde hersencellen zijn afhankelijk van een groep ondersteunende moleculen, neurotrofinen genoemd, die als meststof voor neuronen werken. Een van de belangrijkste is het brain‑derived neurotrophic factor, of BDNF. BDNF bindt aan een aanmeereiwit op neuronen dat TrkB heet, meestal aan de verste uiteinden van zenuwvezels. Zodra BDNF zich hecht, wordt het hele BDNF–TrkB‑complex in kleine membranenblaasjes naar binnen gehaald en terug langs de lange zenuwvezel naar het cellichaam vervoerd. Deze bewegende blaasjes, bekend als signaleringsendosomen, vertellen de kern welke genen moeten worden aangezet om het neuron levend, verbonden en aanpasbaar te houden.
Als cellulaire verzendcontainers te groot worden
Het team richtte zich op neuronen in de basale voorhersenen, een groep cellen die sterk bijdraagt aan geheugen en aandacht en een van de eerste is die afsterft bij zowel het syndroom van Down als de ziekte van Alzheimer. Met een muismodel voor het syndroom van Down, Dp1Tyb, kleurden ze neuronen voor een vroege endosoommarker en vergeleken die met normale neuronen. De neuronen van het syndroom van Down bevatten veel meer vroege endosomen die meer dan 50 procent groter waren dan gebruikelijk. Deze structuren worden gecontroleerd door Rab5, een moleculaire schakelaar die helpt bij het vormen en sorteren van deze interne “verzendcontainers”. De onderzoekers vonden dat Rab5 in een overactieve staat vastzat in de neuronen van mensen met het syndroom van Down, zelfs vóór BDNF‑stimulatie, wat suggereert dat het endosomale systeem al te hard werkte.
Verkeersopstoppingen langs de zenuwvezel
Vervolgens vroegen de wetenschappers zich af of dit verstoorde interne landschap de verplaatsing van BDNF‑signalen zou belemmeren. Ze lieten neuronen groeien in microfluidische apparaten die de cellichamen scheiden van hun axonuiteinden, waardoor ze alleen de axontips kunnen stimuleren. Door onschadelijke fluorescentie‑tracers te volgen die dezelfde transportroute delen als BDNF–TrkB‑complexen, maten ze hoe snel de signaleringsendosomen terug naar de cellichamen reisden. In normale neuronen zorgde het toevoegen van BDNF ervoor dat de endosomen ongeveer 30 procent sneller bewogen en minder vaak pauzeerden, wat wijst op een sterke reactie op groeisignalen. In neuronen van het syndroom van Down faalde BDNF er echter in om het transport te versnellen of het aantal pauzes te verminderen. Een apart experiment dat echte TrkB‑receptoren volgde bevestigde dat minder van deze receptoren met succes het cellichaam bereikten in de cellen van het syndroom van Down.
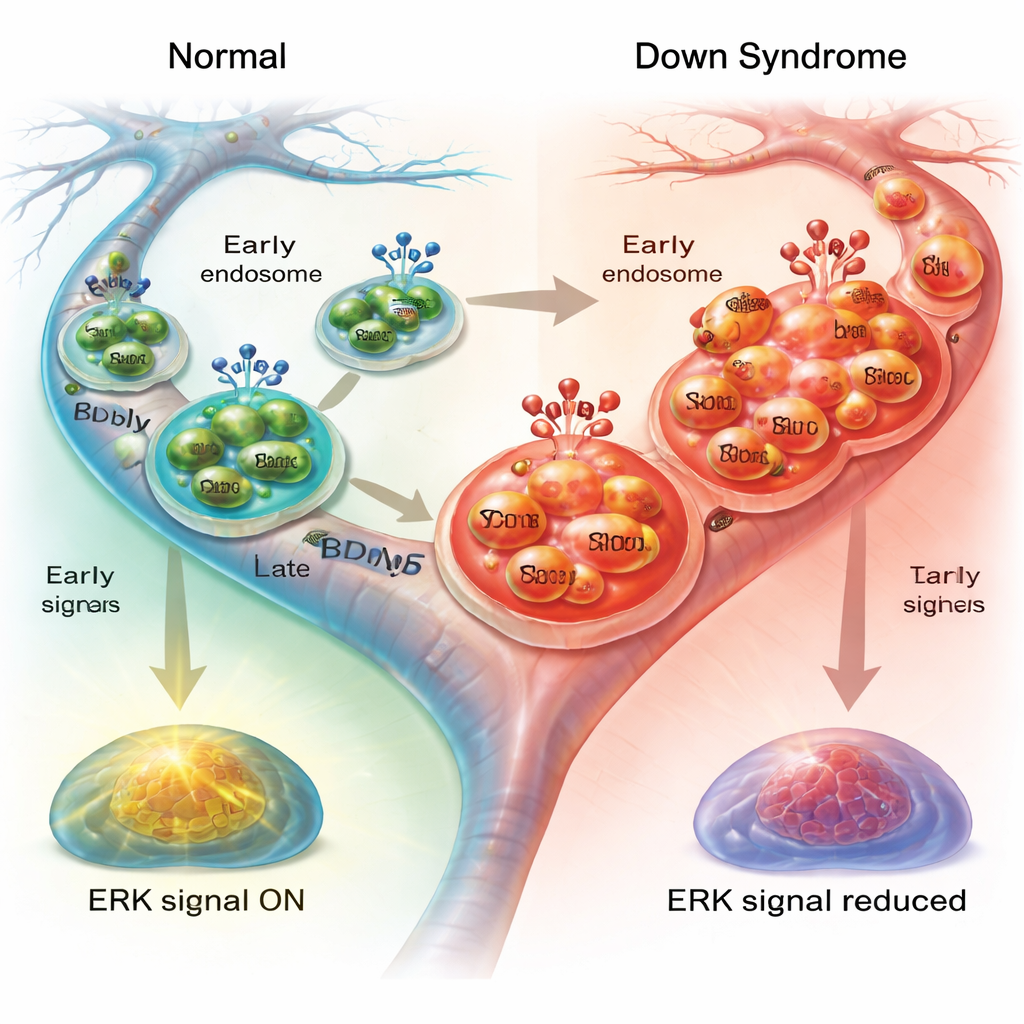
Verzwakte downstreamsignalen binnen de cel
Om deze reizende blaasjes de gezondheid van het neuron te laten ondersteunen, moeten ze interne signaalroutes activeren zodra ze hun bestemming bereiken. Een belangrijke route omvat ERK1/2, een paar enzymen dat BDNF’s boodschap naar de kern doorgeeft en helpt het celskelet en het transportapparaat te reguleren. Toen de onderzoekers geactiveerde ERK1/2 maten na BDNF‑behandeling, zagen ze een duidelijke toename in normale neuronen maar een veel zwakkere respons in neuronen van het syndroom van Down, vooral in de axonen. Het blokkeren van ERK1/2 in gezonde neuronen reproduceerde deels het trage transport dat in de cellen van het syndroom van Down werd gezien, waarbij endosomen vertraagden en vaker pauzeerden. Ter vergelijking had ERK1/2‑blokkade nauwelijks extra effect in de neuronen van het syndroom van Down, wat overeenkomt met reeds afgezwakte signalering.
Wat dit betekent voor hersenveroudering bij het syndroom van Down
Samengevat suggereren de bevindingen een zichzelf versterkend probleem in kwetsbare neuronen: Rab5 is overactief, vroege endosomen zwellen op, en BDNF–TrkB‑complexen raken vast in compartimenten die niet efficiënt bewegen. Daardoor bereiken minder groeisignalen het cellichaam, wordt ERK1/2‑signalering verzwakt, en wordt het mechanisme dat langafstandstransport aandrijft verder aangetast. In de loop der jaren kan dit gebrekkige communicatiesysteem bijdragen aan het vroege en ernstige verlies van basale voorhersenneuronen dat wordt gezien bij mensen met aan het syndroom van Down gerelateerde ziekte van Alzheimer. Door deze koppeling tussen endosomaal “verkeersbeheer” en groeifactor‑signalering te benadrukken, wijst de studie op nieuwe therapeutische ideeën die gericht zijn op het normaliseren van Rab5‑activiteit, het herstellen van endosoomfunctie en het versterken van BDNF‑reacties om deze cruciale neuronen te beschermen.
Bronvermelding: Blackburn, E., Birsa, N., Lopes, A.T. et al. Impaired BDNF-TrkB trafficking and signalling in Down syndrome basal forebrain neurons. Cell Death Dis 17, 214 (2026). https://doi.org/10.1038/s41419-026-08464-z
Trefwoorden: Syndroom van Down, Ziekte van Alzheimer, BDNF, axonale transport, endosomen