Clear Sky Science · nl
PDHA1–acetylatie‑signaal remt cuproptose om het anti‑androgene effect bij prostaatkanker te verminderen
Waarom dit onderzoek ertoe doet
Prostaatkanker is een van de meest voorkomende kankers bij mannen en veel gevorderde gevallen worden behandeld met middelen die de mannelijke hormoonsignalen onderdrukken. Een belangrijk middel, enzalutamide, werkt vaak eerst maar verliest dan effect wanneer tumoren resistent worden. Deze studie onthult een verrassende reden waarom sommige prostaatkankers ontsnappen aan de werking van enzalutamide en laat zien hoe het blokkeren van één metabool pad tumoren weer gevoelig kan maken, wat de weg opent naar duurzamere behandelingen.
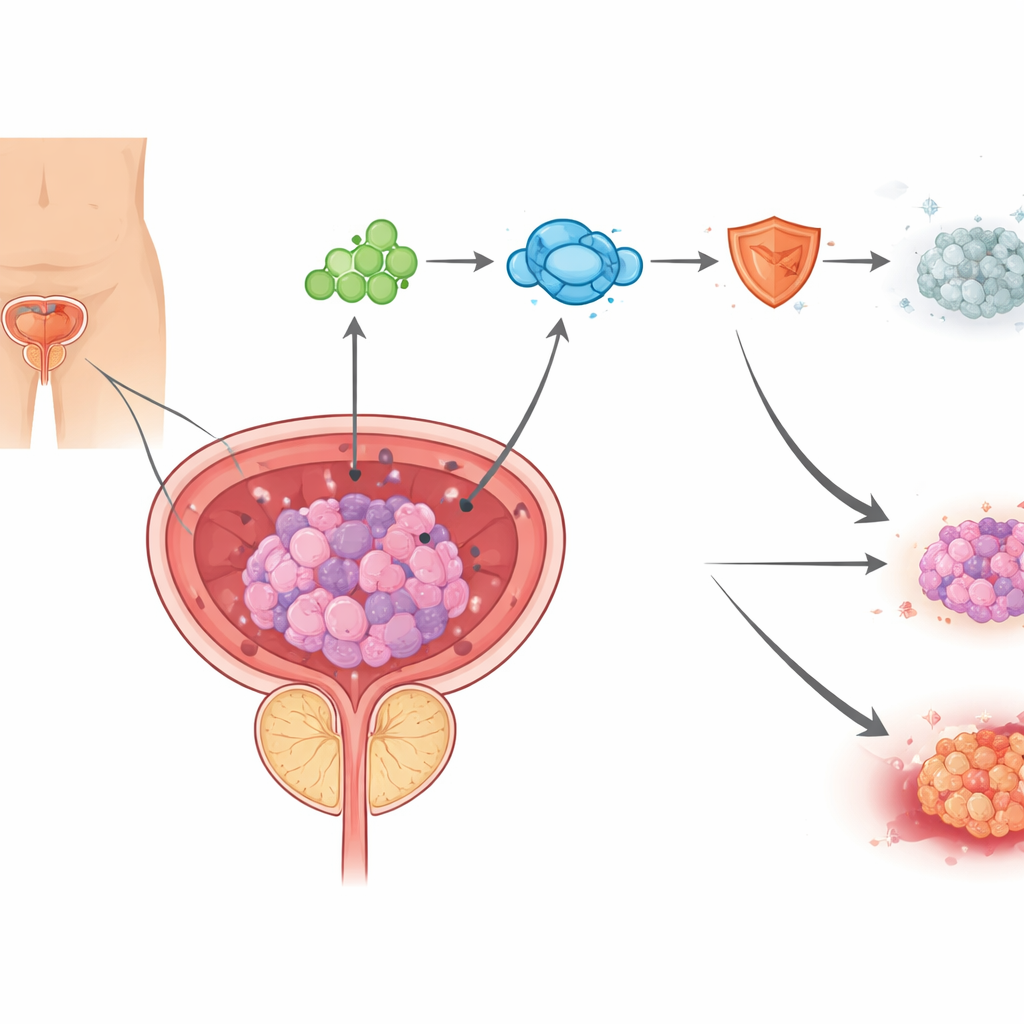
Een nieuw type celdood aangedreven door koper
Cellen kunnen op veel verschillende manieren sterven, en de moderne kankeronderzoek richt zich steeds vaker op het weer activeren van deze natuurlijke doodsprogramma’s in tumorcellen. De auteurs concentreren zich op een recent beschreven vorm van celdood, cuproptose, die wordt getriggerd wanneer koper zich ophoopt in de mitochondriën, de krachtcentrales van de cel. In prostaatkankermonsters van patiënten die behandeld waren met androgenenblokkers vond het team aanwijzingen voor koperophoping en mitochondriale schade, samen met eiwitveranderingen die kenmerkend zijn voor cuproptose. In celkweken verhoogde enzalutamide de koperconcentraties en beschadigde mitochondriën, en een koperbindende verbinding kon de cellen voor een groot deel redden, wat aantoont dat enzalutamide prostaatkankercellen deels kan doden door ze in koper‑gedreven celdood te duwen.
Hoe tumoren kopers giftige effect afzwakken
Toch geven niet alle kankercellen toe. Door meerdere datasets van enzalutamide‑resistente prostaattumoren te doorzoeken en te focussen op genen die met cuproptose samenhangen, identificeerden de onderzoekers één opvallend eiwit: PDHA1, een kernonderdeel van het apparaat dat suikergeneratie omzet in acetyl‑CoA, een centraal bouwblok in de cel. PDHA1‑niveaus waren hoger in resistente tumoren, geassocieerd met slechtere overleving en agressievere ziekte, en werden zelf door enzalutamide verhoogd. In laboratoriumexperimenten maakte het omlaag brengen van PDHA1 kankercellen veel gevoeliger voor zowel enzalutamide als een direct cuproptose‑inducerend middel, terwijl het verhogen van PDHA1 ze moeilijker te doden maakte. In muizen krimpten tumoren met verlaagd PDHA1 veel sterker onder enzalutamide‑behandeling, wat bevestigt dat dit enzym tumoren helpt therapie te weerstaan in levende organismen.
Een metabool en epigenetisch schild tegen behandeling
Het team ontrafelde vervolgens hoe PDHA1 dit schild opbouwt. Aangezien PDHA1 bijdraagt aan de productie van acetyl‑CoA, onderzochten zij of het de manier waarop DNA wordt verpakt en afgelezen kan veranderen. Wanneer PDHA1 hoog was, stegen acetyl‑CoA‑niveaus en chemische “acetyl”‑labels op histoneiwitten, vooral op een merkteken dat met actieve genen geassocieerd is. Eén belangrijke begunstigde was SLC7A11, een transporter die cysteïne de cel in brengt om glutathion te maken, een belangrijke antioxidant. Met meer PDHA1 maakten cellen meer glutathion; met minder PDHA1 daalden cysteïne en glutathion. Glutathion bond op zijn beurt koper en neutraliseerde het, waardoor de stress die cuproptose triggert verminderd werd. Het herstellen van glutathion of SLC7A11 kon de verhoogde koperstress ongedaan maken die optrad wanneer PDHA1 werd geblokkeerd, wat aantoont dat een PDHA1–acetyl‑CoA–histone–SLC7A11–glutathion keten kankercellen in staat stelt koper op te nemen en de dood te ontlopen.
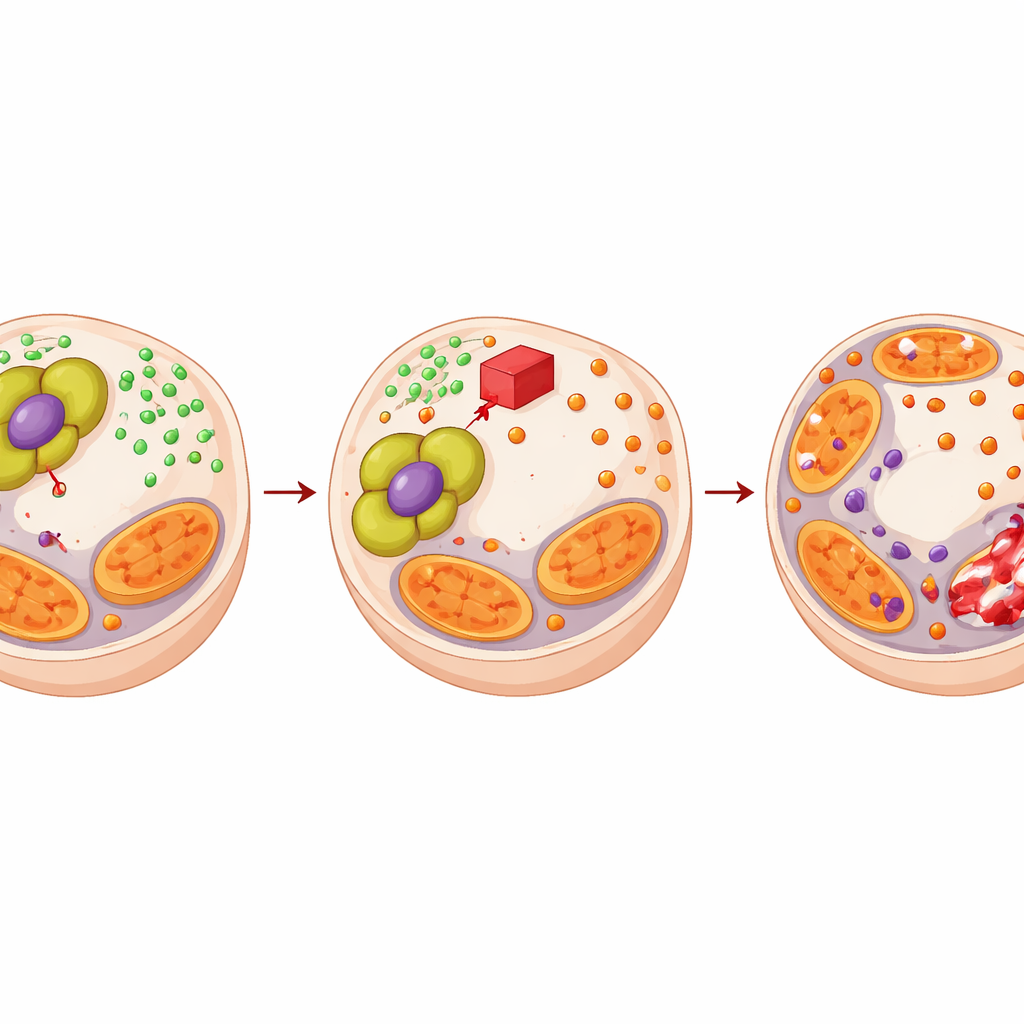
Een kwetsbaarheid omzetten in een therapeutische strategie
Aangezien PDHA1 tumoren helpt resistent te worden tegen enzalutamide door dit koperbufferende systeem te versterken, vroegen de auteurs zich af of een PDHA1‑gerichte therapie het tij kon keren. Ze gebruikten CPI‑613, een verbinding die hetzelfde metabole complex verstoort. CPI‑613 alleen verhoogde de koperstress en beschadigde mitochondriale eiwitten in prostaatkankercellen, maar spaarde normale prostaatcellen. In combinatie met enzalutamide remde CPI‑613 de kankercelgroei veel sterker dan één van beide behandelingen alleen, met wiskundige analyses die echte synergie bevestigden. In muismodellen en patiënt‑afgeleide tumorimplantaten leverde het combinatietherapiepaar kleinere tumoren, meer dood weefsel, minder delende cellen en sterkere signalen van koper‑gedreven celdood op.
Wat dit betekent voor patiënten
Gezamenlijk tonen deze bevindingen aan dat sommige prostaatkankers aan enzalutamide ontsnappen door hun metabolisme te herprogrammeren om meer acetyl‑CoA aan te maken, genactiviteit te herschrijven en glutathion te verhogen, waardoor toxisch koper wordt opgenomen en cuproptose wordt geblokkeerd. Door PDHA1 te remmen kan dit beschermende circuit worden ontmanteld, waardoor koper‑gedreven celdood kan plaatsvinden en het effect van hormoonblokkerende therapie wordt hersteld. Hoewel klinische studies nog nodig zijn, wijst het werk op een concrete, toetsbare strategie: enzalutamide combineren met PDHA1‑gerichte middelen zoals CPI‑613 om resistentie te overwinnen bij mannen met gevorderde, moeilijk te behandelen prostaatkanker.
Bronvermelding: Zhuang, R., Zhou, Q., Cheng, B. et al. PDHA1–acetylation signaling suppresses cuproptosis to attenuate anti-androgen effect in prostate cancer. Cell Death Dis 17, 243 (2026). https://doi.org/10.1038/s41419-026-08462-1
Trefwoorden: prostaatkanker, medicatieresistentie, kopergeïnduceerde celdood, kankermetabolisme, epigenetische regulatie