Clear Sky Science · nl
Endotheliale IRE1‑signaleringsroutes behouden de integriteit van de bloed‑hersenbarrière en beperken neuroinflammatie na traumatisch hersenletsel
Waarom het beschermen van de binnenwand van de hersenen ertoe doet
Na een klap tegen het hoofd is de onmiddellijke schade slechts een deel van het verhaal. In de uren en dagen daarna zet de hersenen een sterke stress‑ en immuunreactie in gang die het letsel stilletjes kan uitbreiden. Deze studie onderzoekt hoe een klein stress‑sensorisch systeem in de cellen die de bloedvaten in de hersenen bekleden helpt om de binnenwand van de hersenen — de bloed‑hersenbarrière — gesloten en rustig te houden na traumatisch hersenletsel. Inzicht in deze verborgen verdediging kan wijzen op nieuwe behandelingen die blijvende beperkingen na een hoofdtrauma beperken.
De poortwachters van de hersenen onder stress
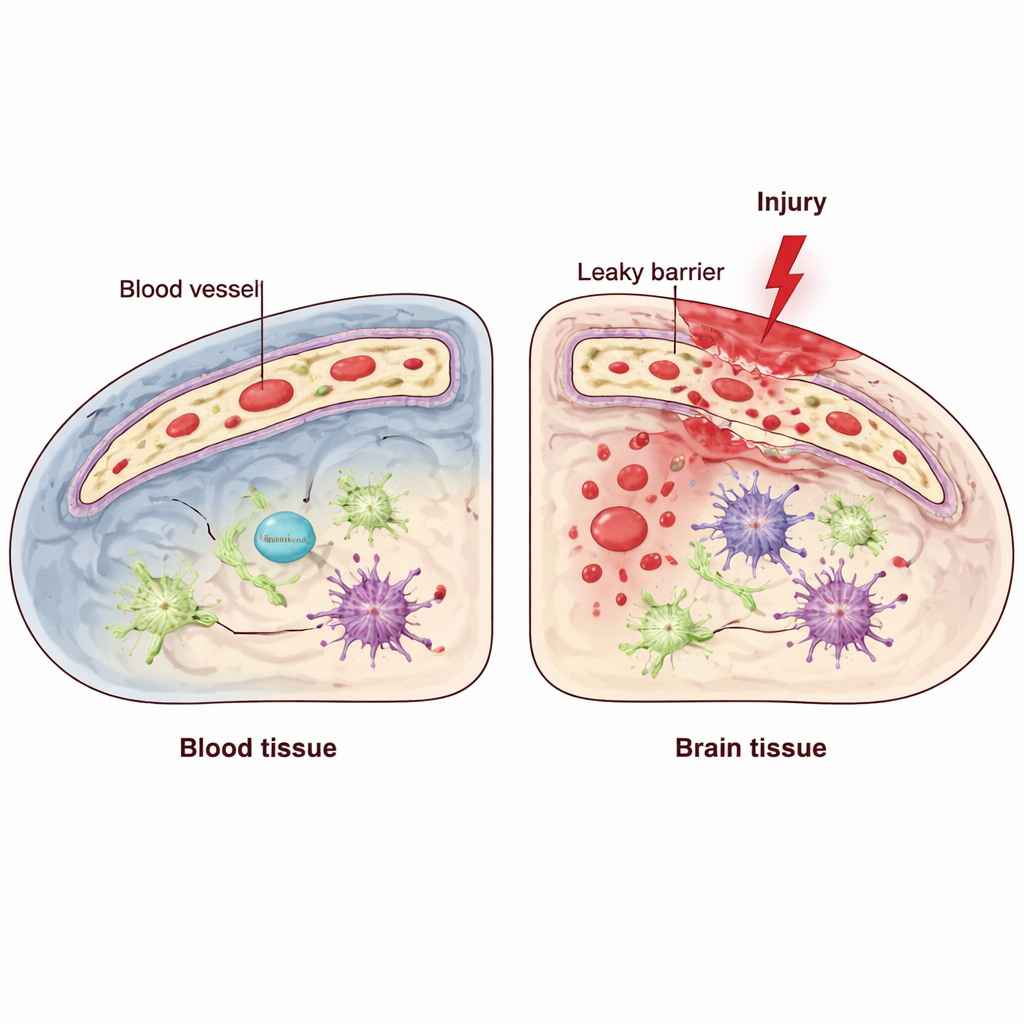
De hersenen vertrouwen op een gespecialiseerde barrière gevormd door endotheelcellen, die de binnenkant van bloedvaten bekleden en strikt controleren wat van het bloed naar het hersenweefsel kan passeren. Traumatisch hersenletsel (TBI) kan deze bloed‑hersenbarrière verstoren, waardoor ontstekingsmoleculen en immuuncellen naar binnen kunnen stromen en de schade verergeren. In deze endotheelcellen bevindt zich een kwaliteitscontrolesysteem, de unfolded protein response, dat cellen helpt omgaan met stress in een structuur die het endoplasmatisch reticulum heet. Een van de sleutelcomponenten, bekend als IRE1, fungeert als sensor en regelaar wanneer cellen onder druk staan. De onderzoekers vroegen zich af: helpt deze endotheliale stresssensor de barrière te verdedigen na TBI, of maakt hij de situatie juist erger?
Een cellulaire sensor uitschakelen in vaatcellen
Om dat te onderzoeken gebruikten de onderzoekers genetisch gemodificeerde muizen waarbij IRE1 selectief alleen in endotheelcellen kon worden uitgeschakeld. Vervolgens brachten ze een gecontroleerd letsel aan in het motorische gebied van de cortex, waarmee aspecten van menselijk TBI werden nagebootst, en vergeleken deze muizen met normale nestgenoten. Ze testten beweging met taken die evenwicht en nauwkeurige pootplaatsing meten, en onderzochten hersenweefsel met hogeresolutiemicroscopie en moleculaire technieken. Bij normale muizen nam de IRE1‑activiteit kort na het trauma toe in bloedvatcellen nabij het letsel, wat suggereert dat endotheelcellen snel stress waarnemen en erop reageren. Wanneer IRE1 specifiek in deze cellen ontbrak, presteerden de dieren slechter op motorische tests, wat op een mindere functionele herstel wijst.
Lekkende vaten, meer immuuncellen en stervende neuronen
De onderzoekers onderzochten vervolgens hoe goed de bloed‑hersenbarrière zich hield. Normaal blijven grote bloed‑eiwitten zoals antilichamen binnen de vaten. Na TBI is enige lekkage rondom de laesie te verwachten, maar muizen zonder endotheliale IRE1 toonden veel wijdere doorgifte van deze eiwitten naar de hersenen. Microscopie toonde dat een sleuteljunction‑molecuul, VE‑cadherine, dat endotheelcellen helpt afdichten, verminderd was in het beschadigde gebied wanneer IRE1 afwezig was, hoewel het totale aantal vaten vergelijkbaar leek. Deze lekkage ging gepaard met een instroom van immuuncellen in de hersenen rondom de laesie en hogere niveaus van ontstekingssignalen. In diezelfde regio’s toonden neuronen vaker tekenen van degeneratie en geprogrammeerde celdood, en de zone van beschadigd weefsel rond het kernletsels was duidelijk groter.
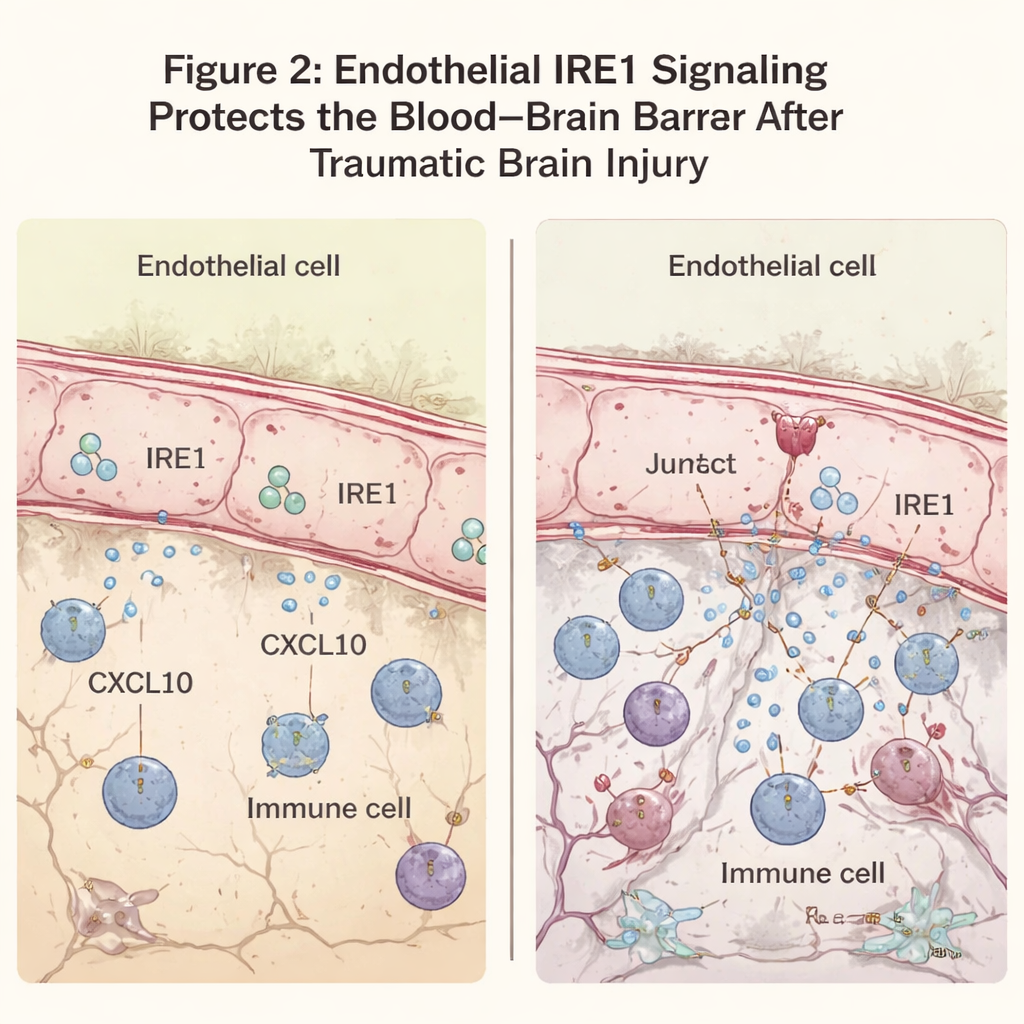
Een stressremmend middel dempt de signaalstorm
Om de moleculaire mechanismen te begrijpen analyseerde het team welke genen werden aangezet na het letsel. Bij muizen zonder endotheliale IRE1 waren genen die betrokken zijn bij antivirale en ontstekingsreacties sterk verhoogd. Opvallend was CXCL10, een chemokine — een soort moleculaire seinvlag — die immuuncellen aantrekt en de barrière verder kan verzwakken. CXCL10 was bijzonder verhoogd in endotheelcellen nabij de laesie wanneer IRE1 ontbrak. In gekweekte hersen‑endotheelcellen die werden blootgesteld aan een inflammatoire trigger, verlaagde het verminderen van endoplasmatisch reticulum‑stress met een middel genaamd TUDCA zowel IRE1‑activiteit als CXCL10‑productie. Toegediend aan gewonde muizen verminderde TUDCA CXCL10 en markers voor immuuncellen in de beschadigde cortex en verbeterde de motorische prestaties, wat suggereert dat het dempen van deze stressroute de secundaire schade kan verzachten.
Wat dit betekent voor mensen met hoofdletsels
Simpel gezegd suggereert dit werk dat de stresssensor IRE1 in de cellen die de bloedvaten van de hersenen bekleden optreedt als een beschermer na traumatisch hersenletsel. Als hij aanwezig en functioneel is, helpt hij de bloed‑hersenbarrière strak te houden, vermindert hij de afgifte van chemische signalen die immuuncellen aantrekken, en beperkt hij de verspreiding van ontsteking en neuronverlies rond de laesie. Wanneer hij is uitgeschakeld, wordt de barrière lekker, stromen immuuncellen naar binnen en raakt meer hersenweefsel beschadigd. Omdat vaatcellen relatief toegankelijk zijn voor geneesmiddelen die in de bloedbaan circuleren, zou het richten op hun stressreacties — met verbindingen zoals TUDCA of meer gerichte toekomstige therapieën — een praktische strategie kunnen worden om langdurige schade na een hoofdtrauma te verminderen.
Bronvermelding: Fan, Q., Takarada-Iemata, M., Tanaka, T. et al. Endothelial IRE1 signaling maintains blood–brain barrier integrity and limits neuroinflammation after traumatic brain injury. Cell Death Dis 17, 210 (2026). https://doi.org/10.1038/s41419-026-08461-2
Trefwoorden: traumatisch hersenletsel, bloed‑hersenbarrière, endothelcellen, neuroinflammatie, cellulaire stress