Clear Sky Science · nl
CD36 verhoogt de gevoeligheid van triple-negatieve borstkankercellen voor palmitaat-geïnduceerde ferroptose
Waarom vet rond tumoren zowel vriend als vijand kan zijn
Borsttumoren groeien in weefsel dat van nature rijk is aan vet, en kankercellen staan erom bekend dat ze ‘voeden’ op nabije vetzuren. Deze studie onderzoekt een verrassende wending: onder de juiste omstandigheden kan een van de meest voorkomende vetten in het lichaam, palmitinezuur, juist helpen een bijzonder agressieve vorm van borstkanker te doden door een specifiek soort celdood te activeren. Begrijpen hoe dit gebeurt kan wijzen op nieuwe behandelingen voor patiënten met momenteel weinig opties.
Een moeilijk te behandelen borstkanker onder de microscoop
Triple-negatieve borstkanker (TNBC) ontbreekt de hormoon- en groeifactorreceptoren waarop veel moderne geneesmiddelen mikken, waardoor het een van de lastigste borstkankertypen is om te behandelen. Deze tumoren leven in nauwe nabijheid van vetcellen, die grote hoeveelheden vetzuren afgeven, waaronder het verzadigde vet palmitinezuur. De onderzoekers wilden weten of palmitinezuur louter de tumorgroei voedt, of dat het ook een zwakte kan creëren die benut kan worden om kankercellen te doden.
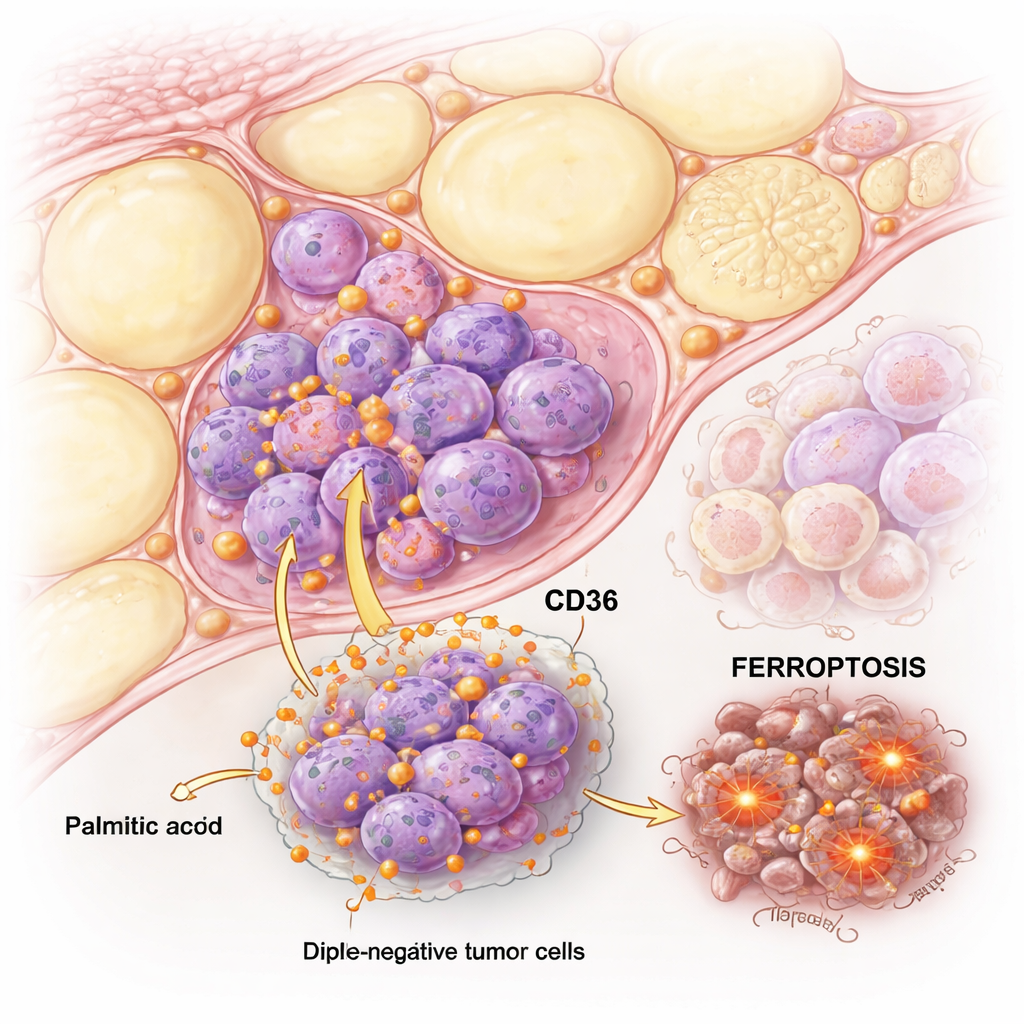
Wanneer palmitinezuur kankercellen over de rand duwt
Het team vergeleek TNBC-cellen met hormoongevoelige ‘luminale’ borstkankercellen en stelde ze bloot aan toenemende hoeveelheden palmitinezuur. Beide celtypen konden door hoge dosissen worden beschadigd, maar TNBC-cellen waren veel gevoeliger. Gedetailleerde tests toonden aan dat palmitinezuur in luminale cellen voornamelijk klassieke apoptose opwekte, een nette vorm van celdood. In TNBC-cellen zette palmitinezuur daarentegen zowel apoptose als een minder bekend pad in gang, ferroptose, dat afhankelijk is van ijzer en de vernietiging van vetten in het celmembraan.
Een poort voor vetzuren genaamd CD36
Om te begrijpen waarom TNBC-cellen zo anders reageerden, richtten de onderzoekers zich op CD36, een eiwit op het celoppervlak dat fungeert als een poort voor langeketenvetzuren. TNBC-cellen droegen van nature veel meer CD36 dan luminale cellen, en blootstelling aan palmitinezuur dreef het CD36-gehalte nog verder omhoog. Dit betekende dat TNBC-cellen meer palmitinezuur opnamen, meer beschadigde lipiden ophoopten, meer reactieve zuurstof in hun mitochondriën produceerden en meer vrij ijzer binnen de cel verzamelden—allemaal belangrijke signalen van ferroptose. Toen CD36 werd geblokkeerd met een geneesmiddel of verminderd met genetische middelen, daalde palmitinezuur-geïnduceerde ferroptose sterk.
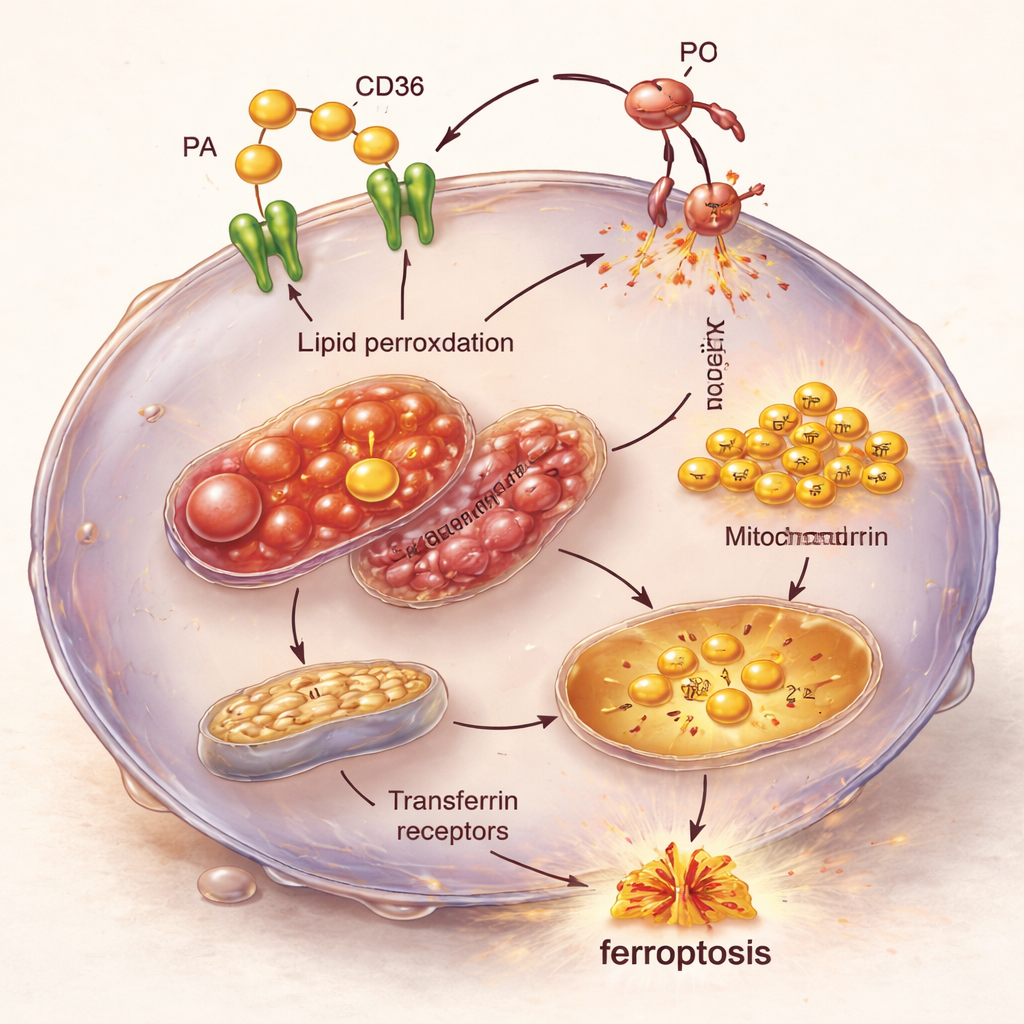
Inzoomen op de kettingreactie binnenin de cel
Microscopie en genactiviteitsanalyses onthulden de interne kettingreactie achter deze kwetsbaarheid. TNBC-cellen die overbelast waren met palmitinezuur en CD36 toonden gezwollen, structureel beschadigde mitochondriën en toenemende niveaus van ijzer, aangevoerd via transferrinereceptoren. Tegelijkertijd werden genen die ferroptose bevorderen aangeschakeld, terwijl genen die normaal beschermen tegen deze vorm van celdood omlaag werden bijgesteld. Het resultaat is een perfecte storm: teveel binnenkomend vet, meer beschikbaar ijzer om chemische reacties aan te jagen, en verzwakte verdedigingen tegen lipidedetectie, die samen TNBC-cellen in ferroptose duwen.
Welke patiënten zouden het meest kunnen profiteren?
Kanker is niet uniform, zelfs niet binnen TNBC. Met behulp van tumorstalen gekweekt in muizen en grote patiëntendatabases, vonden de auteurs dat CD36 vooral hoog was in een bepaald TNBC-subtype genaamd luminal androgen receptor (LAR), dat al eerder was opgemerkt als gevoeliger voor ferroptose. Andere TNBC-subtypen met hoge ijzeropname vertoonden ook vaak hogere CD36-niveaus. Dit patroon suggereert dat CD36 kan dienen als een merker om patiënten te identificeren van wie de tumoren van nature vatbaar zijn voor therapieën die op ferroptose mikken.
Een veelvoorkomend vet veranderen in een therapeutische bondgenoot
Kort gezegd laat dit werk zien dat een overvloedig voedings- en lichaamvet, palmitinezuur, kan helpen bepaalde triple-negatieve borstkankercellen te doden wanneer ze hoge niveaus van de vettransporter CD36 tot expressie brengen. Door vetoverbelasting, ijzerophoping en schade aan celmembranen te veroorzaken, maakt CD36 deze kankercellen vatbaarder voor ferroptose—een verwoestend lot waar ze niet aan kunnen ontsnappen. Als toekomstige behandelingen deze route veilig kunnen versterken—of combineren met geneesmiddelen die de verdediging van de cellen verder verzwakken—kunnen clinici een metabole zwakte omzetten in een nieuwe, nauwkeurigere manier om enkele van de meest agressieve borstkankers aan te pakken.
Bronvermelding: Closset, L., Foy, JP., Louadj, L. et al. CD36 enhances sensitivity of triple negative breast cancer cells to palmitate-induced ferroptosis. Cell Death Dis 17, 219 (2026). https://doi.org/10.1038/s41419-026-08460-3
Trefwoorden: triple-negatieve borstkanker, ferroptose, CD36, palmitinezuur, tumormetabolisme