Clear Sky Science · nl
USP30-gemedieerde deubiquitinering van hexokinase 2 bepaalt het metabolische lot van glucose en de tumorprogressie
Hoe kankercellen hun suikergebruik herbedraden
Kankercellen staan bekend om hun "zoetekauw": ze verbranden suiker op ongebruikelijke manieren om snelle groei aan te sturen. Deze studie onthult een nieuwe schakelaar, een eiwit genaamd USP30, die tumorcellen helpt beslissen hoe ze glucose gebruiken. Door een ander eiwit, hexokinase 2 (HK2), precies bij te sturen, kan USP30 kankercellen ertoe zetten meer suiker te verbranden en sneller te groeien, wat wijst op een nieuw doel voor toekomstige antikankermedicatie. 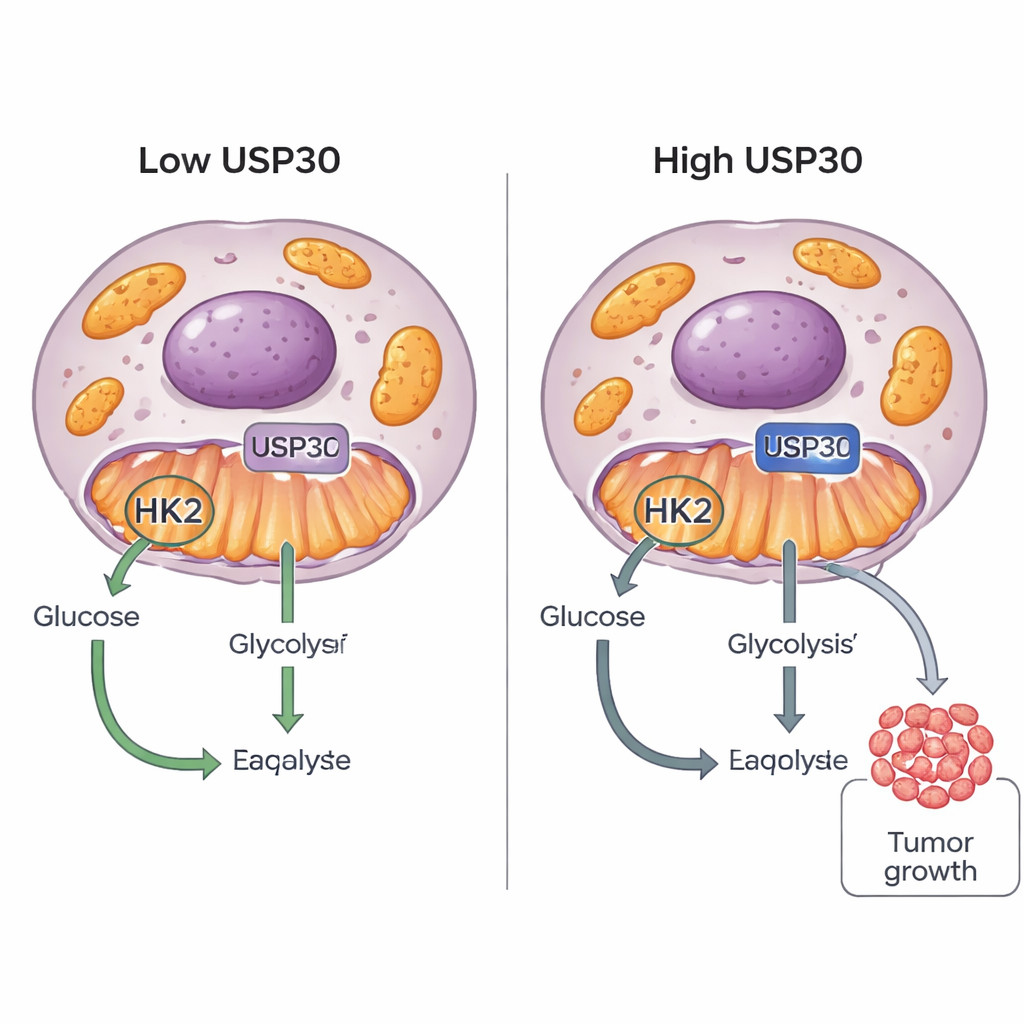
Een suikergierige levensstijl in tumoren
De meeste gezonde cellen winnen efficiënt energie uit voedingsstoffen, maar veel kankercellen geven de voorkeur aan een snelle, minder efficiënte route die aerobe glycolyse wordt genoemd, ook wel het Warburg-effect. Ze nemen grote hoeveelheden glucose op en zetten die snel om in lactaat, zelfs als er voldoende zuurstof aanwezig is. Deze strategie levert meer dan alleen energie: ze levert bouwstenen voor DNA, vetten en eiwitten, helpt tumoren stress te doorstaan en kan zelfs immuunaanvallen verzwakken. Bij de toegangspoort tot deze route bevindt zich hexokinase, een enzym dat binnenkomende glucose voorziet van een fosfaatgroep en het daarmee toewijdt aan verdere afbraak en groeiondersteunende chemie.
Een mitochondriaal enzym in de schijnwerpers
USP30 is een enzym dat op het buitenoppervlak van mitochondriën zit, de energiecentrales van de cel. Het behoort tot een familie van "deubiquitinases" die kleine proteïnetags, ubiquitine, van andere eiwitten verwijderen, wat vaak hun stabiliteit, locatie of activiteit verandert. USP30 was al bekend om rollen in hersencellen en in het controleren van mitochondriale kwaliteit, maar de invloed op kanker was onduidelijk. Door grote kankergen-databases te doorzoeken, zagen de onderzoekers dat tumoren met hogere USP30-niveaus vaker sterke glucose-verbrandingssignaturen en zwakkere vetverbrandingssignaturen vertoonden, wat suggereert dat USP30 tumoren helpt verschuiven naar een suiker-gedreven levensstijl.
USP30 koppelen aan de suikerpoortwachters van de cel
Om deze link te onderzoeken verlaagde of verwijderde het team USP30 in verschillende kankercellijnen en mat hoe ze energie verwerkten. Met instrumenten die zuurproductie en zuurstofgebruik in real time volgen, ontdekten ze dat verlies van USP30 zowel de glycolyse als de mitochondriale respiratie sterk verminderde. Lactaatproductie en glucoseverbruik daalden, wat aantoont dat de suikerverbrandingsmotor van de cellen vertraagde. Een reeks massaspectrometrie-experimenten toonde vervolgens aan dat USP30 fysiek interacteert met meerdere enzymen die met glucosemetabolisme te maken hebben, vooral de hexokines HK1 en HK2. vervolgtests lieten zien dat deze interactie afhankelijk is van de katalytische activiteit van USP30 en direct plaatsvindt, niet alleen via tussenliggende partners.
Een nauwkeurig moleculair handvat op hexokinase 2
Dieper onderzoek toonde aan dat USP30 specifieke typen ubiquitineketens verwijdert — zogenoemde atypische verbindingen — van HK1 en HK2. Voor HK2 vindt deze bewerking plaats op één cruciaal aminozuur, lysine 144 (K144). Wanneer K144 gemuteerd is zodat het geen ubiquitine meer kan dragen, wordt HK2 stabieler, bindt het sterker aan een kanaaleiwit genaamd VDAC1 op mitochondriën en vertoont het hogere enzymatische activiteit. Cellen die dit K144-mutant droegen stuurden meer HK2 naar mitochondriën, verbrandden meer glucose, produceerden meer lactaat en toonden snellere groei en beweeglijkheid in kweek. Bij muizen groeiden tumoren die uit cellen met het K144-mutant waren voortgekomen groter en sneller dan tumoren met normale HK2, wat de impact van deze kleine moleculaire schakelaar benadrukt. 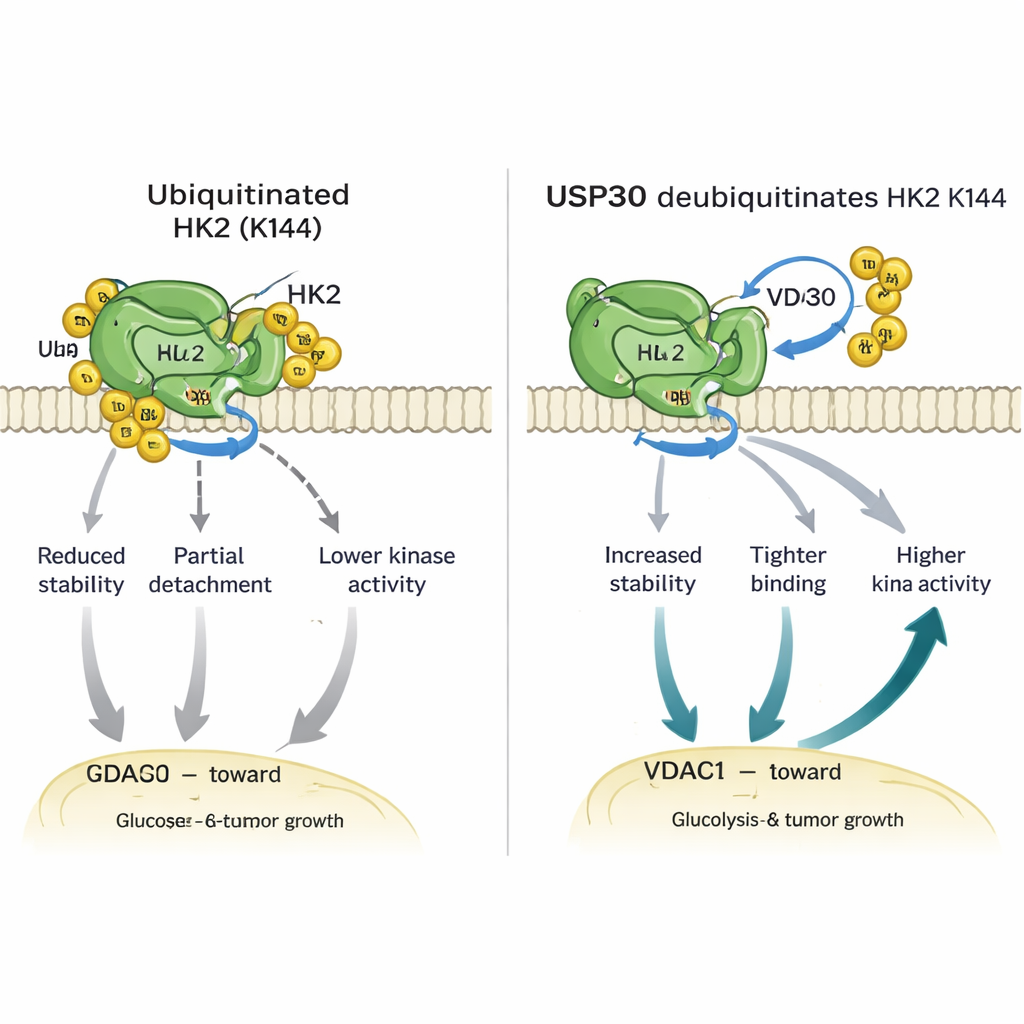
Een metabole schakelaar omgezet in een groeivoordeel
Deze resultaten schetsen een duidelijke keten van gebeurtenissen: USP30 bindt aan HK2, verwijdert ubiquitinetags van K144 en houdt HK2 daarmee actief en verankerd op mitochondriën. Dit verhoogt de glycolyse, voedt deling en migratie van tumorcellen en versnelt uiteindelijk de tumorgroei. Wanneer USP30 ontbreekt of inactief is, wordt HK2 minder stabiel en minder effectief, en verliezen kankercellen een deel van hun metabolische voorsprong. In gewone taal werkt USP30 als een monteur die de suiker-motor van de kankercel afstelt en vastzet — verwijder je de monteur, dan sputtert de motor.
Wat dit betekent voor toekomstige kankerbehandelingen
Voor niet-specialisten is de belangrijkste conclusie dat kankercellen afhankelijk zijn van nauwkeurige controle over hoe ze suiker verbranden, en dat USP30 een nieuw ontdekte draaiknop op dat bedieningspaneel is. Door HK2 op één specifieke plaats te stabiliseren, helpt USP30 tumoren hun glucose-hongerige metabolisme te laten draaien en agressiever te groeien. Medicijnen die USP30 blokkeren, of die zijn greep op HK2 bij lysine 144 verstoren, zouden tumoren kunnen verzwakken door hun suiker-motor uit te hongeren, zonder normale cellen evenveel te schaden. Dit werk voegt daarmee een belangrijk puzzelstuk toe aan het begrip van hoe kanker het metabolisme herschakelt en suggereert een veelbelovende nieuwe invalshoek voor gerichte therapieën.
Bronvermelding: Haowei, Z., Li, X., Liao, W. et al. USP30-mediated Deubiquitination of Hexokinase 2 controls the metabolic fate of glucose and tumor progression. Cell Death Dis 17, 225 (2026). https://doi.org/10.1038/s41419-026-08459-w
Trefwoorden: kankermetabolisme, glycolyse, hexokinase 2, USP30, Warburg-effect