Clear Sky Science · nl
Oocyte-specifieke knock-out van eIF2-subunits veroorzaakt apoptose van muis-oocyten in vroeggroeiende follikels door mitochondriale disfuncties en DNA-schade
Waarom het leven van eicellen ertoe doet
Vrouwen worden geboren met alle eicellen die ze ooit zullen hebben, opgeslagen in kleine structuren in de eierstok die follikels heten. Wanneer deze follikels te snel verloren gaan, kunnen vrouwen prematuur ovarieel falen (POI) ontwikkelen — een aandoening die leidt tot vroege onvruchtbaarheid en vaak vroeg optredende menopauzeachtige klachten. Deze muizenstudie stelt een eenvoudig maar cruciaal vraagstuk: wat gebeurt er in eicellen wanneer een sleutelstap bij het maken van nieuwe eiwitten misgaat, en hoe kan dat leiden tot vroeg verlies van vruchtbaarheid?
De eiwitstartschakel van de cel
Om gezond te blijven moeten eicellen voortdurend de juiste eiwitten op het juiste moment aanmaken. Een centraal onderdeel van dit proces is een drievoudig moleculair complex genaamd eIF2, dat helpt bij het starten van eiwitproductie vanaf genetische boodschappen. De onderzoekers schakelden selectief twee onderdelen van eIF2 uit, eIF2α en eIF2β, alleen in muis-oocyten in de vroege stadia van follikelgroei. Wanneer een van beide subunits ontbrak, werden vrouwelijke muizen volledig onvruchtbaar. Hun eierstokken waren kleiner en de normale overgang van vroege follikels naar rijpe, eicel-afgevende follikels stokte grotendeels, met veel minder follikels in ieder volgend stadium. Na verloop van tijd raakten in wezen alle follikels uitgeput, wat een ernstige, vroeg optredende POI-achtige toestand nabootst.
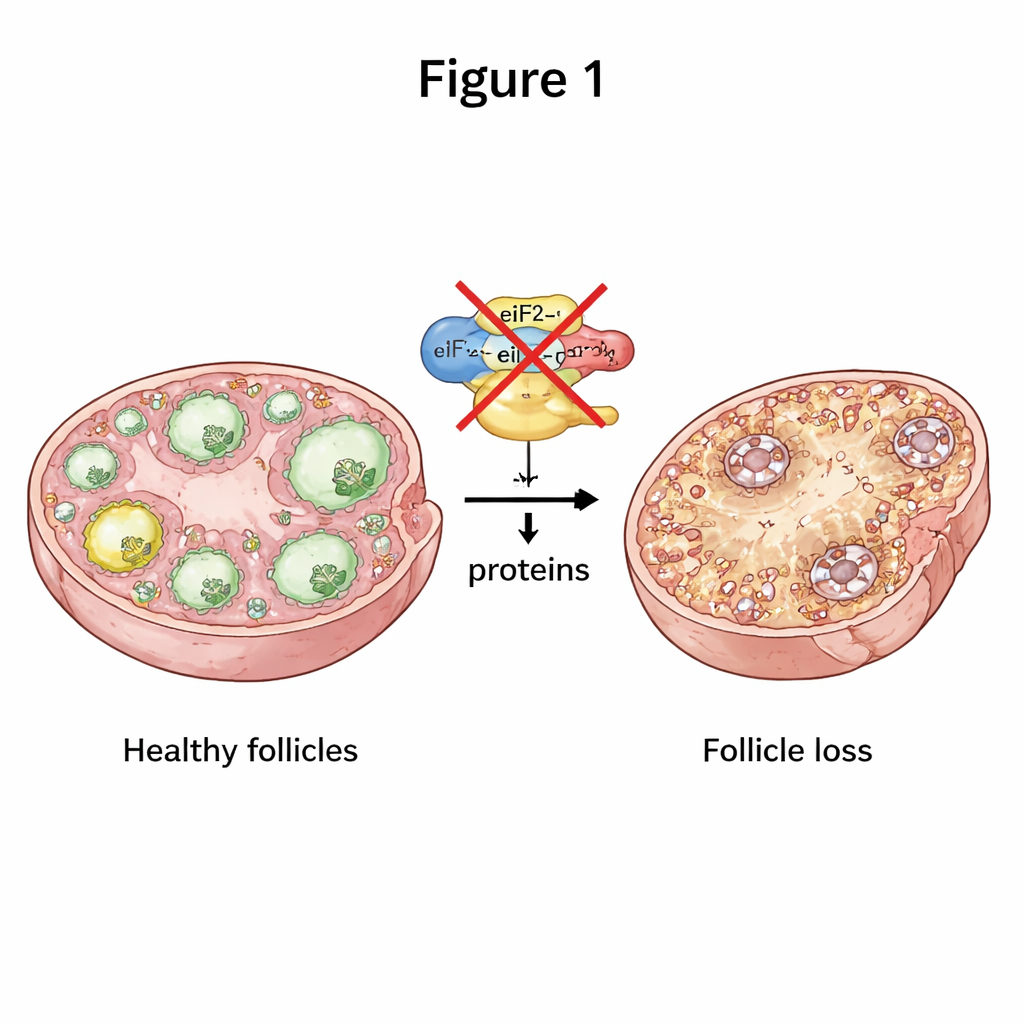
Wanneer communicatie in de eierstok faalt
Follikels zijn niet alleen eicellen die afzonderlijk zweven; het zijn nauwe samenwerkingen tussen een eicel en omliggende 'hulp'-cellen, de granulosa-cellen. Het team ontdekte dat zonder eIF2β oocyten veel minder van verschillende cruciale signaaleiwitten produceerden die normaal de groei van granulosa-cellen en de toevoer van voedingsstoffen ondersteunen. De fysieke bruggen tussen eicel en granulosa-cellen waren gedesorganiseerd en verkort, en de microvilli aan het oppervlak van de eicel leken geremd en beschadigd onder de elektronenmicroscoop. Granulosa-cellen in deze follikels deelden minder en stierven vaker. Deze ineenstorting van tweerichtingscommunicatie betekende dat de follikels niet goed konden groeien, waardoor de eierstok naar follikelverlies werd geduwd.
Stroomuitval in de batterijen van de eicel
Mitochondriën, vaak cellen’ energiecentrales genoemd, zijn bijzonder belangrijk in eicellen omdat ze de energie leveren die nodig is voor groei en latere embryo-ontwikkeling. In eIF2β-deficiënte oocyten daalde de algehele snelheid van nieuwe eiwitproductie en waren veel mitochondriale eiwitten verminderd. Mitochondriën werden abnormaal lang, klonterden dicht bij het celoppervlak en toonden een zwakkere membraanpotentiaal, lagere energie (ATP)-niveaus en minder kopieën van mitochondriaal DNA. Tegelijkertijd stapelden de cellen hoge niveaus reactieve zuurstofsoorten (ROS) op, agressieve zuurstofgebaseerde moleculen die cellulaire componenten kunnen beschadigen. Samen wijzen deze veranderingen op een ingrijpende ineenstorting van mitochondriale dynamiek en functie.
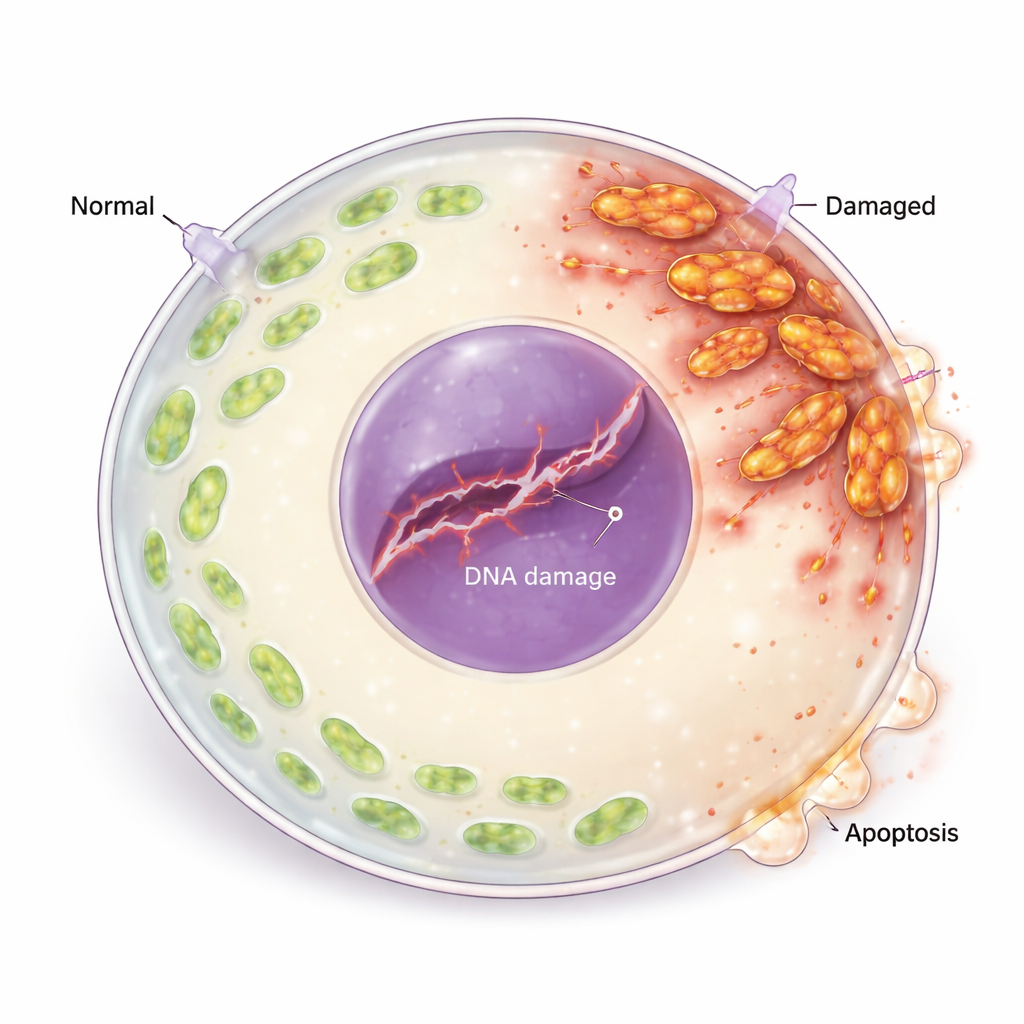
Van oxidatieve stress naar DNA-schade en celdood
Overmaat aan ROS schaadde niet alleen mitochondriën; het beschadigde ook het genetisch materiaal van de eicel. De onderzoekers zagen toegenomen markers van gebroken DNA-strengen en activering van het DNA-schade-responssysteem van de cel, inclusief eiwitten die genetisch letsel detecteren en signaleren. Een belangrijk reparatie-eiwit was verminderd, wat suggereert dat de schade niet efficiënt werd hersteld. Verderop in de keten verschoof de balans tussen levens- en doodregulatoren: pro-dood-eiwitten stegen terwijl beschermende anti-dood-eiwitten afnamen, en eicellen vertoonden duidelijke tekenen van geprogrammeerde celdood (apoptose). Toen het team de oocyten behandelde met een antioxidant (N-acetylcysteïne), daalden ROS-niveaus, namen DNA-schade- en apoptosemarkers af, en verbeterde de eicelmaturatie, wat oxidatieve stress rechtstreeks koppelt aan het verlies van eicellen.
Wat dit betekent voor vroeg ovarieel falen
Door gebeurtenissen te volgen van één moleculair complex (eIF2) via foutieve eiwitproductie, mitochondriale instorting, oxidatieve stress, DNA-schade en uiteindelijk celdood van eicellen, schetst dit werk een gedetailleerde keten van gebeurtenissen die de ovariumreserve kan vernietigen. De studie versterkt het idee dat mutaties in factoren die de start van vertaling reguleren, zoals al gezien bij sommige vrouwen met POI, eicellen rechtstreeks kunnen beschadigen via deze route. Het wijst ook op mogelijke benaderingen om te helpen: antioxidanten, modulatoren van stressreacties of behandelingen die vroege follikels beschermen (zoals anti-Mülleriaans hormoon, dat in deze muizen deels de slapende follikels bewaarde) zouden mogelijk ooit de vruchtbaarheid kunnen ondersteunen bij patiënten wier eierstokken kwetsbaar zijn voor vergelijkbare stressoren.
Bronvermelding: Liu, H., Wang, W., Li, B. et al. Oocyte-specific knockout of eIF2 subunits causes apoptosis of mouse oocytes within the early growing follicles via mitochondrial dysfunctions and DNA damage. Cell Death Dis 17, 196 (2026). https://doi.org/10.1038/s41419-026-08449-y
Trefwoorden: prematuur ovarieel falen, oocyt-apoptose, mitochondriale disfunctie, eiwitvertaling, reactieve zuurstofsoorten