Clear Sky Science · nl
Diploïde hepatocyten weerstaan door paracetamol veroorzaakte leverbeschadiging via geremde JNK-signaaltransductie
Waarom sommige magen beter tegen overdoses kunnen
Paracetamol (acetaminophen) ligt in talloze medicijnkastjes, maar te veel innemen is een belangrijke oorzaak van acute leverfalen. Deze studie stelt een schijnbaar eenvoudige vraag met grote implicaties: reageren alle levercellen op een overdosis op dezelfde manier? De onderzoekers tonen aan dat één specifiek type levercel, diploïde hepatocyten genoemd, verrassend goed bestand is tegen schade en effectiever herstel laat zien na een paracetamoloverdosis, dankzij een gedempte interne stressroute.
Twee soorten levercellen, twee verschillende lotgevallen
De lever is bijzonder omdat de meeste werkende cellen (hepatocyten) extra chromosoomsets dragen, waardoor ze polyploid zijn. Een kleiner deel blijft diploïde, met slechts twee chromosoomsets zoals de meeste lichaamscellen. Wetenschappers wisten dat deze groepen verschillen in hoe ze delen en regenereren, maar hun rol bij geneesmiddel-induced schade was onduidelijk. De auteurs gebruikten speciaal gefokte muizen waarvan de lever grotendeels uit diploïde cellen bestaat maar die verder normaal functioneren, en vergeleken die met typische muizen waarvan de lever vooral uit polyploïde cellen bestaat. Beide groepen kregen lage en hoge overdosisniveaus van paracetamol om te zien hoe hun lever in de tijd reageerde.
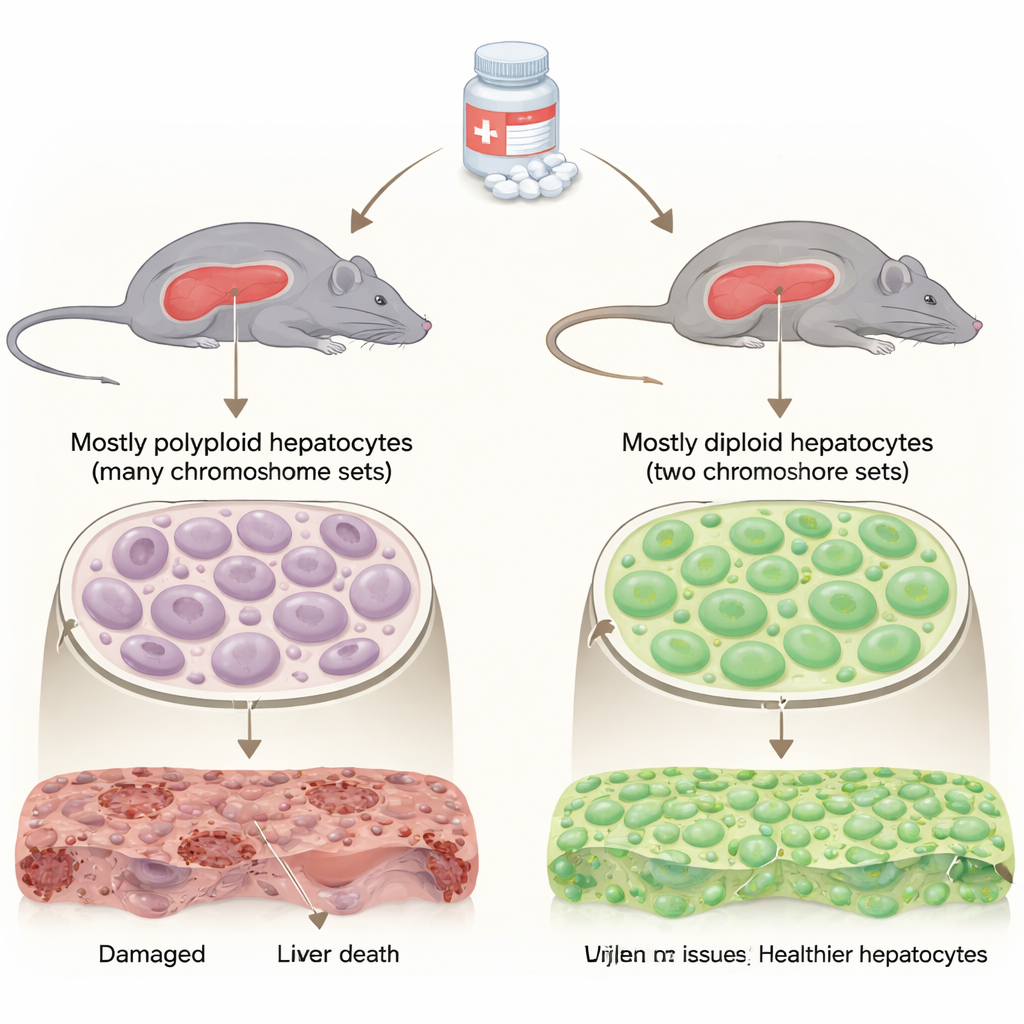
Levers rijk aan diploïde cellen overleven overdoses en herstellen sneller
Wanneer muizen een "regenererende" overdosis paracetamol kregen, lieten beide groepen leverbeschadiging zien, maar de diploïde-rijke muizen deden het veel beter. Ze hadden een hogere overleving, lagere niveaus van leverenzymen in het bloed (een teken van minder schade) en kleinere gebieden met dode weefselcellen en gefragmenteerd DNA onder de microscoop. Zelfs bij een zwaardere, "niet-regenererende" dosis—een dosis die gewoonlijk blijvende schade en sterfte veroorzaakt—overleefde meer dan de helft van de diploïde-rijke muizen, vergeleken met minder dan één op de tien van de controles. Ondanks deze bescherming lagen de diploïde-rijke levers niet stil: ze zetten vroegere expressie van eiwitten voor celdeling aan, wat suggereert dat ze zowel schade weerstaan als sneller met herbouwen beginnen.
Niet het medicijn zelf, maar de stressbedrading
Een voor de hand liggende mogelijkheid was dat diploïde-rijke levers gewoon paracetamol anders verwerkten. Het team mat sleutelenzymen die het geneesmiddel omzetten in het toxische bijproduct, niveaus van het beschermende molecuul glutathion, en de hoeveelheid medicijn gebonden aan levereiwitten. Al deze waarden waren vergelijkbaar tussen de twee muizentypen, wat betekent dat beide hetzelfde aantal toxische moleculen maakten en verwerkten. Het cruciale verschil verscheen later: in hoe cellen reageerden op dat toxische middel. In typische, polyploïde-rijke levers waren genen en eiwitten die betrokken zijn bij cellulaire stress, DNA-schade en mitochondriale beschadiging sterk geactiveerd. In diploïde-rijke levers waren deze reacties gedempt en losten ze eerder op, terwijl genen die aan regeneratie gelinkt zijn eerder aangingen.
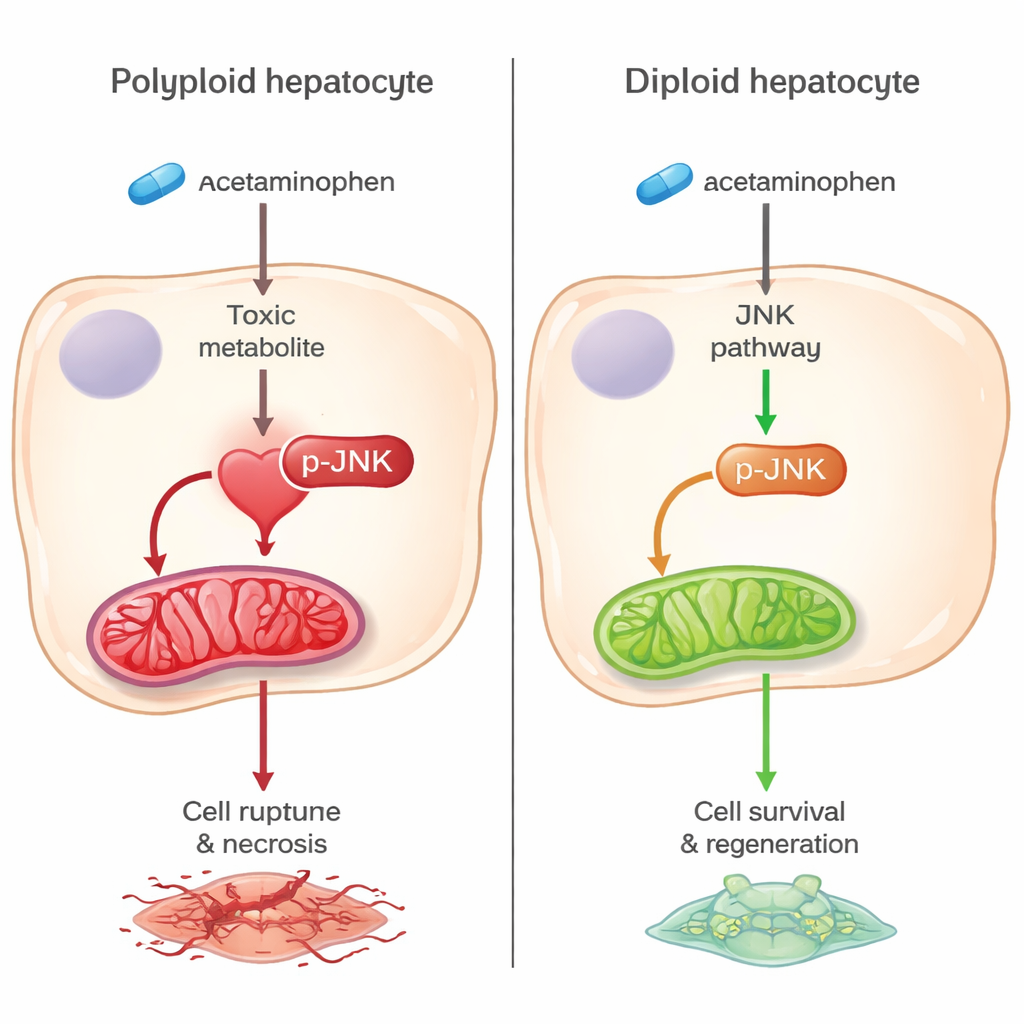
Een stillere celdoodroute beschermt diploïde cellen
De centrale speler in dit verschil is een stress-signaalroute bekend als het JNK-pad. In standaardlevers activeert het toxische bijproduct van paracetamol upstream-enzymen die JNK inschakelen, waarna JNK naar de mitochondriën verhuist, de energiecentrales van de cel, en daar oxidatieve schade en celdood bevordert. In diploïde-rijke levers was de activatie van deze upstream-enzymen en van JNK zelf sterk verminderd, en bereikte veel minder JNK de mitochondriën. Merkers van oxidatieve stress en mitochondriale afbraak waren ook lager, wat aangeeft dat deze energiecentrales beter intact bleven. Belangrijk is dat, wanneer dieselde genen alleen in volwassen levers werden verwijderd zonder de celploidie te veranderen, er geen bescherming optrad, wat erop wijst dat de overvloed aan diploïde cellen—niet de genmanipulatie zelf—de doorslaggevende factor is.
Waarom celtype ertoe doet bij leverbeschadiging bij mensen
Om te onderzoeken of dit patroon algemener geldt, zetten de onderzoekers normale muislevercellen die in petrischaaltjes waren gekweekt bloot aan paracetamol. Cellen met veel chromosoomsets (hoog polyploïde) stierven gemakkelijker, terwijl diploïde en laag-ploidiecellen meer geneigd waren te overleven. Gezamenlijk ondersteunen de bevindingen een model waarin diploïde hepatocyten de "eerstelijnsresponders" van de lever zijn bij plotselinge toxische schade: ze dempen een belangrijke celdoodroute, behouden hun mitochondriën en schakelen snel over naar regeneratie. Polyploïde cellen kunnen nog steeds nuttig zijn in andere situaties, zoals het beschermen tegen kanker of het aanpassen aan langdurige chronische schade. Maar bij een eenmalige overdosis kan een groter aandeel diploïde hepatocyten het verschil betekenen tussen herstel en leverfalen.
Bronvermelding: Wilson, S.R., Delgado, E.R., Alencastro, F. et al. Diploid hepatocytes resist acetaminophen-induced liver injury through suppressed JNK signaling. Cell Death Dis 17, 203 (2026). https://doi.org/10.1038/s41419-026-08448-z
Trefwoorden: paracetamol overdosis, leverbeschadiging, hepatocyten ploidie, JNK-signaaltransductie, leverregeneratie