Clear Sky Science · nl
Transglutaminase 2 verergert het overleven bij eierstokkanker door GSK3β direct te inactiveren
Waarom dit onderzoek van belang is voor de gezondheid van vrouwen
Eierstokkanker is een van de dodelijkste vormen van kanker bij vrouwen omdat de ziekte meestal laat wordt ontdekt en vaak terugkomt, zelfs na krachtige chemotherapie. Deze studie onthult hoe een weinig bekend eiwit, transglutaminase 2 (TGase 2), eierstokkankercellen helpt de behandeling te overleven en zich door het lichaam te verspreiden. Door deze verborgen bondgenoot van kanker bloot te leggen, wijst het werk op nieuwe wegen om bestaande geneesmiddelen effectiever te maken en om dodelijke metastasen te vertragen of te stoppen.
Een verborgen drijfveer in agressieve tumoren
Artsen merken al langer dat veel eierstokkankers resistent worden tegen chemotherapie en zich uitgebreid door de buikholte verspreiden. Een belangrijke boosdoener is een proces dat epithelial–mesenchymal transition (EMT) heet, waarbij kankercellen hun verbindingen losser maken, mobieler worden en zich meer gedragen als invasieve "zwervers" dan als georganiseerd weefsel. De auteurs tonen aan dat TGase 2, dat in normaal eierstokweefsel op heel lage niveaus voorkomt maar in eierstokkankers veel hoger is, sterk verband houdt met deze omschakeling. In een groot panel van menselijk weefsel stegen de TGase 2-niveaus gestaag van vroege tumoren naar gevorderde en gemetastaseerde ziekte, en de hoeveelheid kwam goed overeen met de activiteit van vele EMT-gerelateerde genen die celbeweging, groei en vaatvorming regelen. 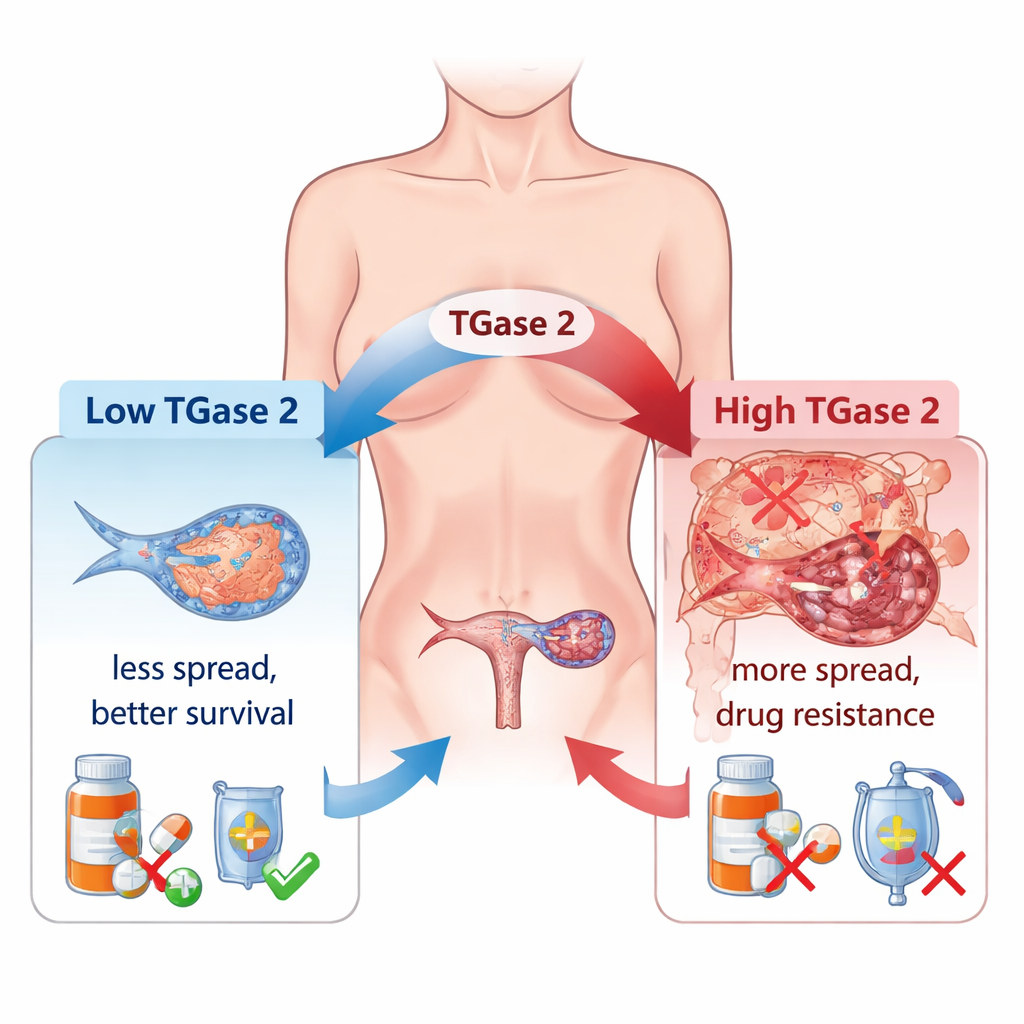
Hoe TGase 2 een belangrijke beveiligingsschakel uitschakelt
Om te begrijpen wat TGase 2 daadwerkelijk doet in kankercellen, richtten de onderzoekers zich op de relatie met een ander eiwit, GSK3β. Onder gezonde omstandigheden werkt GSK3β als een rem op invasie: het houdt de niveaus van het signaalmolecuul β-catenine laag, wat op zijn beurt genen die EMT aandrijven beperkt. Het team ontdekte dat TGase 2 fysiek aan GSK3β bindt en zowel diens activiteit verzwakt als bijdraagt aan de afbraak via het recyclingsysteem van de cel, een route die autophagie wordt genoemd. Wanneer TGase 2 overvloedig aanwezig was, migreerden eierstokkankercellen gemakkelijker en toonden ze hogere niveaus van klassieke EMT‑kenmerken zoals fibronectine, vimentine en β-catenine. Toen de onderzoekers TGase 2 met genetische middelen verminderden, daalden deze invasieve eigenschappen en werd β-catenine‑signaalgeving afgezwakt, wat aantoont dat TGase 2 een cruciale beveiligingsschakel tegen metastase uitschakelt.
Van kankercellen naar levende dieren
Vervolgens vroegen de onderzoekers of het blokkeren van TGase 2 kanker in dieren daadwerkelijk kon vertragen. Ze maakten eierstokkankercellen zonder het TGase 2-gen en implanteerden die in muizen. Vergeleken met muizen die normale kankercellen ontvingen, ontwikkelden dieren die TGase 2‑deficiënte cellen kregen kleinere tumoren en leefden ze langer. In een apart model dat de verspreiding van kanker via de bloedbaan nabootst, ontwikkelden muizen die TGase 2‑deficiënte cellen kregen veel minder en kleinere longmetastasen. Belangrijk is dat deze metastatische afzettingen hogere niveaus van GSK3β vertoonden, wat past bij het idee dat het wegnemen van TGase 2 de natuurlijke rem op invasie herstelt en helpt de ziekte te beperken.
Een laboratoriumhint naar een geneesmiddelstrategie
Aangezien het verwijderen van een gen bij patiënten niet praktisch is, testten de auteurs een kleine molecule genaamd streptonigrine, waarvan eerder bekend was dat die bindt aan hetzelfde uiteinde van TGase 2 dat wordt gebruikt om andere eiwitten vast te pakken. Ze ontdekten dat streptonigrine de TGase 2–GSK3β‑interactie in cellen kon verstoren, hun colocalisatie verminderde en de migratie van kankercellen beperkte. In muismodellen van eierstokkanker vertraagde orale behandeling met streptonigrine de tumorgroei, verkleinde metastatische laesies en verlengde de overleving. Het meest opvallend was dat wanneer streptonigrine werd gecombineerd met standaard chemotherapiemiddelen zoals cisplatine of paclitaxel, de muizen weken langer leefden dan bij chemotherapie alleen. Chemotherapie alleen neigde ertoe TGase 2‑niveaus te verhogen en GSK3β te verlagen, wat cellen indirect richting EMT duwde, maar het toevoegen van de TGase 2‑remmer keerde deze trend om en beperkte de nieuw verworven mobiliteit van de cellen. 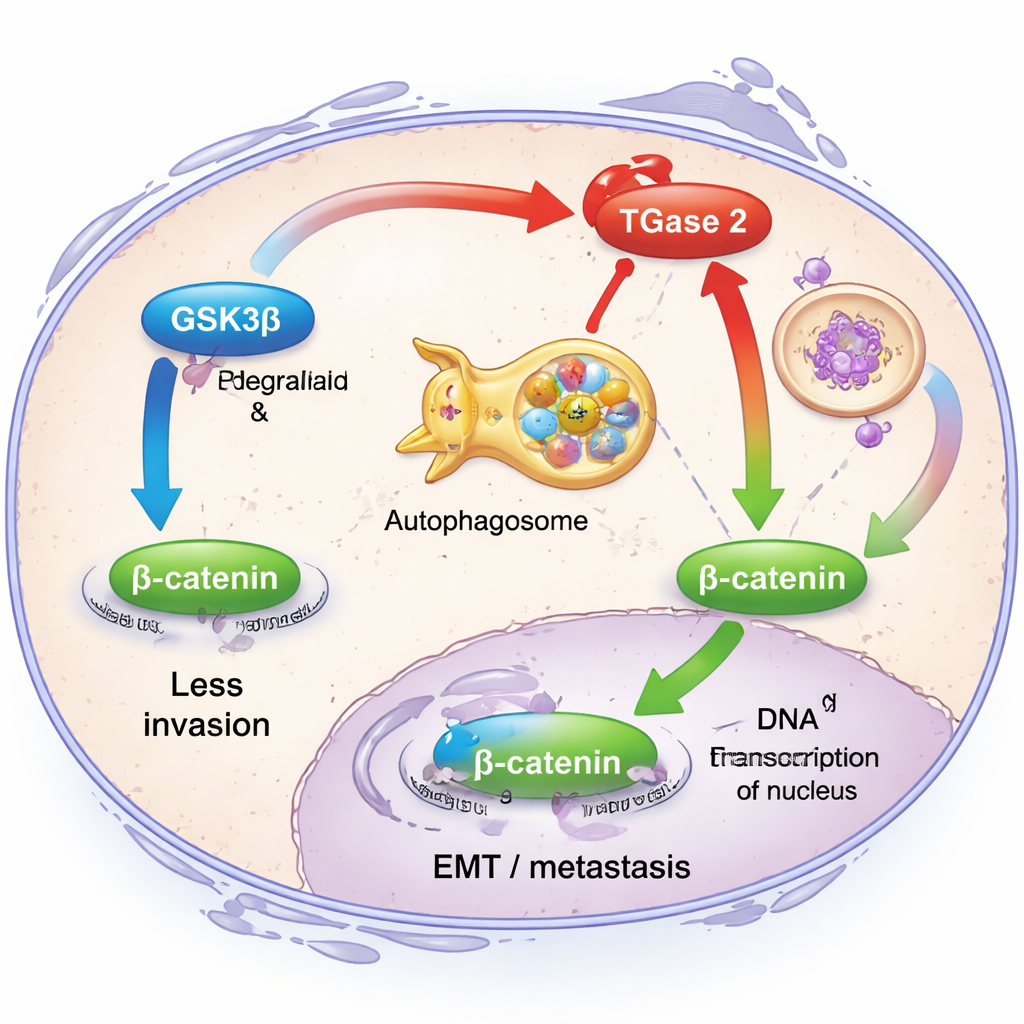
Wat dit kan betekenen voor toekomstige behandeling
Voor niet‑specialisten is de kernboodschap dat eierstokkankercellen TGase 2 exploiteren om een ingebouwde anti‑metastase‑rem uit te schakelen en om de storm van chemotherapie te doorstaan. Door GSK3β direct te inactiveren en β‑catenine te stabiliseren, helpt TGase 2 tumoren invasiever en medicijnresistenter te worden. Dit werk suggereert dat geneesmiddelen gericht op het N‑terminaal van TGase 2 — zoals streptonigrine of toekomstige, veiligere verbindingen die daarop zijn gebaseerd — bestaande chemotherapieën effectiever kunnen maken, de kans op terugkeer kunnen verkleinen en de overleving kunnen verbeteren. In eenvoudige termen kan het gericht remmen van TGase 2 een "ontsnappingsroute" van kanker afsluiten, waardoor eierstoktumoren gevoeliger voor behandeling blijven en minder geneigd zijn zich te verspreiden.
Bronvermelding: Lee, H., Kang, J.H., Kim, H.J. et al. Transglutaminase 2 exacerbates ovarian cancer survival by directly inactivating GSK3β. Cell Death Dis 17, 199 (2026). https://doi.org/10.1038/s41419-026-08447-0
Trefwoorden: eierstokkanker, medicatieresistentie, metastase, epitheliale mesenchymale transitie, gerichte therapie