Clear Sky Science · nl
Remming van auto-antigeen-geïnduceerde internalisatie van de B-celreceptor (BCR) als therapeutische strategie bij diffuus grootcellig B-cellymfoom (DLBCL)
Waarom dit belangrijk is voor patiënten
Diffuus grootcellig B-cellymfoom (DLBCL) is de meest voorkomende snelgroeiende bloedkanker bij volwassenen, en veel patiënten krijgen nog steeds een terugval na de standaard chemo-immunotherapie. Deze studie onderzoekt een verrassende kwetsbaarheid in een groot deel van deze tumoren: hun afhankelijkheid van een celoppervlakte-antenne genaamd de B-celreceptor (BCR). Door aan te tonen dat het blokkeren van de manier waarop deze antenne in de cel wordt getrokken de overleving van kankercellen kan ondermijnen, opent het werk de deur naar hergebruik van langgebruikte anti-misselijkheid- en antipsychotica als gerichte hulpmiddelen tegen lymfoom.
De antenne van de kankercel
B-cellen, een type witte bloedcel, gebruiken de B-celreceptor op hun oppervlak om bedreigingen te herkennen. In veel DLBCL’s, vooral het hoog-risico ‘‘activated B-cell’’ (ABC) subtype, wordt deze receptor gekaapt om voortdurend ‘‘blijf leven en groei’’-signalen te sturen. Vaak herkennen deze BCR’s eigen lichaamsmoleculen (auto-antigenen), die werken als een vastzittende deurbel. Wanneer auto-antigenen binden, doet de BCR meer dan alleen signaleren aan het oppervlak: hij wordt in de cel getrokken en voegt zich bij een intern eiwitcomplex met sensors zoals TLR9 en MYD88. Dit supercomplex schakelt vervolgens NFκB in, een krachtige signaalroute die groei bevordert. Tot nu toe was onduidelijk of deze inward reis van de receptor echt vereist is voor de kankerveroorzakende signalen.
De antenne ombouwen om zijn grenzen te testen
Om die vraag te beantwoorden gebruikten de onderzoekers CRISPR-genbewerking om de ‘‘punten’’ van de BCR in lymfoomcellijnen precies te veranderen. Ze vervingen de natuurlijke, zelf-Reactieve herkenningsgebieden door varianten die ovalbumine herkennen, een onschadelijk eiwit uit eiwit dat als laboratoriumtool wordt gebruikt. Deze gemodificeerde receptoren grepen niet langer hun gebruikelijke auto-antigenen, maar konden nog wel op gecontroleerde wijze worden geactiveerd met toegevoegd ovalbumine. In ABC-type lymfomen die normaal afhankelijk zijn van binding door zelf-antigenen, verminderde deze omwisseling sterk de activiteit van veel belangrijke signaalenzymen en dempte de expressie van NFκB-responsieve genen. De cellen groeiden langzamer, ondanks dat er eigenlijk meer BCR op hun oppervlak aanwezig was, wat aantoont dat voortdurende betrokkenheid door auto-antigenen en daaropvolgende interne signalering cruciaal zijn voor hun overleving.
Receptoren naar binnen trekken: een cruciale stap
Het team bekeek vervolgens rechtstreeks wat er met de BCR gebeurt nadat deze zijn antigeen ontmoet. In hun geconstrueerde modellen veroorzaakten zowel antilichaam-gebaseerde triggers als ovalbumine dat de receptor binnen enkele minuten van het celoppervlak verdween, wat snelle internalisatie bevestigt. Dit gebeurde niet alleen wanneer het antigeen buiten de cel verklaarde, maar ook wanneer het kunstmatig op het eigen membraan van dezelfde cel werd weergegeven, waarmee bepaalde echte tumorsituaties werden nagebootst. Het genetisch blokkeren van dit inwaartse verkeer, met een dominant-negatieve vorm van een eiwit genaamd dynamine-2 dat essentieel is voor clathrine-gemedieerde endocytose, hield BCR op het oppervlak, verkleinde de interne BCR–TLR9–NFκB-complexen, verminderde NFκB-doelgenen en vertraagde de celdeling. Interessant genoeg nam, wanneer endocytose werd geblokkeerd, sommige ‘‘achtergrond’’-BCR-signalen aan het oppervlak toe, wat suggereert dat kankercellen kunnen proberen te compenseren door een zwakkere, tonische signaalmodus te versterken.
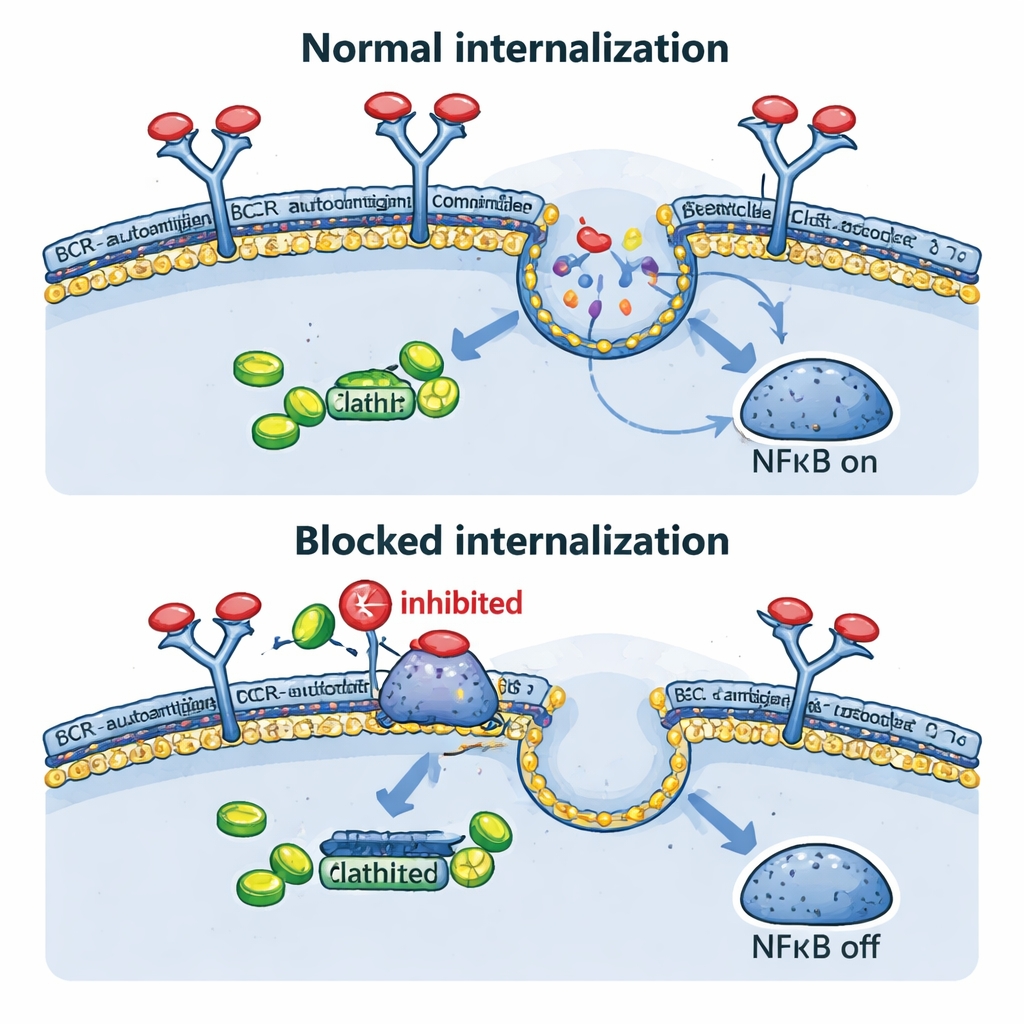
Oude medicijnen, nieuwe toepassingen
Aangezien het ontwikkelen van nieuwe geneesmiddelen traag en duur is, vroegen de auteurs zich of bestaande middelen die endocytose blokkeren de genetische experimenten konden nabootsen. Fenothiazinen, een familie antipsychotica en anti-misselijkheidsmiddelen, remmen bekend dynamine-2 en clathrine-afhankelijke opname van receptoren. In lymfoomcellen verhoogden stoffen zoals prochlorperazine en chlorpromazine het aantal BCR’s aan het oppervlak en verminderden sterk de antigeen-gedreven internalisatie. Dit leidde tot lagere NFκB-gedreven genactiviteit en verminderde levensvatbaarheid van ABC-type DLBCL-cellen, met name die met intacte BCR-componenten. In muizen met humane lymfoomtransplantaten vertraagde prochlorperazine, bij klinisch haalbare doses, de tumorgroei aanzienlijk. Bovendien gaf de combinatie van fenothiazinen met middelen die andere BCR-gekoppelde enzymen blokkeren, zoals SYK en PI3Kδ, sterkere kankerdodende effecten dan een van beide behandelingen alleen.
Wat dit voor de behandeling kan betekenen
Samenvattend laat de studie zien dat bij een substantieel subgroep van DLBCL’s de kankerveroorzakende signalen niet eenvoudigweg voortkomen van receptoren op het celoppervlak; ze zijn in belangrijke mate afhankelijk van het naar binnen trekken van het BCR–antigeencomplex via een specifieke endocytoseweg. Het onderbreken van deze stap—hetzij met genetische ingrepen, hetzij met fenothiazine-geneesmiddelen—verzwakt NFκB-signaaloverdracht en schaadt de overleving van tumorcellen, terwijl het mogelijk de gevoeligheid voor bestaande BCR-route-inhibitoren vergroot. Omdat fenothiazinen als anti-misselijkheidsmiddelen al een goed begrepen dosering en veiligheidspatroon hebben, biedt dit werk een realistisch stappenplan voor klinische onderzoeken die deze middelen, alleen of in combinatie, testen bij patiënten van wie het lymfoom auto-antigeen-afhankelijke BCR-activiteit vertoont.
Bronvermelding: Górniak, P., Polak, A., Rams, A. et al. Inhibition of autoantigen-induced B-cell receptor (BCR) internalization as a therapeutic strategy in diffuse large B cell lymphoma (DLBCL). Cell Death Dis 17, 216 (2026). https://doi.org/10.1038/s41419-026-08446-1
Trefwoorden: diffuus grootcellig B-cellymfoom, B-celreceptor, endocytose, fenothiazinen, NFkB-signaleringsroute