Clear Sky Science · nl
Tijdresolutie multi-omische analyse van paclitaxelblootstelling in humane iPSC‑afgeleide sensorische neuronen onthult mechanismen van chemotherapie-geïnduceerde perifere neuropathie
Waarom sommige kankermedicijnen zenuwen beschadigen
Chemotherapie heeft miljoenen mensen geholpen kanker te overleven, maar veel patiënten betalen een verborgen prijs: maanden of jaren van brandende pijn, tintelingen en gevoelloosheid in handen en voeten. Deze studie stelt een eenvoudige maar belangrijke vraag: wat doet het veelgebruikte kankermedicijn paclitaxel precies met menselijke sensorische zenuwcellen, en kan begrip van die veranderingen aanwijzingen geven voor betere preventie en behandeling van deze zenuwbeschadiging?
Van patiëntencellen naar in het lab gekweekte pijnzenuwen
In plaats van te vertrouwen op proefdieronderzoek begonnen de onderzoekers met cellen van vijf menselijke donoren, inclusief borstkankerpatiënten die paclitaxel hadden gekregen. Ze programmeerden deze cellen tot geïnduceerde pluripotente stamcellen en leidden ze vervolgens naar sensorische neuronen — hetzelfde type zenuwcel dat aanraking- en pijnsignalen van de huid naar het ruggenmerg geleidt. Deze in het lab gekweekte neuronen vormden lange, fragiele vezels en vertoonden elektrische activiteit die sterk leek op echte pijnreceptoren in het lichaam. Het team stelde ze daarna bloot aan toenemende doses paclitaxel, nabootsend de medicijnspiegels die bij patiënten voorkomen, en volgde de gezondheid van de cellen over meerdere dagen. Bij lage concentraties hielden de neuronen het goed vol, maar bij een klinisch relevante dosis (100 nM) begon hun overleving na ongeveer twee dagen te dalen, wat het begin van toxische zenuwbeschadiging markeerde.
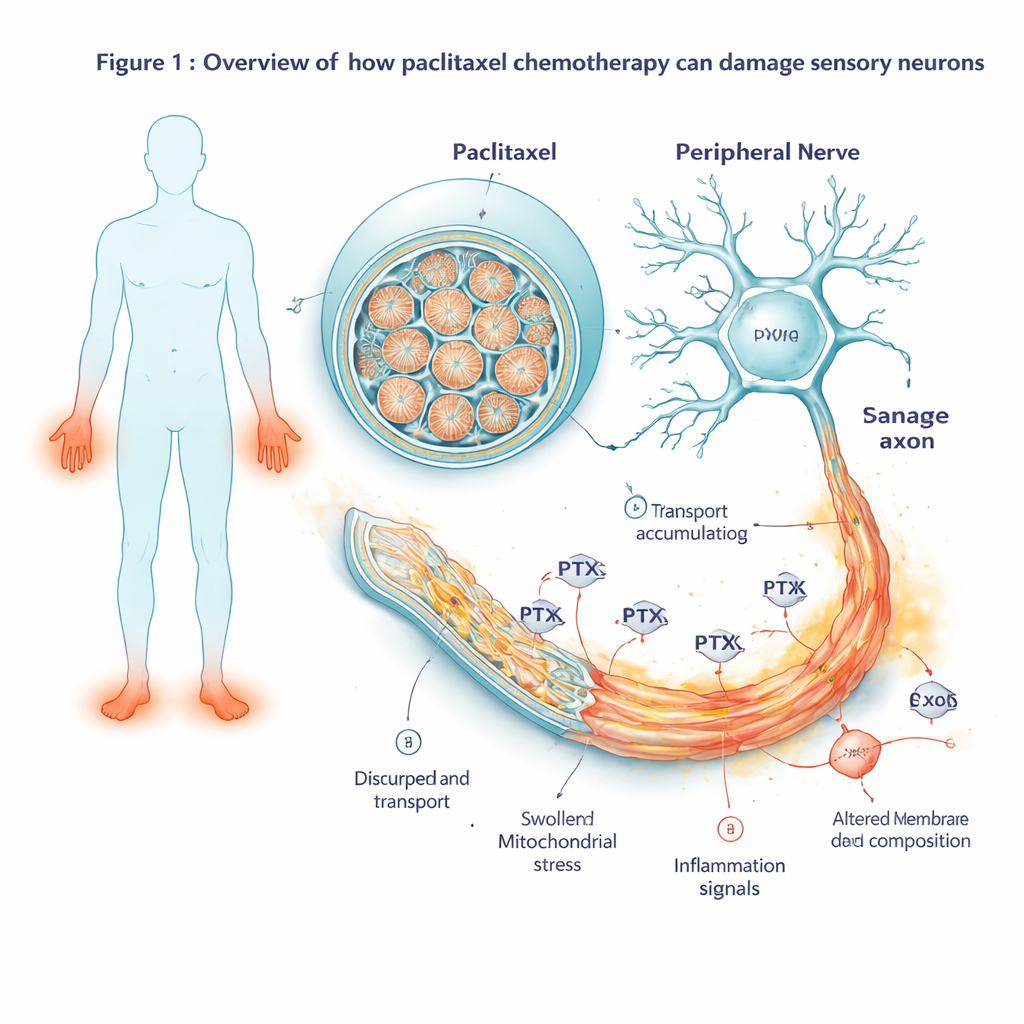
Het in de tijd volgen van genactiviteit
Om te zien hoe de cellen reageerden voordat ze zichtbaar verslechterden, maten de wetenschappers welke genen aanvingen of uitgingen op meerdere tijdstippen, van twee uur na blootstelling tot enkele dagen nadat het middel was weggespoeld. Vroeg zagen ze de activering van een klassiek cellair stressprogramma gecentreerd rond een gen dat JUN heet. Naarmate de blootstelling voortduurde, verbreedde dit stresssignaal zich tot een volwaardige zelfvernietigingscascade: genen die cellen naar geprogrammeerde celdood duwen werden sterk aan gezet, terwijl beschermende partners overweldigd raakten. Tegelijkertijd werden genen die verband houden met ontsteking en pijnsignalering actiever. De neuronen begonnen meer ontstekingsboodschappers, pijngerelateerde peptiden en receptoren te produceren die cellen gevoeliger maken voor schadelijke prikkels — veranderingen die spiegelen wat gezien wordt bij pijnlijke zenuwaandoeningen.
Diepgaande blik op eiwitten en lipiden binnen neuronen
Aangezien genen slechts blauwdrukken zijn, onderzocht het team ook de eiwitten die daadwerkelijk in de neuronen aanwezig waren, evenals hun lipide (vet) samenstelling. Na 48 uur paclitaxelblootstelling verschenen veel van dezelfde stress- en ontstekingssignalen die op RNA-niveau werden gedetecteerd ook als verhoogde eiwitniveaus, wat bevestigt dat de neuronen deze schadelijke programma’s uitvoerden. Opvallend was dat eiwitten die nodig zijn voor axonaal transport — de moleculaire motoren en steigerstructuren die vracht langs de lange zenuwvezels verplaatsen — sterk verminderd waren. Dit omvatte kinesines en regulerende eiwitten die microtubule‑sporen stabiel houden. Op lipideniveau lieten de neuronen een daling zien in belangrijke bouwstenen voor cholesterol en membraanlipiden, naast een toename in opgeslagen vetten die triacylglycerolen worden genoemd. Gezamenlijk suggereren deze verschuivingen dat paclitaxel niet alleen celdoodroutes activeert, maar ook de fysieke structuur en energiebalans van de zenuwvezels verzwakt.
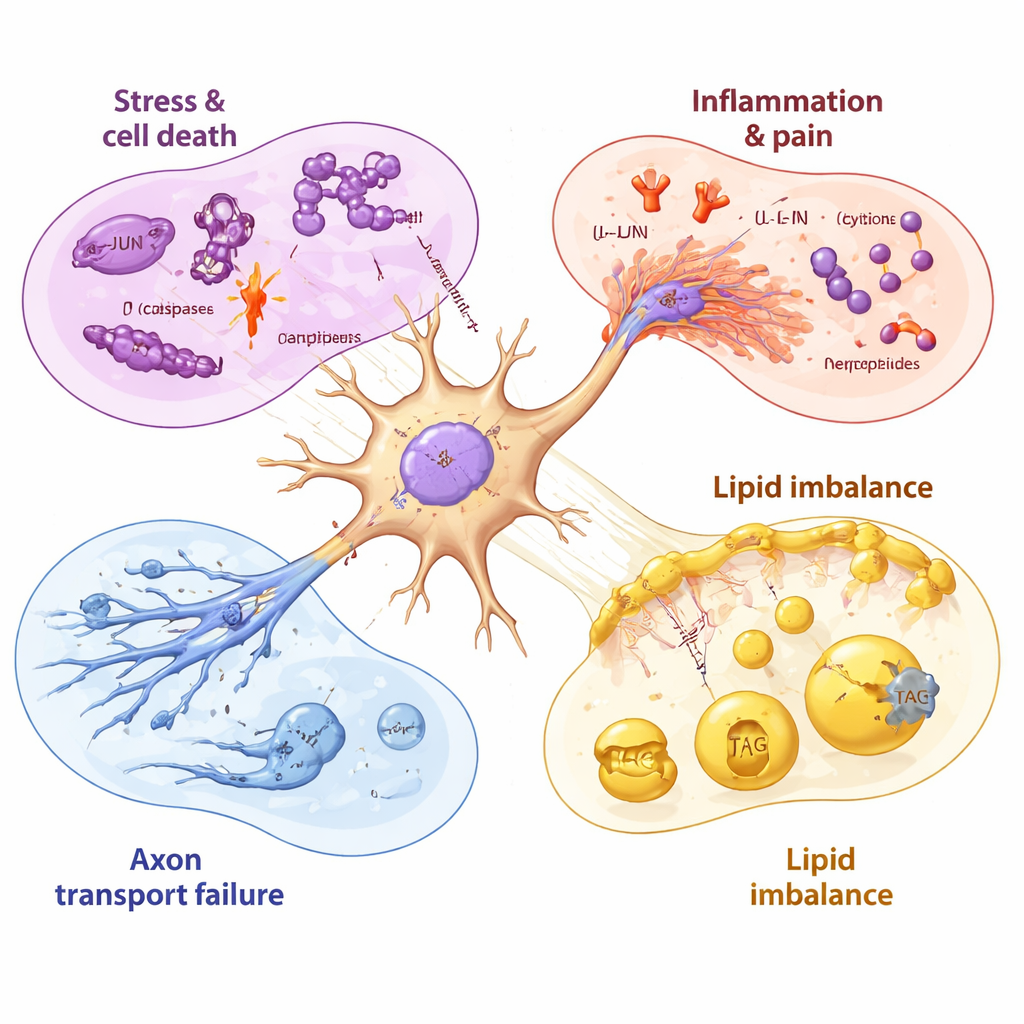
Een tijdlijn van zenuwschade en onvolledige herstel
Door de neuronen te bemonsteren vóór, tijdens en na medicijnblootstelling konden de onderzoekers deze gebeurtenissen in de tijd ordenen. Mitochondriale (energie‑gerelateerde) genen raakten binnen enkele uren verstoord, gevolgd door het stressgen JUN, en daarna door sterkere activering van celdood- en ontstekingsprogramma’s toen de levensvatbaarheid begon te dalen. Zelfs nadat paclitaxel was verwijderd, bleven veel schadelijke signalen dagenlang verhoogd, terwijl de genen die nodig zijn voor de aanmaak van gezonde membraanlipiden verder afnamen. Sommige laat opkomende moleculen, zoals een medicijn‑effluxpomp die paclitaxel kan uitdrijven en bepaalde groeifactoren, suggereerden dat neuronen probeerden zichzelf te beschermen en te herstellen — maar deze reacties leken relatief traag en onvolledig in vergelijking met de snelle, vroege neiging naar schade.
Wat dit betekent voor patiënten die met zenuwpijn leven
Voor een niet‑specialist is de kernboodschap dat paclitaxel sensorische zenuwen schaadt via een gecoördineerde reeks klappen: het zet hun energiesystemen onder druk, schakelt genen om richting celdood, veroorzaakt ontsteking en pijnsignalering, verstoort de interne “transportwegen” in zenuwvezels en verandert de vetten die zenuwmembranen stabiel houden. Door deze veranderingen in menselijk afgeleide neuronen tot in detail in kaart te brengen, toont de studie concrete, geneesmiddelbare doelen aan — zoals specifieke stressregulatoren, ontstekingsreceptoren en enzymen voor lipideproductie — die mogelijk geblokkeerd of ondersteund kunnen worden om zenuwen te beschermen zonder de kankertherapie te verzwakken. Hoewel nieuwe behandelingen verder onderzoek en testen vereisen, biedt dit werk een duidelijker routekaart om chemotherapie‑geïnduceerde zenuwbeschadiging te voorkomen of te verlichten en zo de levenskwaliteit van kankeroverlevenden te verbeteren.
Bronvermelding: Schinke, C., Maierhof, S.K., Hew, L. et al. Time‑resolved multi-omic analysis of paclitaxel exposure in human iPSC‑derived sensory neurons unveils mechanisms of chemotherapy‑induced peripheral neuropathy. Cell Death Dis 17, 211 (2026). https://doi.org/10.1038/s41419-026-08445-2
Trefwoorden: chemotherapie-geïnduceerde perifere neuropathie, paclitaxel, sensorische neuronen, neuroinflammatie, axondegeneratie