Clear Sky Science · nl
Omkeerbare argininemethylatie reguleert mitochondriale IDH2-activiteit: gecoördineerde controle door CARM1 en KDM3A/4A
De fijnregeling van de energiecentrales van de cel
Mitochondriën, vaak de energiecentrales van onze cellen genoemd, doen veel meer dan alleen energie produceren. Ze passen voortdurend aan hoe ze brandstof verbranden om aan de behoeften van het lichaam te voldoen, en wanneer dit misgaat kan dat bijdragen aan ziekten zoals diabetes, hartfalen en kanker. Deze studie onthult een verborgen "dimmer" binnen mitochondriën: een klein chemisch merkteken op één bouwsteen van een sleutelenzym, IDH2, dat helpt bepalen of mitochondriën op een laag pitje draaien of hun energieproductie opvoeren.
Een klein merkteken met grote gevolgen
Eiwitten in onze cellen zijn niet statisch; ze worden vaak gewijzigd met kleine chemische groepen die hun functioneren veranderen. Hoewel veel van zulke modificaties in de celkern en het cytosol goed bestudeerd zijn, zijn die binnen mitochondriën minder verkend. De auteurs richtten zich op één specifiek type merkteken, argininemethylatie, en vroegen of het de activiteit van mitochondriale enzymen zou kunnen reguleren. Ze concentreerden zich op het enzym IDH2, een werkpaard van de tricarbonzuurcyclus (TCA), dat bijdraagt aan de omzetting van nutriënten in zowel energie als belangrijke metabolische bouwstoffen. Met biochemische middelen en massaspectrometrie ontdekten ze dat IDH2 een specifiek methylmerk draagt op één aminozuur, arginine 188, en dat dit merk wordt aangebracht door het enzym CARM1, dat verrassend genoeg binnen mitochondriën actief is.
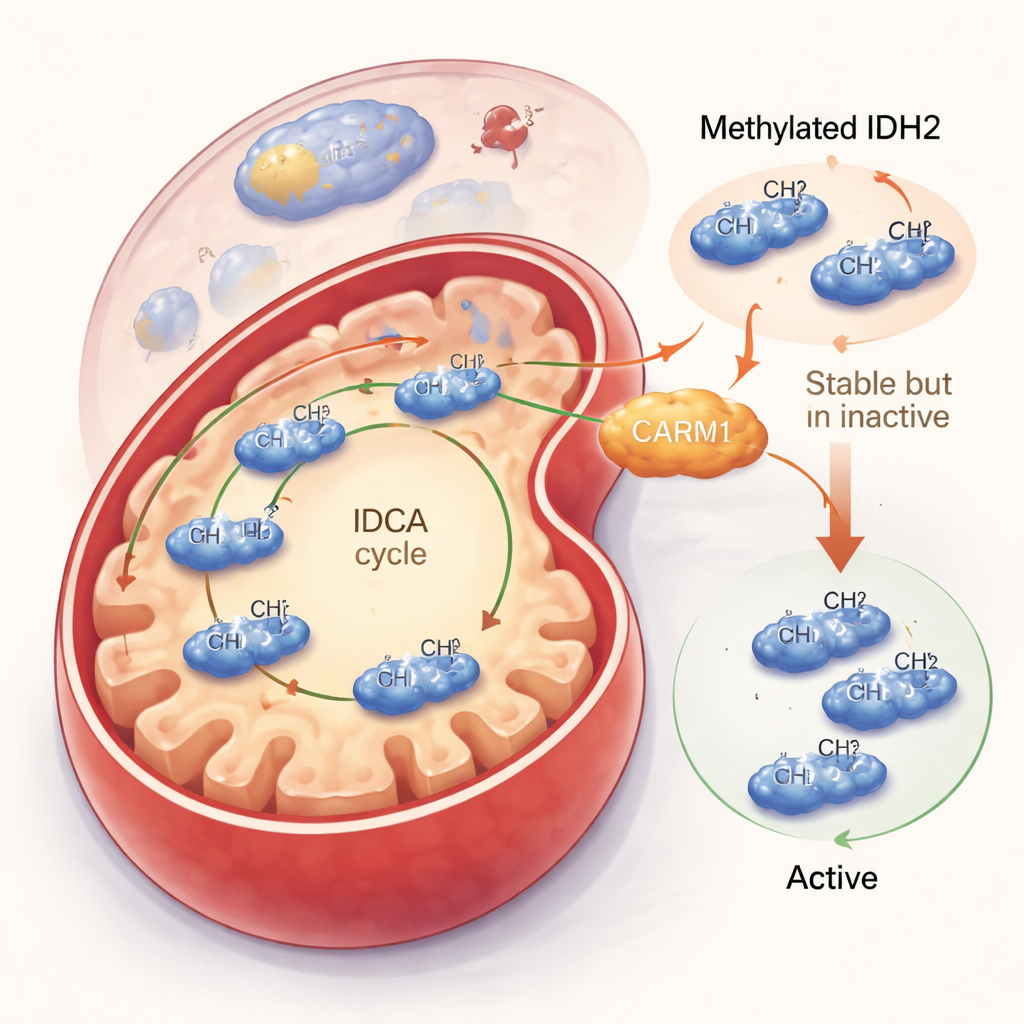
IDH2 minder actief maar stabieler maken
Het team vroeg vervolgens wat dit methylmerkteken precies doet. Wanneer CARM1 actief was en IDH2 gemethyleerd kon worden, werd het IDH2-eiwit stabieler en bleef het langer in de cel aanwezig. Maar deze schijnbare winst ging gepaard met een nadeel: gemethyleerd IDH2 was minder actief. In celproeven en testen met gezuiverd eiwit produceerde gemethyleerd IDH2 minder van zijn hoofdproduct, alfa‑ketoglutaraat, en genereerde het minder van de beschermende molecule NADPH. Een variant van IDH2 die niet op arginine 188 gemethyleerd kon worden, vormde juist meer van de actieve dimerstructuur, werkte sneller en verhoogde zowel alfa‑ketoglutaraat- als NADPH-niveaus. Hoewel er overall minder van dit ongemethyleerde IDH2 aanwezig was, deed elk molecuul meer werk, wat leidde tot een netto toename van de mitochondriale output.
Een omkeerbare schakelaar met twee gummiddelen
Kernachtig was dat dit methylmerk niet permanent is. De onderzoekers toonden aan dat twee enzymen die normaal bekendstaan om het verwijderen van een ander soort merkteken, lysine-demetylasen KDM3A en KDM4A, ook het argininemethylmerk van IDH2 kunnen wissen. Wanneer deze demetylasen aanwezig waren, verloor het gemethyleerde arginine op positie 188 zijn extra chemische groepen, werd IDH2 minder stabiel maar actiever, en nam de dimervorm toe. Cellen met meer actieve KDM3A of KDM4A vertoonden een hogere mitochondriale membraanpotentiaal en verbruikten meer zuurstof, signalen dat hun mitochondriën actiever waren in oxidatieve stofwisseling. Wanneer deze enzymen werden verminderd, gebeurde het omgekeerde: de IDH2-activiteit daalde en de mitochondriale prestaties namen af, wat benadrukt dat dit een omkeerbaar regelsysteem is in plaats van een eenrichtingsverandering.
De koppeling tussen metabolisme en ziekte
Aangezien IDH2 in verband is gebracht met kanker en andere aandoeningen, onderzochten de auteurs hoe deze methylatieschakelaar in ziekteachtige omstandigheden van belang kan zijn. In verschillende normale en kankercellijnen zagen ze dat hogere IDH2-eiwitniveaus vaak samen gingen met meer methylatie en verrassend genoeg lagere enzymactiviteit, wat suggereert dat "meer eiwit" niet altijd "meer functie" betekent. In datasets van borstkanker leken patiënten met hogere IDH2-eiwitniveaus slechter te overleven, ook al correleerde IDH2-genexpressie niet met de uitkomst. De resultaten ondersteunen een model waarin CARM1‑gedreven methylatie de TCA‑cyclus vertraagt en cellen aanstuurt naar alternatieve, door kanker begunstigde manieren om nutriënten te gebruiken, terwijl demetylasen zoals KDM3A en KDM4A cellen weer richting efficiëntere energieproductie kunnen duwen.
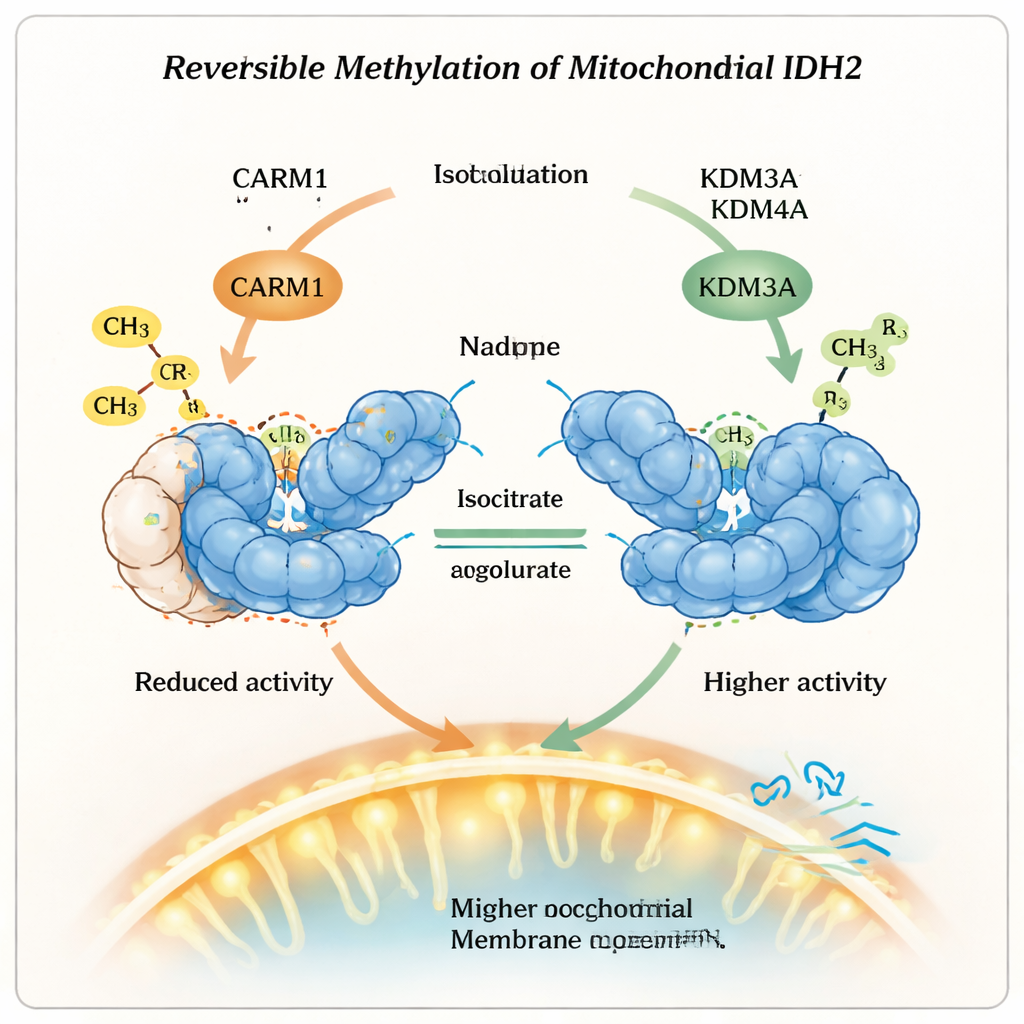
Wat dit betekent voor gezondheid en therapie
In gewone bewoordingen laat dit werk zien dat mitochondriën enzymen niet simpelweg aan- of uitzetten, maar omkeerbare chemische merktekens gebruiken als fijninstelbare knoppen. Door een methylgroep toe te voegen zet CARM1 IDH2 om in een langer bestaand maar minder actief formaat; door dat merkteken te verwijderen ruilen KDM3A en KDM4A wat stabiliteit in voor meer krachtoutput. Deze balans beïnvloedt hoe cellen kiezen tussen snelle maar inefficiënte suikerverbranding en langzamere, efficiëntere energieproductie. Inzicht in deze methylatie-"dimmer" op IDH2 opent nieuwe mogelijkheden voor therapieën die erop gericht zijn foutief mitochondriaal metabolisme te corrigeren bij aandoeningen zoals kanker en metabole ziekten, door de enzymen aan te pakken die deze kleine maar krachtige chemische merktekens schrijven en wissen.
Bronvermelding: Cho, Y., Winarto, J., Song, DG. et al. Reversible arginine methylation regulates mitochondrial IDH2 activity: coordinated control by CARM1 and KDM3A/4A. Cell Death Dis 17, 195 (2026). https://doi.org/10.1038/s41419-026-08444-3
Trefwoorden: mitochondriën, IDH2, argininemethylatie, celmetabolisme, CARM1