Clear Sky Science · nl
Een MIF-p38-GSDMD ontstekingslus in keratinocyten ligt ten grondslag aan door UVB veroorzaakte cutane lupus
Waarom zonlicht een groot probleem kan zijn bij lupus
Voor de meeste mensen zorgt zonlicht hooguit voor een kleurtje of, in het ergste geval, een zonnebrand. Voor veel lupuspatiënten kan echter al enkele minuten ultraviolette B‑straling (UVB) pijnlijke, langdurige huiduitslag uitlokken en zelfs de hele ziekte verergeren. Deze studie onthult een verborgen "feedbacklus" in huidcellen die helpt verklaren waarom hun huid zo lichtgevoelig is—en wijst op nieuwe, zeer lokale behandelingen die de reactie kunnen temperen zonder het hele immuunsysteem te onderdrukken.
Huidcellen als onverwachte aanstichters
Artsen wisten al dat cutane lupus erythematosus (CLE) gepaard gaat met chronische ontsteking en littekenvorming van de huid, maar de aandacht ging vaak uit naar binnendringende immuuncellen. Met single‑cell RNA‑sequencing zoomden de auteurs juist in op de bouwstenen van de huid zelf—keratinocyten in de bovenste laag en fibroblasten daaronder. Ze vonden dat bij lupuspatiënten specifieke subgroepen keratinocyten waren uitgebreid en een sterk "interferon‑handtekening" vertoonden, een patroon van antivirale alarmgenen dat permanent aanstaat. Binnen deze abnormale keratinocyten viel één boodschapperprotein op: macrophage migration inhibitory factor, of MIF, dat veel hoger werd geproduceerd dan meer bekende ontstekingsmoleculen zoals TNF of IL‑6.
Een verborgen boodschapper die door zonlicht vrijkomt
Het aantreffen van veel MIF in keratinocyten verklaarde nog niet waarom zonlicht zo gevaarlijk is. Toen het team gekweekte keratinocyten aan UVB blootstelde, ontdekten ze dat de totale hoeveelheid MIF in de cellen nauwelijks veranderde—maar dat het eiwit dosisafhankelijk in de omringende vloeistof werd vrijgegeven. Hoe meer UVB, hoe meer MIF lekte, en dat volgde nauwkeurig een merker voor membraanschade. Wanneer deze MIF‑rijke vloeistof op verse keratinocyten en fibroblasten werd aangebracht, veroorzaakte dit klassieke CLE‑achtige veranderingen: meer ontstekingscytokinen en enzymen die de steunmatrix van de huid afbreken en herbouwen. Het stilleggen van MIF met genetische middelen of het blokkeren ervan met een kleinmoleculair middel verminderde deze schadelijke reacties sterk, wat aantoont dat door keratinocyten geproduceerd MIF geen bijproduct is maar een belangrijke versterker van UVB‑geïnduceerde schade. 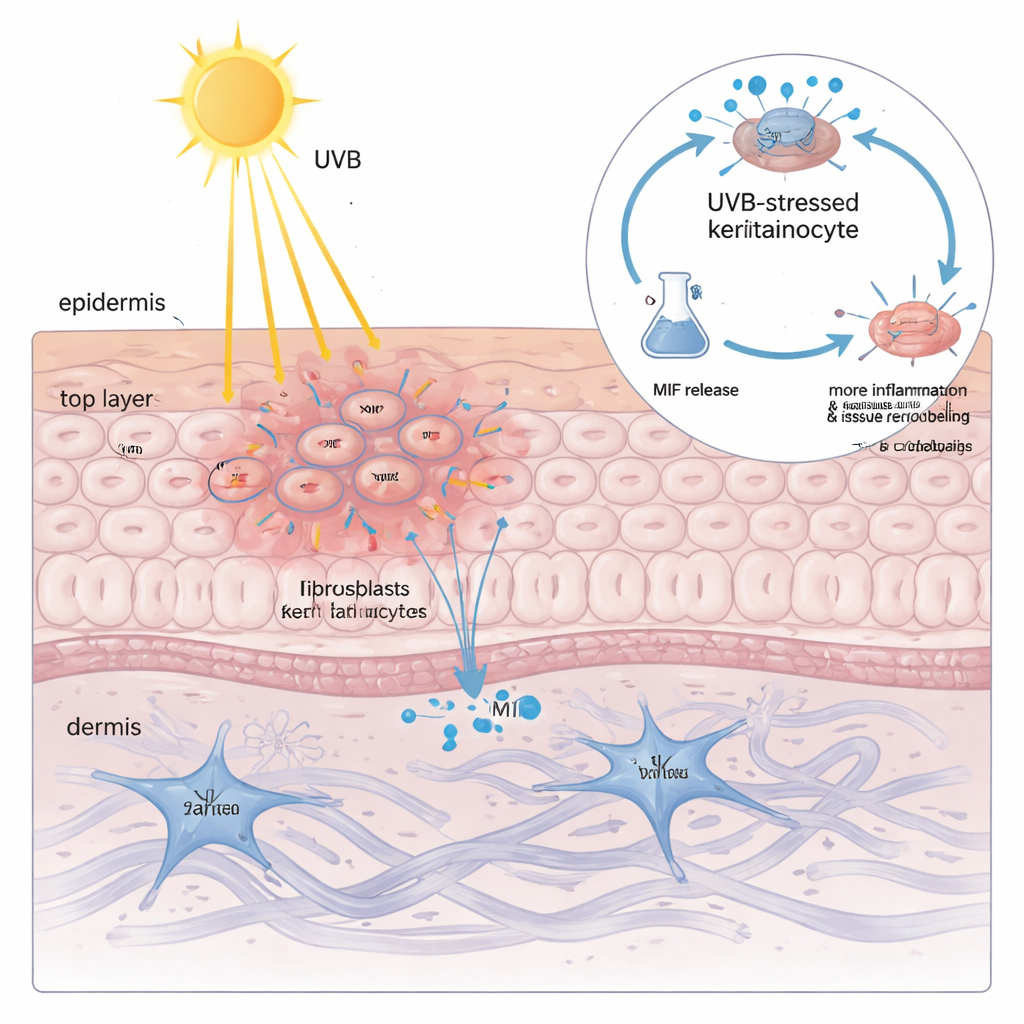
Een zichzelf in stand houdende ontstekingslus in keratinocyten
Om te begrijpen hoe UVB keratinocyten dwingt MIF vrij te geven, bouwden de onderzoekers een "lupusachtige" keratinocyten‑model door cellen te beladen met hun eigen DNA en RNA, waarmee ze het slecht afgehandelde genetische afval uit lupus nabootsten. In deze geprimede toestand activeerde UVB een zogeheten ribotoxische stressrespons: een schadesignaal van ribosomen dat een kinase genaamd ZAKα inschakelde en op zijn beurt het stressenzym p38 activeerde. Deze route verhoogde een ander eiwit, de transcriptiefactor C/EBPβ, die aan de controleregio van het NLRP3‑gen bond en dit aanzette. NLRP3 dreef vervolgens de splitsing van GSDMD aan, een porievormend eiwit dat gaten in het celmembraan maakt en een ontstekingsvorm van celdood veroorzaakt die pyroptose wordt genoemd. Cruciaal was dat MIF voornamelijk via deze GSDMD‑poriën ontsnapte—niet via normale secretie‑blaasjes. Eenmaal buiten binde MIF aan zijn oppervlaktereceptor CD74 op keratinocyten, waardoor p38, NLRP3 en GSDMD opnieuw werden geactiveerd en zo de vicieuze cirkel sloot: UVB → p38 → NLRP3 → GSDMD‑poriën → MIF‑release → meer p38‑activatie.
Van moleculair inzicht naar nieuwe lokale behandelingen
Deze lus was niet alleen een labcuriositeit. Bij een lupusgevoelige muizenstam veroorzaakte UVB‑blootstelling ernstige huidlaesies met hoge niveaus van MIF, p38‑activatie, NLRP3 en gespleten GSDMD in de epidermis. Toen de onderzoekers een gen‑therapeutisch virus gebruikten om het Mif‑gen specifiek in de huid stil te leggen, werden UVB‑geïnduceerde huiduitslag veel milder en daalden ontstekings‑ en weefselherstelmarkers in zowel keratinocyten als fibroblasten. Om bijwerkingen in het hele lichaam te vermijden, ontwikkelden ze ook oplosbare microneedle‑pleisters beladen met de MIF‑remmer ISO‑1. Kort in de huid gedrukt, leverden deze kleine naaldjes pijnloos het middel in de bovenste lagen af. Behandelde lupusgevoelige muizen ontwikkelden veel minder en minder ernstige laesies na UVB en het moleculaire kenmerk van de MIF‑p38‑GSDMD‑lus werd duidelijk onderdrukt. 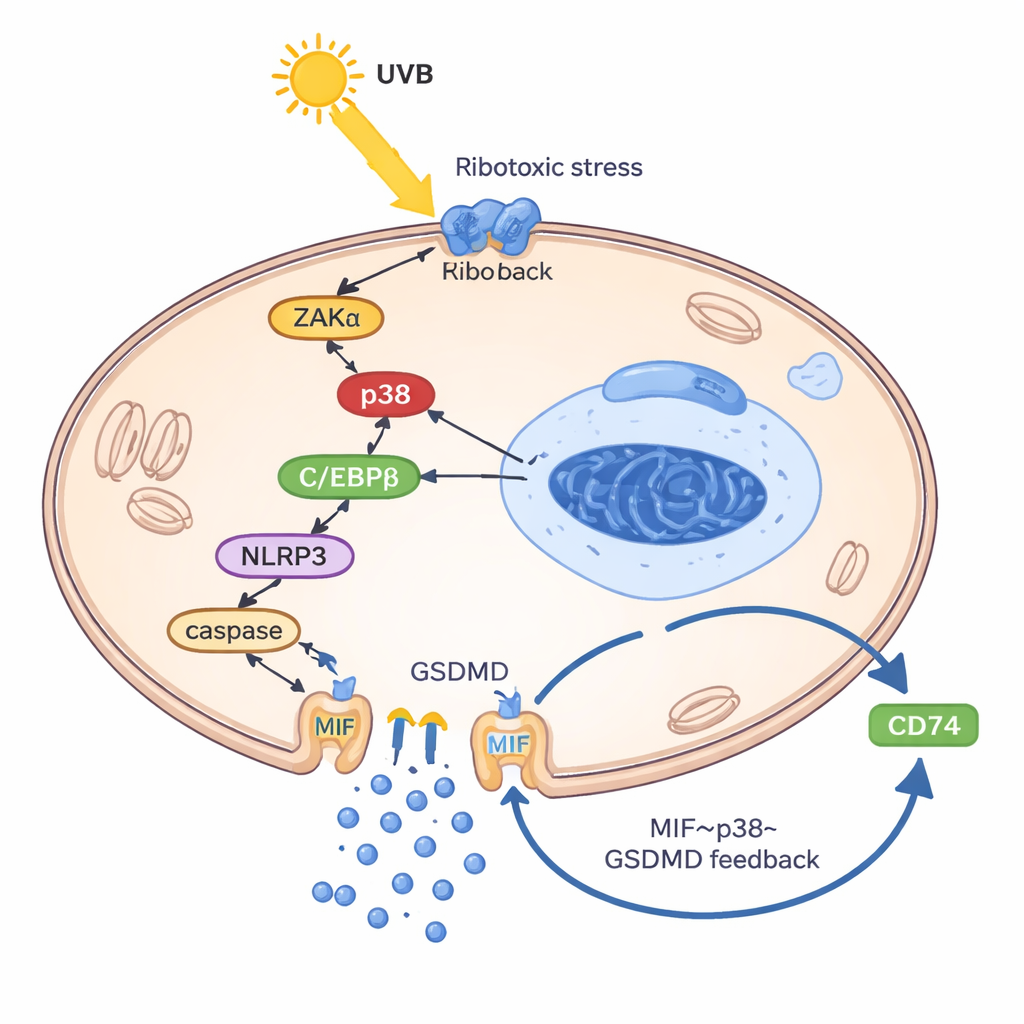
Wat dit betekent voor mensen met lupus
In eenvoudige bewoordingen laat dit werk zien dat bij lupus bepaalde huidcellen zodanig geprogrammeerd zijn dat ze overreageren op UVB‑licht door een krachtig "versterkings"‑molecuul, MIF, vrij te geven via zelfgemaakte membraanporiën. Die versterking voedt vervolgens de ontstekingsmachine, zelfs nadat de initiële lichtprikkel is verdwenen. Door deze lus stap voor stap in kaart te brengen, suggereert de studie dat het blokkeren van MIF direct in de huid—met genstillegging of slimme afleveringssystemen zoals microneedle‑pleisters—de vicieuze cirkel van fotosensitieve opvlammingen kan doorbreken zonder het immuunsysteem breed te onderdrukken. Als vergelijkbare strategieën veilig en effectief blijken bij mensen, zouden ze mensen met lupus nieuwe manieren kunnen bieden om comfortabeler in het licht te leven.
Bronvermelding: Guo, C., Luo, S., Luo, J. et al. A MIF-p38-GSDMD inflammatory loop in keratinocytes underlies UVB-induced cutaneous lupus. Cell Death Dis 17, 198 (2026). https://doi.org/10.1038/s41419-026-08443-4
Trefwoorden: cutane lupus, fotosensitiviteit, keratinocyten, ontstekingslus, microneedle-therapie