Clear Sky Science · nl
SOX21 onderdrukt de groei van glioblastoom door de AP-1-activiteit te remmen
Waarom deze studie naar hersenkanker ertoe doet
Glioblastoom is een van de dodelijkste vormen van hersenkanker, grotendeels omdat een kleine populatie hardnekkige “startende” cellen het tumorgroeiproces kan blijven aansturen en de tumor na behandeling kan laten terugkeren. Deze studie onthult hoe een van nature voorkomend eiwit in hersencellen, SOX21, deze gevaarlijke cellen kan uitschakelen door een groeibevorderend programma in hun DNA uit te schakelen. Inzicht in deze interne uit‑schakelaar kan nieuwe strategieën inspireren om glioblastoom af te remmen en huidig behandelingen effectiever te maken.
De verborgen aanjagers in hersentumoren
Binnen een glioblastoom zijn niet alle cellen gelijk. Een minderheid, bekend als glioblastoom-voorlopercellen (GPC’s), gedraagt zich als stamcellen: ze vernieuwen zichzelf, zijn therapieresistent en kunnen de tumor opnieuw zaaien na operatie, bestraling of chemotherapie. Deze cellen worden aangestuurd door netwerken van transcriptiefactoren, eiwitten die bepalen welke genen actief of stil zijn. Sommige goed bestudeerde factoren, zoals SOX2 en leden van de AP‑1-familie, stimuleren doorgaans groei en overleving. In tegenstelling daarmee is SOX21 in verband gebracht met verminderde celdeling en verhoogde rijping van normale hersenstamcellen, en eerder werk suggereerde dat het tegen hersentumoren zou kunnen beschermen. Het was echter onduidelijk of het verhogen van SOX21-niveaus in een reeds bestaande tumor de groei daadwerkelijk kon vertragen, en hoe SOX21 precies in kankercellen werkte.
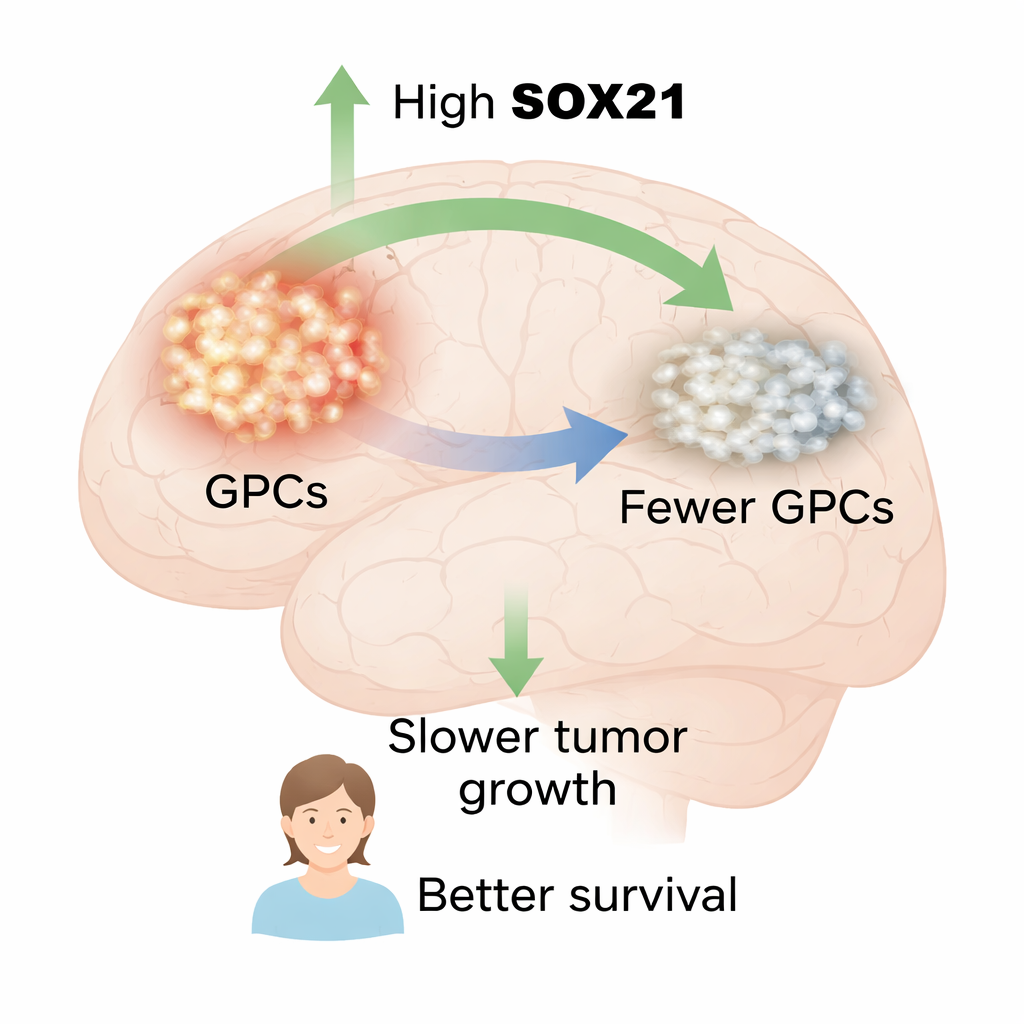
SOX21 wijst op een betere prognose en verzwakt tumorcellen
De onderzoekers begonnen met het onderzoeken van menselijke glioblastoommonsters. Ze vonden dat SOX21-eiwit voornamelijk aanwezig was in cellen die ook stamachtige markers zoals SOX2 en OLIG2 droegen, en in cellen die actief deelden, geïdentificeerd met de marker KI67. Dit toonde aan dat SOX21 zich precies in de GPC‑compartiment van de tumor bevindt. Door grote publieke datasets van patiëntentumoren te bekijken, vergeleken ze vervolgens de overleving van mensen wiens kankers hoge versus lage SOX21-genactiviteit hadden. In twee onafhankelijke cohorten leefden patiënten met hogere SOX21-expressie significant langer, wat SOX21 koppelt aan een gunstiger ziekteverloop.
SOX21 aanzetten vertraagt groei en verkleint de tumorvormende potentie
Om oorzaak en gevolg te testen, maakten de onderzoekers GPC’s uit patiëntentumoren die een schakelbare SOX21-genconstructie droegen die met het middel doxycycline kon worden ingeschakeld. Wanneer SOX21 in kweek werd geïnduceerd, deelden deze cellen minder, namen ze minder van het DNA‑bouwblok op (een teken van vertraagde proliferatie) en vertoonden ze meer kenmerken van geprogrammeerde celdood. Hun vermogen om vrijzwevende sferen te vormen, een maat voor stamachtige zelfvernieuwing, daalde sterk en ze werden gevoeliger voor het standaardmiddel tegen glioblastoom, temozolomide. In muisexperimenten werden menselijke GPC’s eerst toegelaten om hersentumoren te vestigen en pas daarna werd SOX21 aangezet. Onder deze omstandigheden vertraagde SOX21—maar niet SOX2—de tumorgroei, verminderde het aandeel delende en stamachtige cellen binnen de massa en verlengde het significant de overleving van de dieren. Dit toont aan dat het verhogen van SOX21 kan werken op bestaande tumoren, niet alleen bij preventie.
Hoe SOX21 een kankerversterkend programma ontwapent
Diepgaand op het moleculaire mechanisme brachten de auteurs in kaart welke genen veranderden toen SOX21 werd aangezet en waar langs het DNA SOX21 fysiek gebonden was. SOX21 verhoogde genen die betrokken zijn bij celcyclusstop en celdood, waaronder de tumorsuppressor p21, en verlaagde genen die eerder aan glioma‑progressie werden gekoppeld, zoals CDK6, EFNB2, HDAC9 en SOX2 zelf. Opvallend was dat SOX21 sterk gebonden bleek aan DNA‑regio’s die ook bezet waren door c‑JUN, een sleutellid van de AP‑1-familie dat doorgaans groeibevorderende genen activeert. Deze gedeelde regio’s bevatten klassieke AP‑1‑sequentiemotieven en chemische kenmerken van actieve enhancers—DNAfragmenten die genexpressie versterken. Toen SOX21‑niveaus stegen, werden deze enhancers minder toegankelijk en verloren ze activatiemarkeringen, en de gekoppelde genen werden naar beneden gereguleerd. Middelen die AP‑1 blokkeren, reproduceerden veel van dezelfde genveranderingen en biologische effecten als SOX21, terwijl het geforceerd overproduceren van c‑JUN cellen kon redden van de onderdrukkende invloed van SOX21.
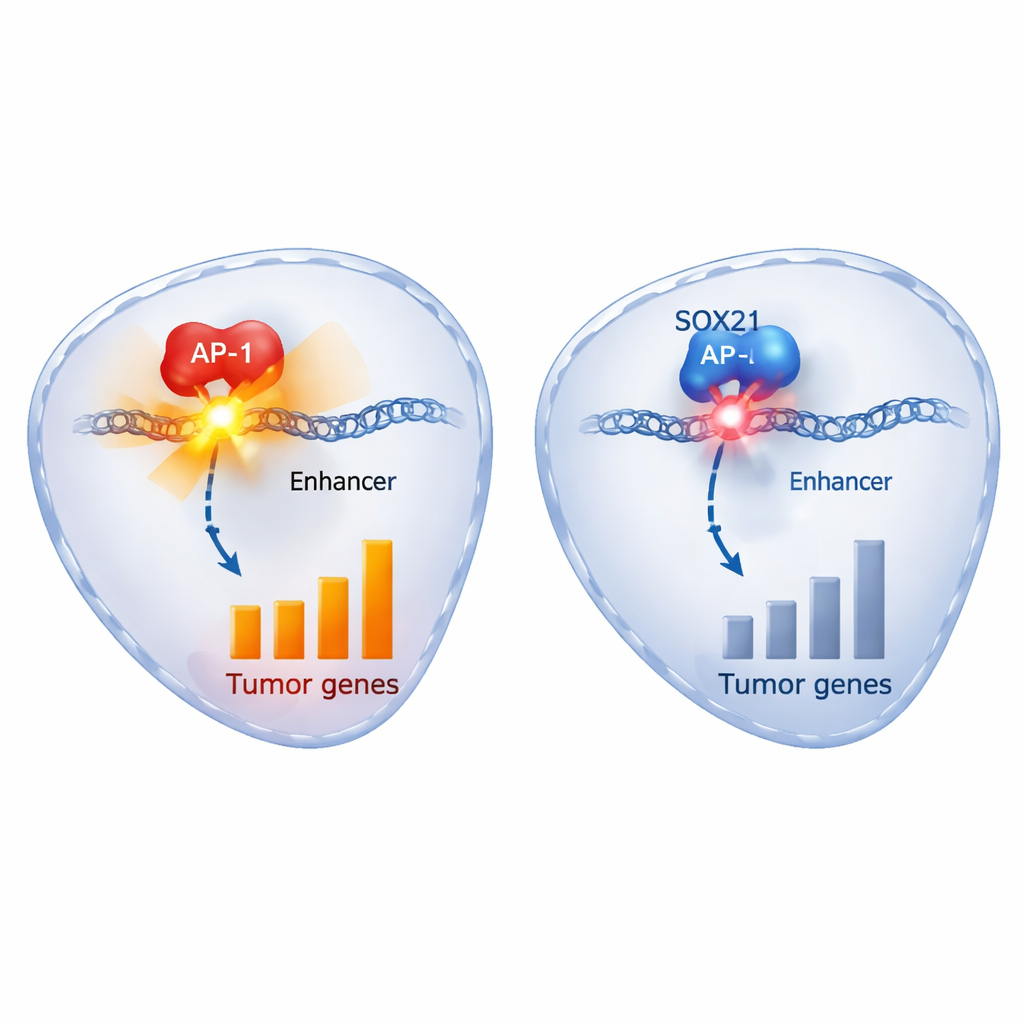
Wat dit betekent voor toekomstige behandeling van glioblastoom
Kort gezegd fungeert SOX21 als een rem in de gevaarlijkste cellen van glioblastoom door zich te binden aan dezelfde DNA‑schakelaars die AP‑1 gebruikt om tumorgroei aan te jagen, en die schakelaars vervolgens te dimmen. Patiënten waarvan de tumoren van nature meer SOX21 produceren, blijken doorgaans beter af te zijn, en in diermodellen vertraagt het aanzetten van SOX21 in gevestigde tumoren hun groei en verbetert het de respons op chemotherapie. Hoewel het direct afleveren of activeren van SOX21 bij patiënten nog niet praktisch is, bieden de paden die het reguleert—en zijn touwtrekken met AP‑1—veelbelovende aanknopingspunten voor nieuwe geneesmiddelen die de stamachtige kern van de tumor verzwakken en de kans op terugkeer verkleinen.
Bronvermelding: Rrapaj, E., Yuan, J., Kurtsdotter, I. et al. SOX21 suppresses glioblastoma growth by repressing AP-1 activity. Cell Death Dis 17, 191 (2026). https://doi.org/10.1038/s41419-026-08442-5
Trefwoorden: glioblastoom, kankerstamcellen, SOX21, AP-1, hersentumortherapie