Clear Sky Science · nl
Honokiol remt tumorontwikkeling en metastase via mitochondriën‑gerichte effecten
Een boomverbinding omgezet in een kankerkampioen
Veel kankergeneesmiddelen zijn afgeleid van planten, en wetenschappers ontrafelen nog steeds hoe sommige van deze natuurlijke moleculen in onze cellen werken. Deze studie richt zich op honokiol, een stof uit de bast van Magnolia die al lang in de traditionele geneeskunde wordt gebruikt, en toont aan hoe het direct de kleine energiecentrales in kankercellen kan aansturen om tumorgroei te vertragen en uitzaaiing te blokkeren, terwijl normale cellen grotendeels gespaard blijven.
De energiecentrales in onze cellen
Elke cel is afhankelijk van mitochondriën, vaak de "energiecentrales" van de cel genoemd, om de energiemolecuul ATP te produceren. Bij kanker doen mitochondriën meer dan alleen brandstof maken — zij helpen ook bepalen of een cel overleeft of sterft. Eén groot moleculair machineriecomplex, ATP‑synthase, zit in het binnenmembraan van mitochondriën en maakt ATP. Kankercellen produceren vaak in overvloed een partnerproteïne genaamd IF1 die zich vastklampt aan ATP‑synthase en fungeert als een soort veiligheidsvergrendeling, waardoor tumoren weerstand bieden tegen een vorm van zelfvernietiging die samenhangt met het openen van de mitochondriale permeabiliteitstransitie en daaropvolgende celdood.
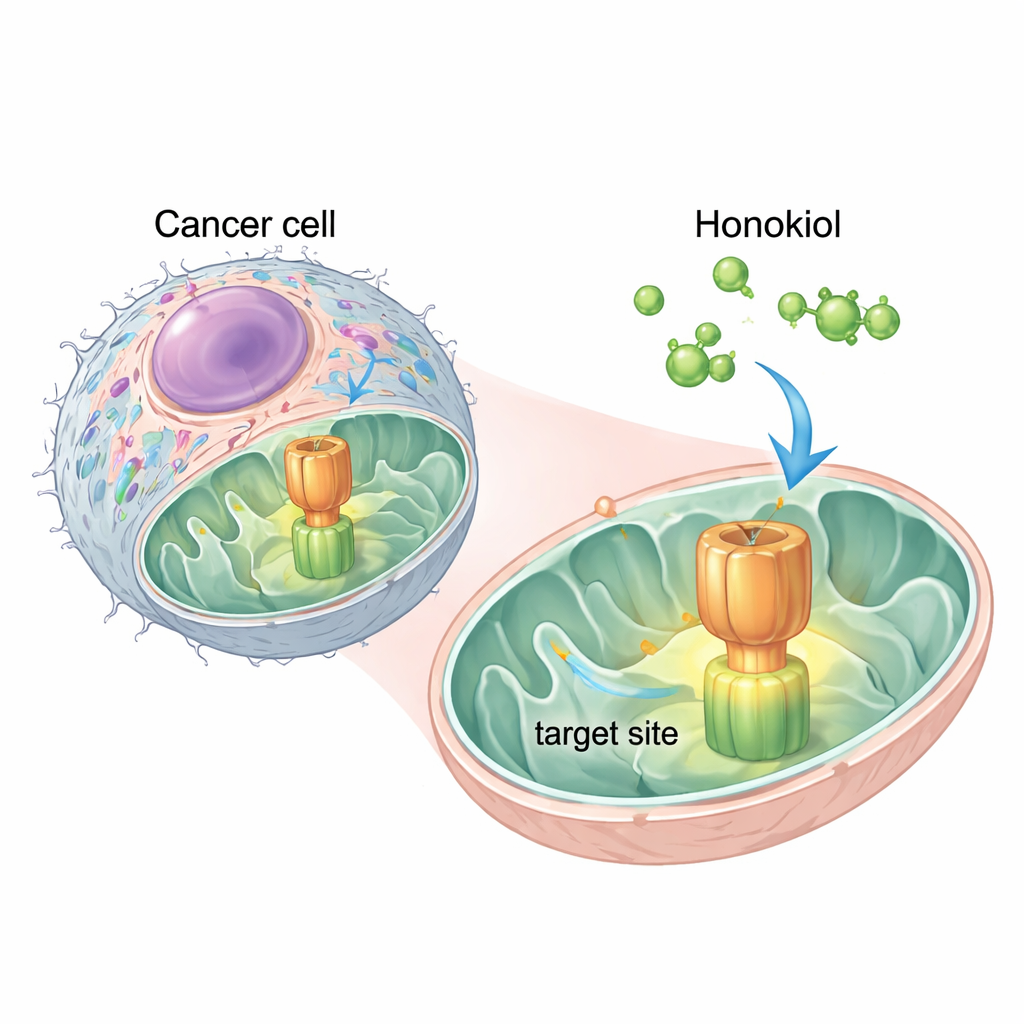
Een natuurlijk molecuul vindt een kritieke schakelaar
De onderzoekers gebruikten computersimulaties om te bepalen waar honokiol mogelijk op ATP‑synthase zou binden. Ze vonden twee veelbelovende "dockingsites" op een van de componenten, een gebied genaamd OSCP. De sterkste site overlapt met hetzelfde vlak dat IF1 gebruikt om zich aan ATP‑synthase vast te houden. Dit suggereerde dat honokiol als een moleculaire wig kan werken, die in OSCP schuift en IF1 wegduwt. Experimenten met menselijke cervixkankercellen (HeLa) bevestigden dit idee: toevoeging van honokiol verminderde het fysieke contact tussen IF1 en OSCP, zonder andere delen van het enzym te verstoren, wat aantoont dat het effect specifiek was.
Van cellen naar levende dieren: minder tumor, minder uitzaaiing
Om te zien of deze moleculaire duw een impact in de echte wereld had, plaatste het team lichtgevende menselijke kankercellen in kleine zebravisembryo’s, een erkend model om tumorgroei en metastase in een heel organisme te volgen. In vissen geïnjecteerd met normale, IF1‑rijke HeLa‑cellen verkleinde honokiolbehandeling de tumormassa’s aanzienlijk en verminderde het aantal kankercellen dat naar verre gebieden uitzaaide, waardoor het patroon leek op vissen die waren geïnjecteerd met IF1‑knockoutcellen zonder het beschermende eiwit. Interessant was dat honokiol ook het aantal metastatische cellen verminderde wanneer IF1 ontbrak, wat wijst op een tweede, IF1‑onafhankelijke manier om kankerspreiding te beperken.
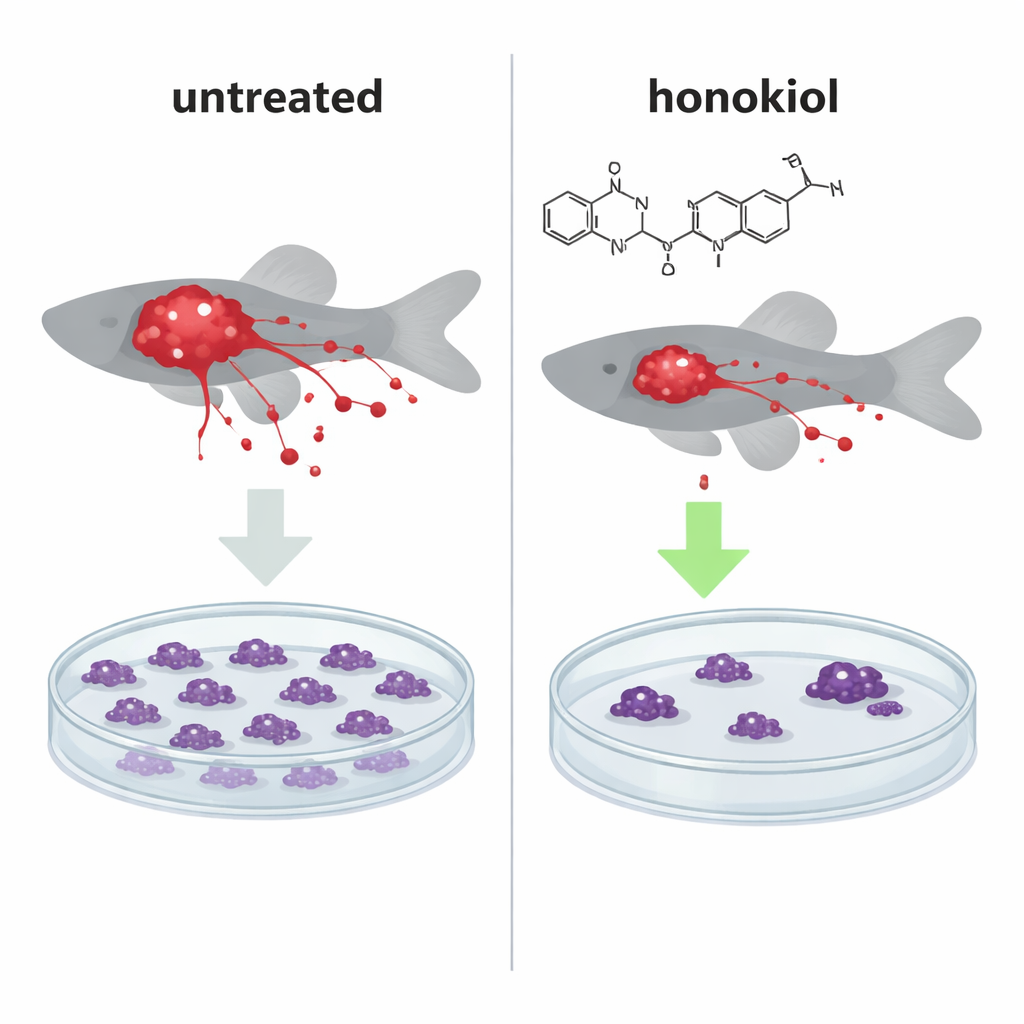
Defecte energiecentrales dwingen zelfvernietiging af
Terug in de petrischaal verminderde honokiol het vermogen van kankercellen om grote kolonies te vormen in zacht agar, een test die de stressvolle, zuurstofarme omstandigheden in solide tumoren nabootst. Dit gebeurde zonder een grote vertraging van normale celdeling of de basale mitochondriale ademhaling, wat wijst op een verandering in hoe mitochondriën tussen leven en dood beslissen. Metingen van calciumhuishouding toonden aan dat honokiol mitochondriën gevoeliger maakte voor het openen van de permeabiliteitstransitiepoort bij lagere calciumconcentraties, een bekende trigger voor zwelling en het vrijkomen van doodsbevorderende factoren. Bij matige doses hing dit effect af van het wegduwen van IF1; bij hogere doses werkte honokiol via zijn tweede OSCP‑bindingssite en via verhoogde reactieve zuurstofsoorten, waardoor zelfs IF1‑deficiënte cellen gevoeliger werden voor geprogrammeerde celdood.
Voorkomen dat kankercellen gaan migreren
Kanker wordt het gevaarlijkst wanneer cellen losraken en naar nieuwe organen migreren. In wondachtige "scratch"‑testen vertraagde honokiol sterk de collectieve migratie van celvlakken en verminderde het markers van epitheliaal‑mesenchymale transitie, een proces dat tumorcellen in staat stelt te bewegen en te infiltreren. Gedetailleerde elektronenmicroscopische beelden toonden dat migrerende cellen normaal gesproken hun mitochondriën vergroten en hervormen, met extra interne plooien om te voldoen aan de hoge energiebehoefte aan de voorste rand. Met honokiol werden deze voorste mitochondriën in plaats daarvan gezwollen en structureel beschadigd — kenmerken van het openen van de permeabiliteitstransitiepoort — terwijl mitochondriën in niet‑bewegende gebieden minder aangetast waren of zelfs in aantal toenamen, afhankelijk van IF1.
Wat dit betekent voor toekomstige kankerbehandelingen
Simpel gezegd tonen deze resultaten aan dat honokiol zich kan richten op een klein regelgevend gebied van het mitochondriale ATP‑producerende apparaat en een ingebouwde veiligheidschakelaar kan omdraaien die kankercellen vaak vergrendeld houden. Door IF1 los te maken en de poort direct richting openen te duwen, stimuleert honokiol tumoren tot zelfvernietiging en bemoeilijkt het hun vermogen te migreren en uitzaaiingen te zaaien. Omdat deze effecten voortkomen uit kenmerken die veel kankers gemeen hebben — eerder dan uit één specifiek oppervlaktekenmerk — zou gerichtheid op de OSCP‑regio van ATP‑synthase een nieuwe klasse therapieën kunnen inspireren die de kwetsbaarheden van kankercel‑energiecentrales uitbuiten terwijl ze schade aan gezonde weefsels beperken.
Bronvermelding: Grandi, M., Boldrin, F., Risato, G. et al. Honokiol blocks tumor development and metastasis through mitochondrion-targeted effects. Cell Death Dis 17, 186 (2026). https://doi.org/10.1038/s41419-026-08441-6
Trefwoorden: honokiol, mitochondriën, ATP‑synthase, apoptose, metastase