Clear Sky Science · nl
Immune checkpointremmer-geassocieerde pneumonitis: huidige ontwikkelingen en de veronderstelde rol van mesenchymale stamceltherapie
Wanneer kankerbehandeling de longen treft
Geneesmiddelen die het immuunsysteem loslaten op kanker hebben de zorg voor ziekten zoals longkanker en melanoom getransformeerd. Deze nieuwe kracht heeft echter een keerzijde: bij sommige patiënten keert dezelfde immuunreactie die tumoren aanvalt zich tegen de longen en veroorzaakt een aandoening die bekendstaat als immune checkpointremmer-geassocieerde pneumonitis (ICIP). Deze overzichtsartikel legt uit wat ICIP is, waarom het optreedt, hoe artsen het momenteel behandelen en waarom een speciaal type stamcel — mesenchymale stamcellen (MSC’s) — mogelijk in de toekomst een veiliger, meer gerichte manier kan bieden om de ontstekingsstorm te temperen zonder het antikankereffect op te offeren. 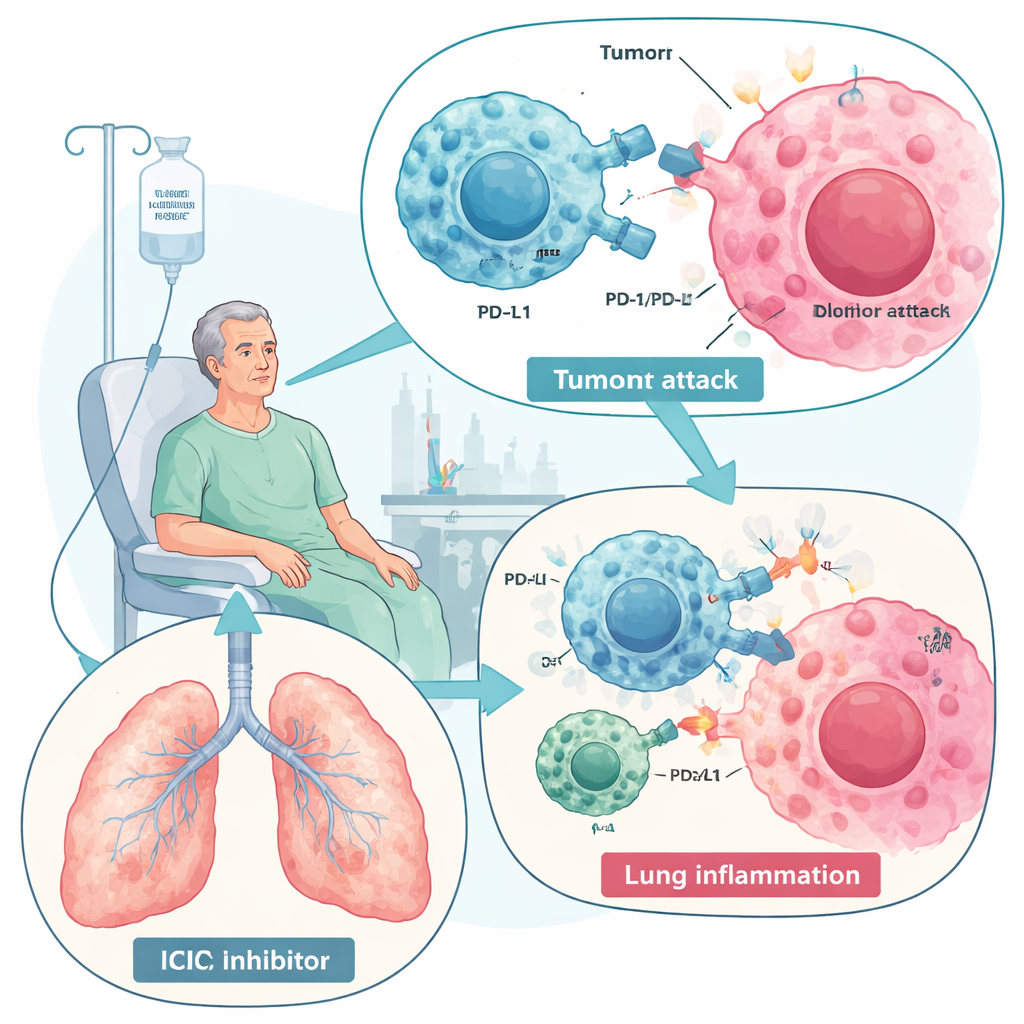
Krachtige kankerremedies met een verborgen longrisico
Immune checkpointremmers, vooral diegenen die PD-1 en PD-L1 blokkeren, werken door moleculaire “remmen” te verwijderen die normaal immuunreacties temperen. Zonder die remmen kunnen T-cellen kankercellen beter herkennen en vernietigen, wat de overleving bij veel tumortypes verbetert. Maar diezelfde stimulatie kan de normale tolerantie verstoren en immuungerelateerde bijwerkingen in meerdere organen veroorzaken. ICIP is de ernstigste longcomplicatie van deze middelen en een van de belangrijkste immuungerelateerde oorzaken van therapiegerelateerde sterfte. De incidentie varieert van enkele procenten tot bijna een derde van de patiënten in sommige real-world studies, vooral bij patiënten met longkanker of vooraf bestaande longaandoeningen zoals COPD of interstitiële longziekte. Symptomen variëren van milde hoest en kortademigheid tot levensbedreigende respiratoire insufficiëntie.
Hoe het immuunsysteem de long beschadigt
De review beschrijft ICIP als het gevolg van een verstoorde immuurbalans in de longen. Overactieve “strijders” — CD8 T-cellen, bepaalde helper-T-cellen, inflammatoire macrofagen, neutrofielen en natural killer-cellen — overspoelen het longweefsel en geven agressieve signaalstoffen af, waaronder interferon-gamma, TNF-alpha en interleukines zoals IL-6 en IL-17. Tegelijkertijd zijn normaal beschermende cellen die ontsteking dempen, zoals regelgevende T-cellen en reparatiegerichte macrofagen, verminderd. Sommige patiënten tonen ook stijgende niveaus van zelfreactieve antilichamen voor of tijdens de behandeling, wat suggereert dat ICIP deels op een auto-immuunziekte kan lijken. In gewassen longvocht vinden artsen een inflammatoir patroon rijk aan T-cellen en een cytokinemix die verschilt van infectie of tumorprogressie, wat de diagnose kan ondersteunen.
Waarnemen, indelen en behandelen van de schade
Op CT-scans verschijnt ICIP meestal als waasachtige “ground-glass”-gebieden of vlekkerige consolidaties verspreid door beide longen, patronen die afwijken van stralingsschade die beperkt blijft tot het bestraalde veld. Artsen stellen de diagnose ICIP door scanbevindingen, symptomen en een zorgvuldige uitsluiting van infectie en andere oorzaken te combineren. Internationale richtlijnen gradëren de ernst van 1 (mild, vaak alleen radiologisch) tot 4 (levensbedreigende respiratoire insufficiëntie). De huidige hoeksteen van de behandeling zijn glucocorticoïden — krachtige ontstekingsremmende steroïden — soms gecombineerd met andere immuundempende middelen zoals tocilizumab (die IL-6 blokkeert) of infliximab (die TNF-alpha blokkeert) bij ernstige of steroid-resistente gevallen. Deze benaderingen kunnen levensreddend zijn, maar ze zijn grove instrumenten: steroïden hebben veel bijwerkingen, sommige patiënten reageren niet en brede immuunsuppressie kan juist de antitumorrespons verzwakken die de behandeling beoogt te versterken.
Waarom stamcellen in beeld komen
Mesenchymale stamcellen, die uit beenmerg, vetweefsel of navelstrengweefsel kunnen worden gewonnen, zijn naar voren gekomen als veelbelovende “immuunmodulatoren” in plaats van louter weefselbouwers. Wanneer ze in de bloedbaan worden ingebracht, blijven veel van deze cellen tijdelijk vastzitten in de fijne bloedvaten van de long — het zogenaamde first-pass-effect — wat een nadeel is voor de behandeling van verre organen maar een potentieel voordeel voor longziekten. In diermodellen en vroege humane trials bij aandoeningen zoals ernstige longontsteking, acute respiratory distress syndrome, inflammatoire darmziekte en graft-versus-host ziekte dempen MSC’s overactieve immuunreacties, verschuiven ze immuuncellen naar een meer gebalanceerde staat en scheiden ze groeifactoren af die weefselherstel bevorderen en littekenvorming beperken. Belangrijk is dat hun voordelen vaak niet voortkomen uit het omvormen tot longcellen zelf, maar uit het mengsel van signaalmoleculen en kleine vesikels dat ze afgeven. 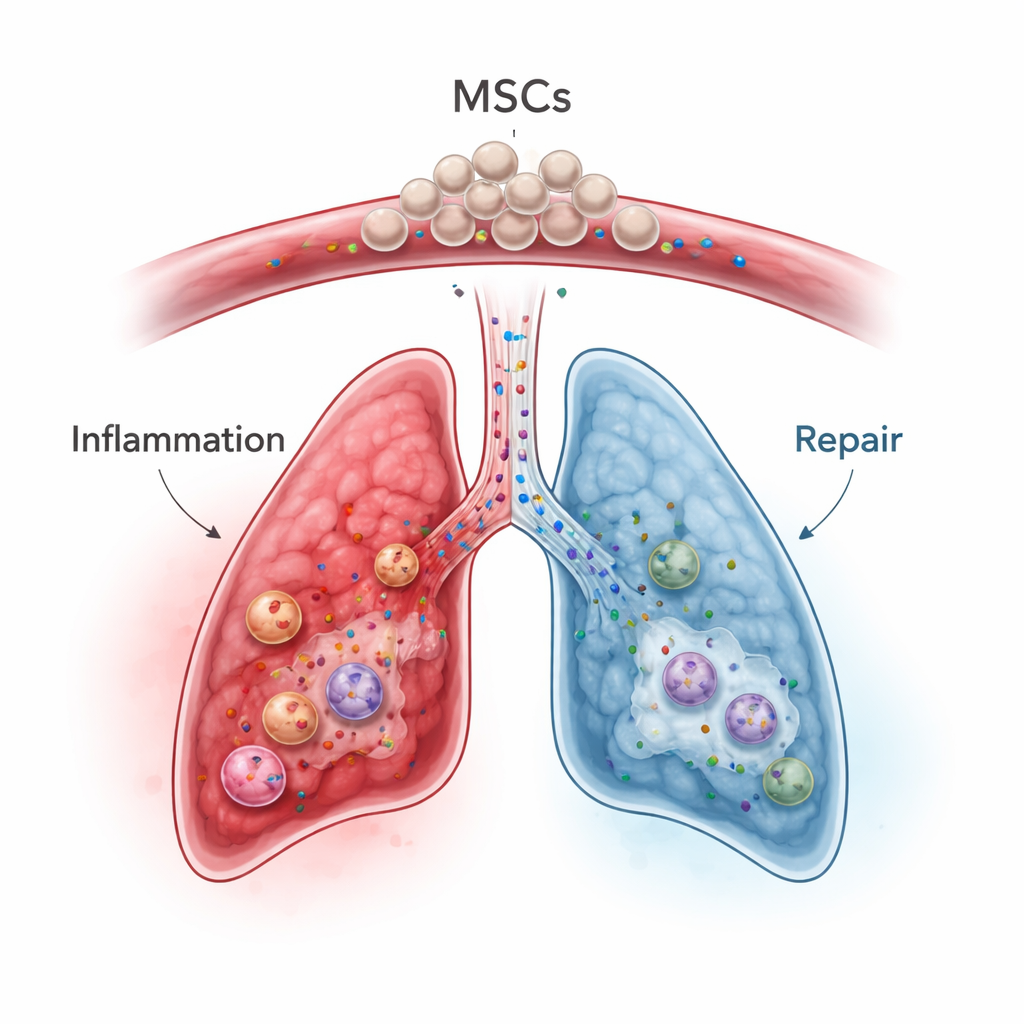
Hoe MSC’s ICIP zouden kunnen kalmeren zonder de behandeling te saboteren
In de context van ICIP zouden MSC’s theoretisch meerdere problemen tegelijk kunnen aanpakken. Ze kunnen geactiveerde T-cellen rechtstreeks remmen, de groei en functie van regelgevende T-cellen bevorderen en macrofagen wegsturen van een agressieve, weefselschadelijke toestand naar een helende toestand. Ze verlagen ook belangrijke ontstekingsboodschappers zoals IL-6, IL-1β en TNF-alpha en verhogen anti-inflammatoire factoren en beschermende eiwitten zoals TSG-6 die helpen longschade en fibrose te beperken. Preklinisch werk suggereert dat MSC’s of ingenieuze MSC-afgeleide exosomen cytokinenstormen en orgaanschade veroorzaakt door checkpointremmers of bestraling kunnen verminderen, terwijl ze in sommige settings de antitumoractiviteit beter behouden dan standaard immunosuppressiva. De auteurs waarschuwen echter dat MSC’s ook op complexe manieren met tumoren en bloedstolling kunnen interageren en dat hun effecten sterk afhangen van de omliggende inflammatoire omgeving en zelfs van de MSC-bron (beenmerg, vetweefsel of navelstreng).
Vooruitblik: veelbelovend maar behoedzaam testen
Voor patiënten wier kankerbehandeling wordt onderbroken of bedreigd door ernstige longtoxiciteit, zouden op MSC’s gebaseerde therapieën uiteindelijk een meer gerichte manier kunnen bieden om ontsteking te koelen, longweefsel te herstellen en langdurige littekenvorming te voorkomen — idealiter zonder de levensreddende voordelen van immune checkpointinhibitie teniet te doen. Er zijn echter nog geen ICIP-specifieke MSC-studies afgerond. De auteurs pleiten voor zorgvuldig ontworpen dierstudies en klinische trials om te bepalen welk type MSC- of exosoomproduct het beste werkt, welke dosis gegeven moet worden, wanneer het gegeven moet worden ten opzichte van steroïden en immunotherapie, en hoe men risico’s zoals tumorgroei of trombose kan monitoren. Tot die tijd blijven MSC’s een hoopvolle maar nog experimentele optie aan de horizon voor de behandeling van deze ernstige bijwerking van moderne kankerzorg.
Bronvermelding: Li, Z., Zheng, X., Xia, H. et al. Immune checkpoint inhibitor-related pneumonitis: current advances and the putative role of mesenchymal stem cell therapy. Cell Death Dis 17, 200 (2026). https://doi.org/10.1038/s41419-026-08440-7
Trefwoorden: bijwerkingen van immunotherapie, pneumonitis, checkpointremmers, mesenchymale stamcellen, longontsteking