Clear Sky Science · nl
c-Myc/GRPEL1 behoudt vetzuursynthese via FASN om PDAC-celproliferatie te ondersteunen
Waarom het vetverlangen van kankercellen ertoe doet
Pancreaskanker behoort tot de dodelijkste vormen van kanker, deels omdat de tumorcellen uitblinken in het herprogrammeren van hun eigen metabolisme om te overleven en te groeien. Deze studie onderzoekt een verrassend onderdeel van dat verhaal: hoe pancreas-tumorcellen hun interne “vetfabriekjes” opvoeren om niet aflatende groei te voeden, en hoe het blokkeren van dit proces mogelijk nieuwe behandelopties voor patiënten kan openen.
Een taaie kanker met een metabolisch voordeel
De meeste pancreaskankers zijn van het type pancreatisch ductaal adenocarcinoom (PDAC), dat meestal laat wordt ontdekt en slecht reageert op de huidige therapieën. PDAC-cellen leven in een vijandige omgeving met weinig zuurstof en schaarse voedingsstoffen, maar weten te gedijen door te herschakelen hoe ze suikers, vetten en andere brandstoffen gebruiken. Hun mitochondriën — de kleine energiecentrales in de cel — spelen een centrale rol in deze herprogrammering. Om deze energiecentrales draaiende te houden, controleren en repareren cellen voortdurend duizenden mitochondriale eiwitten, een proces dat bekend staat als mitochondriale eiwit-kwaliteitscontrole. Tot nu toe was onduidelijk hoe dit kwaliteitscontrolemachinerie verbonden is met de manier waarop pancreastumoren zichzelf van brandstof voorzien.
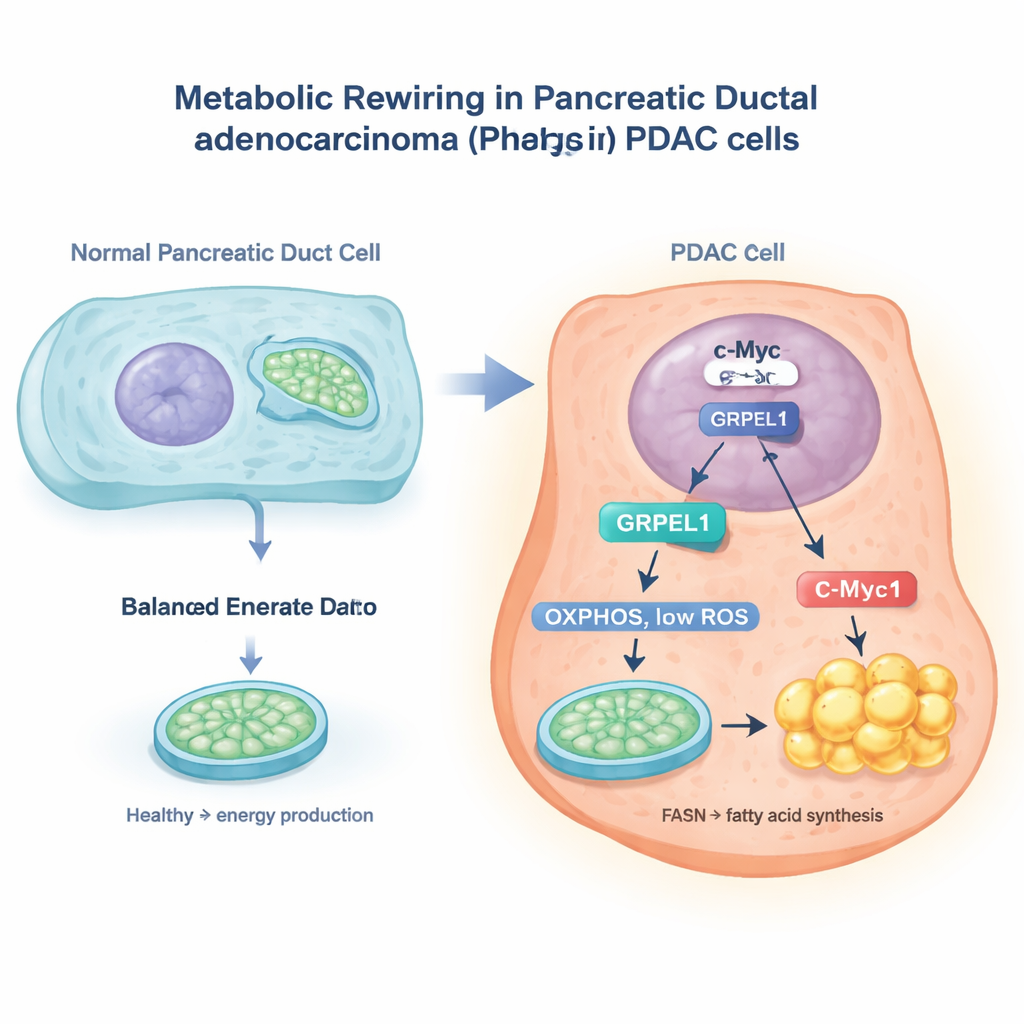
De c-Myc-schakelaar en een mitochondriaal helper-eiwit
De onderzoekers gebruikten grote kankerdatabanken en experimenten in pancreaskankercellen om zich te richten op een eiwit genaamd GRPEL1, een helper die betrokken is bij de afhandeling van mitochondriale eiwitten. Ze ontdekten dat een bekend kankergen, c-Myc, fungeert als een moleculaire schakelaar in de celkern die het GRPEL1-gen aanzet. Wanneer c-Myc-niveaus werden verlaagd, daalden ook de GRPEL1-niveaus; wanneer c-Myc werd verhoogd, steeg GRPEL1. Tumormonsters van patiënten lieten ook zien dat c-Myc en GRPEL1 vaak tegelijkertijd hoog zijn, en beide gepaard gaan met slechtere uitkomsten. In in vitro gekweekte PDAC-cellen vertraagde het verlagen van GRPEL1 de celdeling en koloniegroei, terwijl extra GRPEL1 de proliferatie versnelde, vooral wanneer c-Myc anderszins was geremd.
Van mitochondriën naar vetproductie
Dieper gravend vonden de onderzoekers dat GRPEL1 meer doet dan alleen mitochondriale eiwitten op orde houden. Wanneer GRPEL1 werd uitgeput, werden mitochondriën in PDAC-cellen minder efficiënt in energieproductie, verloren ze hun normale vorm en gaven ze meer reactieve zuurstofsoorten (ROS) vrij — chemisch reactieve bijproducten die soms als cellulair "roest" worden aangeduid. Deze toename van ROS had een kettingreactie tot gevolg: het verlaagde de niveaus van fatty acid synthase (FASN), een sleutelenzym dat nieuwe vetzuren in de cel opbouwt. Met minder FASN maakten de cellen minder vetten, sloegen ze minder lipiden op en vertraagde hun groei. Toen de onderzoekers ROS wegvingen met een antioxidant, herstelden de FASN-niveaus zich, wat aantoont dat de GRPEL1–FASN-koppeling door ROS wordt aangestuurd. Interessant genoeg leek c-Myc zelf in dit systeem niet direct het FASN-gen aan te zetten, maar beïnvloedde het FASN indirect via GRPEL1 en mitochondriale stress.
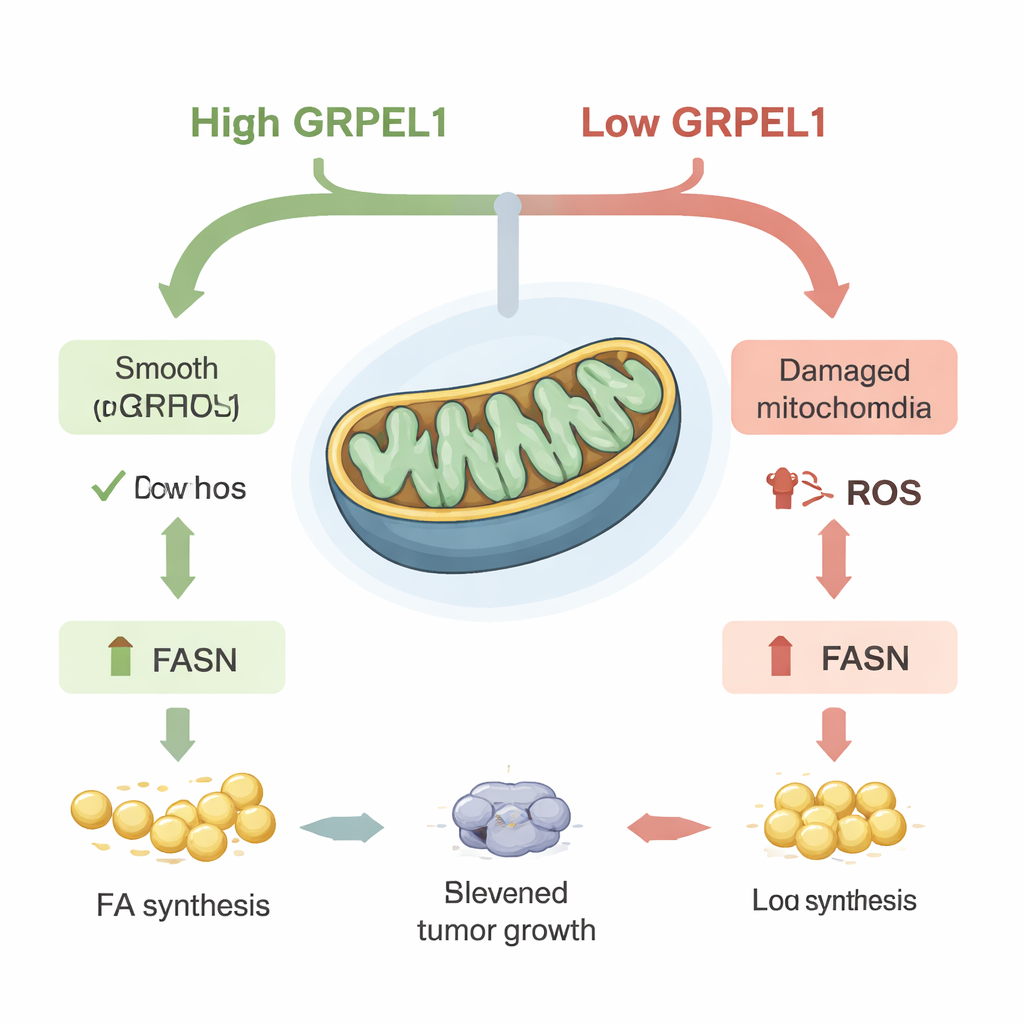
Vet als brandstof voor tumorengroei
Aangezien FASN centraal staat in vetopbouw, vroegen de wetenschappers zich af of het herstellen van FASN de tumorgroei kon redden wanneer GRPEL1 laag was. In celkweken keerde het forceren van extra FASN deels de groeivertraging en verminderde kolonieformatie ten gevolge van verlies van GRPEL1 om. Hetzelfde gold in muizen: tumoren gevormd uit GRPEL1-uitgeputte cellen groeiden langzamer, maar het opnieuw introduceren van FASN herstelde zowel tumorgrootte als vetinhoud. Gedetailleerde analyses van metabolieten en lipiden toonden brede dalingen in veel vetgerelateerde stoffen wanneer GRPEL1 of c-Myc werden gereduceerd. Belangrijker nog, het toedienen van extra vetzuren of een lipidenmengsel van buitenaf herstelde deels de groei in zowel kankecellijnen als patiënt-afgeleide pancreaskanker-organoïden — mini-tumoren gekweekt in 3D — wat suggereert dat het belangrijkste probleem het verlies van nieuw gemaakte vetten was.
Een kwetsbaarheid omzetten in therapie
Al met al schetst het werk een helder beeld: in pancreaskanker zet c-Myc GRPEL1 aan, wat helpt mitochondriën soepel te laten draaien en ROS onder controle te houden. Deze rustige mitochondriale toestand stelt cellen in staat hoge FASN-niveaus te behouden, waardoor ze nieuwe vetzuren produceren die dienen als bouwstenen voor membranen, energiereserves en groeisignalen. Wanneer GRPEL1 wordt geblokkeerd, falen mitochondriën, stijgt ROS, daalt FASN en krijgen de kankercellen moeite met groeien — een effect dat deels kan worden omzeild als vetten van buitenaf worden aangeleverd. Voor het brede publiek is de conclusie dat pancreastumoren afhankelijk zijn van een intern “vetfabriek”-circuit, aangedreven door c-Myc, GRPEL1 en FASN. Geneesmiddelen die deze vetzuurmaak-as verstoren, vooral in tumoren waarin deze sterk actief is, zouden een veelbelovende manier kunnen bieden om pancreaskankercellen uit te hongeren terwijl normale weefsels minder worden aangetast.
Bronvermelding: Wang, J., Zhang, L., Chen, K. et al. c-Myc/GRPEL1 maintains fatty acid synthesis via FASN to support PDAC cell proliferation. Cell Death Dis 17, 205 (2026). https://doi.org/10.1038/s41419-026-08439-0
Trefwoorden: pancreaskanker, tumormetabolisme, vetzuursynthese, mitochondriën, c-Myc